用软锰矿(主要成分为 ,含少量
,含少量 、
、 )和
)和 制备高纯
制备高纯 的工艺流程如下:
的工艺流程如下:

已知: 是一种两性氧化物;
是一种两性氧化物; 时相关物质的
时相关物质的 见下表。
见下表。
回答下列问题:
(1)①净化时需先加入的试剂 为
为_______ (填化学式),再使用氨水调溶液的 ,则
,则 的理论最小值为
的理论最小值为_______ (当溶液中某离子浓度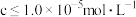 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
②碳化过程中发生反应的离子方程式为_______ 。
(2)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料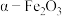 。其主要实验流程如下:
。其主要实验流程如下:
除杂:向“还原”后的滤液中加入 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的
沉淀除去。若溶液的 偏低,将会导致
偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是_______ [ ,
, ]。
]。
 ,含少量
,含少量 、
、 )和
)和 制备高纯
制备高纯 的工艺流程如下:
的工艺流程如下:
已知:
 是一种两性氧化物;
是一种两性氧化物; 时相关物质的
时相关物质的 见下表。
见下表。| 物质 |  |  |  |  |
 | 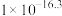 | 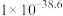 | 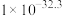 |  |
回答下列问题:
(1)①净化时需先加入的试剂
 为
为 ,则
,则 的理论最小值为
的理论最小值为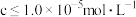 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。②碳化过程中发生反应的离子方程式为
(2)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料
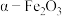 。其主要实验流程如下:
。其主要实验流程如下:
除杂:向“还原”后的滤液中加入
 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的
沉淀除去。若溶液的 偏低,将会导致
偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是 ,
, ]。
]。
21-22高二·全国·课时练习 查看更多[1]
更新时间:2022-09-08 14:28:53
|
相似题推荐
【推荐1】镍酸锂(LiNiO2)是一种具有潜力的锂离子电池材料。以镍催化剂废渣(主要成分是Ni,含少量Zn、Fe、CaO、SiO2等杂质)为原料制备镍酸锂的流程如下。

请回答下列问题:
(1)LiNiO2中镍的化合价为_______ 。
(2)在实验室中,“萃取、分液”需要的仪器有_______ (填字母)。

(3)如果加入足量次氯酸钠溶液“除铁”,则“除铁”反应的离子方程式为_______ 。
(4)“除钙”操作不能在玻璃仪器中进行,其原因是_______ 。
(5)有人认为“除钙”中可以用HF替代NH4F,则“除钙”反应Ca2+(aq)+2HF(aq) CaF2(s)+2H+(aq)的平衡常数K=
CaF2(s)+2H+(aq)的平衡常数K=_______ [已知:室温下,HF的电离常数Ka=4.0×10-4,Ksp(CaF2)=1.6×10-10]。
(6)“酸浸”中镍浸出率与液固比(稀硫酸浓度一定时溶液体积与镍渣质量之比)的关系如图1所示,最佳液固比为_______ 。当液固比一定时,镍浸出率与温度的关系如图2所示,40℃之前,随着温度升高,镍浸出率逐渐增大的主要原因是_______ 。

(7)用3NiCO3·2Ni(OH)2·H2O制备镍酸锂的化学方程式为_______ 。

请回答下列问题:
(1)LiNiO2中镍的化合价为
(2)在实验室中,“萃取、分液”需要的仪器有

(3)如果加入足量次氯酸钠溶液“除铁”,则“除铁”反应的离子方程式为
(4)“除钙”操作不能在玻璃仪器中进行,其原因是
(5)有人认为“除钙”中可以用HF替代NH4F,则“除钙”反应Ca2+(aq)+2HF(aq)
 CaF2(s)+2H+(aq)的平衡常数K=
CaF2(s)+2H+(aq)的平衡常数K=(6)“酸浸”中镍浸出率与液固比(稀硫酸浓度一定时溶液体积与镍渣质量之比)的关系如图1所示,最佳液固比为

(7)用3NiCO3·2Ni(OH)2·H2O制备镍酸锂的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】水合肼(N2H4·H2O)是一种精细化工原料,常用于医药、农药、染料、航天等领域。实验室模拟尿素法制备N2H4·H2O,并进一步制取副产品Na2SO3的流程如图所示。
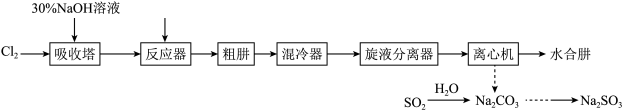
已知:①N2H4·H2O具有强还原性,易被氧化成N2;
②一定条件下,碱性NaClO溶液与尿素溶液反应生或主要产物中有N2H4·H2O和Na2CO3;
③尿素中氮元素为-3价。
回答下列问题
(1)吸收塔内发生反应的离子方程式为_______________________ 。
(2)为提高吸收塔内NaOH的有效利用率,将二氧化锰和浓盐酸制取的Cl2通入吸收塔前应进行的操作是_________________ ,选用的试剂是______________ 。
(3)反应器内生成水合肼的化学方程式为____________________ 。
(4)制备过程中要控制反应器内NaClO溶液的供给量不能过量,其主要目的是____________________ 。

已知:①N2H4·H2O具有强还原性,易被氧化成N2;
②一定条件下,碱性NaClO溶液与尿素溶液反应生或主要产物中有N2H4·H2O和Na2CO3;
③尿素中氮元素为-3价。
回答下列问题
(1)吸收塔内发生反应的离子方程式为
(2)为提高吸收塔内NaOH的有效利用率,将二氧化锰和浓盐酸制取的Cl2通入吸收塔前应进行的操作是
(3)反应器内生成水合肼的化学方程式为
(4)制备过程中要控制反应器内NaClO溶液的供给量不能过量,其主要目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】陶瓷工业中钴系色釉具有呈色稳定、呈色强度高等优点。利用含钴废料(主要成分Co3O4,还含有Fe、Al、Cu等杂质)为原料回收复合氧化钴的工艺流程如图:

回答下列问题:
(1)“碱溶”所得溶液a中含有的阴离子为______ 。
(2)“氧化”步骤发生反应的离子方程式为______ 。确定氧化反应是否反应完全可选择的试剂是______ (填字母)。
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN溶液 D.铁粉
(3)向溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10-5mol•L-1],应控制C2O 的浓度不小于
的浓度不小于_____ mol•L-1。[Ksp(CoC2O4)=6.3×10-8]
(4)某小组设计钴硫液流电池,电池总反应为:2Co3++SO +H2O
+H2O Co2++SO
Co2++SO +2H+,其结构如图所示:(已知电解液均为200mL)
+2H+,其结构如图所示:(已知电解液均为200mL)

①充电时,阳极发生的是______ (填“氧化”或“还原”)反应。
②放电时,电池的负极反应式为______ 。
③充分放电后SO 的浓度为0.4mol•L-1,此时对电池进行充电,电路中通过0.1mol电子时,理论上充电完成率为
的浓度为0.4mol•L-1,此时对电池进行充电,电路中通过0.1mol电子时,理论上充电完成率为_____ 。

回答下列问题:
(1)“碱溶”所得溶液a中含有的阴离子为
(2)“氧化”步骤发生反应的离子方程式为
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN溶液 D.铁粉
(3)向溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10-5mol•L-1],应控制C2O
 的浓度不小于
的浓度不小于(4)某小组设计钴硫液流电池,电池总反应为:2Co3++SO
 +H2O
+H2O Co2++SO
Co2++SO +2H+,其结构如图所示:(已知电解液均为200mL)
+2H+,其结构如图所示:(已知电解液均为200mL)
①充电时,阳极发生的是
②放电时,电池的负极反应式为
③充分放电后SO
 的浓度为0.4mol•L-1,此时对电池进行充电,电路中通过0.1mol电子时,理论上充电完成率为
的浓度为0.4mol•L-1,此时对电池进行充电,电路中通过0.1mol电子时,理论上充电完成率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】ZnO是一种难溶于水的白色固体,在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上由菱锌矿(主要成分为 、ZnO,还含有少量
、ZnO,还含有少量 、FeO、
、FeO、 、
、 等杂质)制备ZnO的工艺流程如图所示:
等杂质)制备ZnO的工艺流程如图所示: ,
,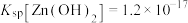 ;
;
②“溶浸”后的溶液所含金属离子主要有: 、
、 、
、 、
、 ;
;
③氧化性顺序: 。
。
回答下列问题:
(1)基态Zn原子的最高能层符号为__________ 。
(2)滤渣1的化学式是__________ ,“溶浸”过程中 发生反应的离子方程式是
发生反应的离子方程式是__________ 。
(3)“氧化”时适当加热,其目的是__________ ,但温度不能过高,其原因是__________ 。
(4)已知“氧化”后溶液中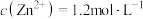 ,“调pH”的pH范围是
,“调pH”的pH范围是__________ (保留两位有效数字)。(已知:溶液中离子浓度小于等于 时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是
时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是__________ 。
(5)有机萃取剂HA与 反应的化学方程式为
反应的化学方程式为 ,则“反萃取”时加入试剂X的化学式是
,则“反萃取”时加入试剂X的化学式是__________ 。
(6)在“沉锌”与“灼烧”之间进行的操作是__________ ,“沉锌”得到碱式碳酸锌[化学式为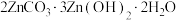 ],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是
],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是__________ (填化学式)。
 、ZnO,还含有少量
、ZnO,还含有少量 、FeO、
、FeO、 、
、 等杂质)制备ZnO的工艺流程如图所示:
等杂质)制备ZnO的工艺流程如图所示: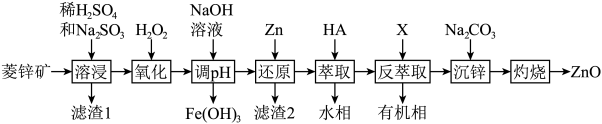
 ,
,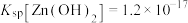 ;
;②“溶浸”后的溶液所含金属离子主要有:
 、
、 、
、 、
、 ;
;③氧化性顺序:
 。
。回答下列问题:
(1)基态Zn原子的最高能层符号为
(2)滤渣1的化学式是
 发生反应的离子方程式是
发生反应的离子方程式是(3)“氧化”时适当加热,其目的是
(4)已知“氧化”后溶液中
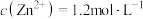 ,“调pH”的pH范围是
,“调pH”的pH范围是 时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是
时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是(5)有机萃取剂HA与
 反应的化学方程式为
反应的化学方程式为 ,则“反萃取”时加入试剂X的化学式是
,则“反萃取”时加入试剂X的化学式是(6)在“沉锌”与“灼烧”之间进行的操作是
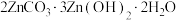 ],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是
],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是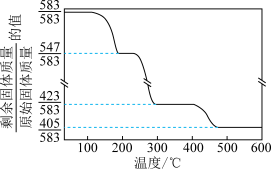
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】已知常温下:
① ,
, ,
, ,
, ;
;
②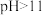 时,
时, 会转化为
会转化为 ;
;
③离子完全除去的标准:该离子浓度 。
。
某工业废水中含有 和
和 ,可采用沉淀法将其除去。
,可采用沉淀法将其除去。
(1)若加入 来沉淀
来沉淀 和
和 ,当溶液中
,当溶液中 和
和 共存时,
共存时,
___________ 。
(2)若加入 溶液来调节
溶液来调节 ,使
,使 和
和 完全沉淀,
完全沉淀, 应满足的范围为
应满足的范围为___________ 。
①
 ,
, ,
, ,
, ;
;②
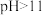 时,
时, 会转化为
会转化为 ;
;③离子完全除去的标准:该离子浓度
 。
。某工业废水中含有
 和
和 ,可采用沉淀法将其除去。
,可采用沉淀法将其除去。(1)若加入
 来沉淀
来沉淀 和
和 ,当溶液中
,当溶液中 和
和 共存时,
共存时,
(2)若加入
 溶液来调节
溶液来调节 ,使
,使 和
和 完全沉淀,
完全沉淀, 应满足的范围为
应满足的范围为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用。
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O="6Cu+" SO2
在③中被氧化与被还原元素原子的物质的量之比为____________ ;若由3mol CuFeS2生成3molCu,理论上消耗O2的物质的量为______________ 。
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式________________ 。
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:
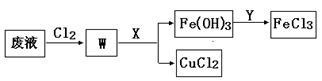
①试剂Y的名称___________ ;物质X最好是__________ (填化学式)。
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5mol·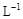 , 则加入Cl2气和物质X使溶液的pH在
, 则加入Cl2气和物质X使溶液的pH在________________ 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38、 KSP[Cu(OH)2]=2.0×10—20 、 lg5=0.7)
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O="6Cu+" SO2
在③中被氧化与被还原元素原子的物质的量之比为
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:

①试剂Y的名称
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5mol·
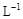 , 则加入Cl2气和物质X使溶液的pH在
, 则加入Cl2气和物质X使溶液的pH在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】一种高硫锰矿的主要成分为MnCO3和MnS,主要杂质为FeS、SiO2、CaCO3、Al2O3、MgO等,研究人员设计了如图流程,制备Mn3O4。
②Ksp(MgF2)=6.4×10-9、Ksp(CaF2)=4.0×10-11.
(1)“焙烧”的主要目的是___________ 。
(2)“酸浸”过程中,___________ (填“能”或“不能”)用盐酸替换硫酸。
(3)“氧化1”时,试剂a为MnO2,并控制溶液的pH=3,此时发生反应的离子方程式为___________ 。
(4)若省略“氧化”步骤直接进行“中和除杂”,则造成的影响是___________ 。
(5)“净化除杂”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=1.0×10-5mol•L-1,则滤液中c(Ca2+)为___________ mol•L-1.
(6)“氧化2”过程中,在MnSO4溶液中滴入一定浓度的氮水,加压通入空气反应7小时制备Mn3O4,此时发生反应的离子方程式为___________ 。
(7)锰的一种氧化物晶胞结构如图所示:___________ ,该晶胞的密度为___________ g•cm-3(列出计算式,设NA为阿伏加德罗常数的值,晶胞底面边长为apm,高为bpm)。

| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉定的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“焙烧”的主要目的是
(2)“酸浸”过程中,
(3)“氧化1”时,试剂a为MnO2,并控制溶液的pH=3,此时发生反应的离子方程式为
(4)若省略“氧化”步骤直接进行“中和除杂”,则造成的影响是
(5)“净化除杂”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=1.0×10-5mol•L-1,则滤液中c(Ca2+)为
(6)“氧化2”过程中,在MnSO4溶液中滴入一定浓度的氮水,加压通入空气反应7小时制备Mn3O4,此时发生反应的离子方程式为
(7)锰的一种氧化物晶胞结构如图所示:

您最近一年使用:0次
【推荐2】以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取精银、Mn及MnO2的一种流程示意图如下。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是_______ 。
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有_______ 。
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整:_______ 。
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:_______ 。
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:
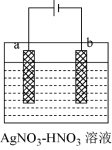
①_______ 极为“粗银电极”(填“a”或“b”)。
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为_______ ;当电路中通过0.025NA电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为_______ mL(保留三位有效数字)。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以
 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整:
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:

①
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锰酸锂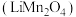 作为一种新型锂电池正极材料受到广泛关注。工业上利用
作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如下,回答下列问题:
溶液多途径制备锰酸锂的流程如下,回答下列问题:

已知:①硫酸的结构为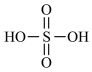
②干冰的晶胞结构见图。
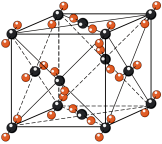
(1)将干冰晶胞沿体对角线投影,●代表 分子,则
分子,则 的投影图为______(选填序号)
的投影图为______(选填序号)
(2)工艺1中, 中S元素的化合价为
中S元素的化合价为 ,画出
,画出 的结构式
的结构式______ 。
(3)工艺2中,发生电解反应的离子方程式为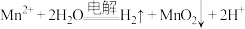 。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入
。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入______ (填化学式)。
(4)工艺3中,“沉锰、过滤”得到 和
和 ;若“控温、氧化”时溶液的pH显著减小,此时
;若“控温、氧化”时溶液的pH显著减小,此时 发生反应的化学方程式为
发生反应的化学方程式为______ 。
(5)为控制碳排放,用NaOH溶液吸收焙烧窑中释放的 并转化为正盐,理论上消耗的
并转化为正盐,理论上消耗的 和NaOH的物质的量之比为
和NaOH的物质的量之比为______ 。
 作为一种新型锂电池正极材料受到广泛关注。工业上利用
作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如下,回答下列问题:
溶液多途径制备锰酸锂的流程如下,回答下列问题:
已知:①硫酸的结构为

②干冰的晶胞结构见图。

(1)将干冰晶胞沿体对角线投影,●代表
 分子,则
分子,则 的投影图为______(选填序号)
的投影图为______(选填序号)A.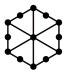 | B.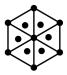 |
C.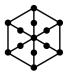 | D.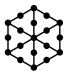 |
(2)工艺1中,
 中S元素的化合价为
中S元素的化合价为 ,画出
,画出 的结构式
的结构式(3)工艺2中,发生电解反应的离子方程式为
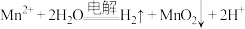 。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入
。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入(4)工艺3中,“沉锰、过滤”得到
 和
和 ;若“控温、氧化”时溶液的pH显著减小,此时
;若“控温、氧化”时溶液的pH显著减小,此时 发生反应的化学方程式为
发生反应的化学方程式为(5)为控制碳排放,用NaOH溶液吸收焙烧窑中释放的
 并转化为正盐,理论上消耗的
并转化为正盐,理论上消耗的 和NaOH的物质的量之比为
和NaOH的物质的量之比为
您最近一年使用:0次



