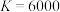已知某温度时Ksp(BaSO4)=1.0×10-10,在该温度下BaSO4与BaCO3沉淀溶解平衡曲线如图所示,下列说法不正确的是
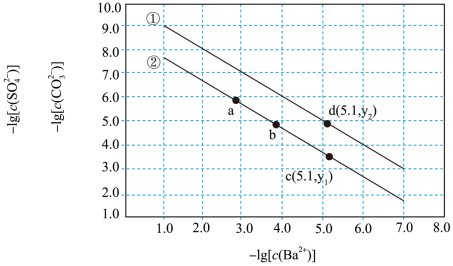

| A.曲线①表示BaSO4的饱和溶液 |
| B.加适量BaCl2固体可使溶液由b点变到a点 |
C.相同浓度的SO 、CO 、CO 混合液中滴加BaCl2溶液,先生成BaSO4沉淀 混合液中滴加BaCl2溶液,先生成BaSO4沉淀 |
D.c(Ba2+)=10−5.1mol•L-1时两溶液中 |
更新时间:2022-09-21 08:19:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知常温下:Ksp〔Mg(OH)2〕=1.2×10-11,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,Ksp(CH3COOAg)=2.3×10-3,下列叙述正确的是
| A.等体积混合浓度均为0.2 mol•L-1的AgNO3溶液和CH3COONa溶液一定不产生CH3COOAg沉淀 |
| B.将0.001 mol•L-1的AgNO3溶液滴入0.001 mol•L-1的KCl和0.001 mol•L-1的K2CrO4溶液中先产生Ag2CrO4沉淀 |
| C.在Mg2+为0.12 mol•L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上 |
| D.向1ml 0.1 mol•L-1AgNO3溶液中加入2滴0.1 mol•L-1NaCl溶液产生白色沉淀,再滴加2滴0.1 mol•L-1KI溶液,又产生黄色沉淀,证明相同温度下Ksp(AgCl)大于Ksp(AgI) |
您最近一年使用:0次
【推荐2】25℃时,用 的NaCl溶液滴定25.00mL
的NaCl溶液滴定25.00mL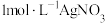 溶液的滴定曲线如图所示,
溶液的滴定曲线如图所示,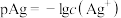 ,
,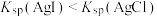 。下列有关叙述错误的是
。下列有关叙述错误的是

 的NaCl溶液滴定25.00mL
的NaCl溶液滴定25.00mL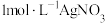 溶液的滴定曲线如图所示,
溶液的滴定曲线如图所示,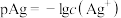 ,
,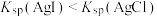 。下列有关叙述错误的是
。下列有关叙述错误的是
A.25℃时, |
| B.x点的横坐标为12.5 |
C.当滴入25.00mLNaCl溶液时,溶液中 |
D.相同条件下,若改为 的NaI溶液,反应终点的纵坐标值会增大 的NaI溶液,反应终点的纵坐标值会增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于难溶盐MX,其饱和溶液Mn+和Xn-的离子的物质的量浓度之间的关系近似于水的离子积Kw(Kw=[H+][OH-]),存在着[Mn+] [Xn-]=Ksp的关系(Ksp为常数).现将足量的AgCl固体分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是
①20mL0.1mol/L(NH4)2CO3 溶液②40 mL 0.03 mol/LHCl ③50mL0.05mol/L AgNO3溶液 ④30mL0.02mol/ LCaCl2溶液 ⑤10 mL蒸馏水 ⑥30mL0.02mol/LNH4NO3溶液
①20mL0.1mol/L(NH4)2CO3 溶液②40 mL 0.03 mol/LHCl ③50mL0.05mol/L AgNO3溶液 ④30mL0.02mol/ LCaCl2溶液 ⑤10 mL蒸馏水 ⑥30mL0.02mol/LNH4NO3溶液
| A.⑤>②>④>③>⑥>① | B.①>⑥>⑤>②>④>③ |
| C.①>②>③>④>⑤>⑥ | D.③>②>④>⑥>①>⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列对沉淀溶解平衡的描述正确的是
| A.电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 |
| B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 |
| C.沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变 |
| D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】以磷石膏(含CaSO4和少量SiO2等)为原料制备轻质CaCO3的部分流程如图12图所示。室温下,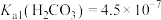 ,
,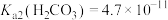 ,
, 。
。
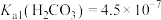 ,
,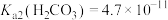 ,
, 。
。
A. 溶液中: 溶液中: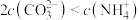 |
B.室温下,pH=6的NH4Cl溶液中: |
C.“转化”后的清液中一定存在 |
D.“浸取”发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
A. 和 和 溶于水后均能导电,故 溶于水后均能导电,故 和 和 均为电解质 均为电解质 |
B.高炉炼铁中焦炭直接将 还原成铁 还原成铁 |
C.相同条件下, ,故 ,故 沉淀易转化成 沉淀易转化成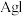 沉淀 沉淀 |
D. 能溶于 能溶于 溶液,也能溶于氢氟酸,所以是两性氧化物 溶液,也能溶于氢氟酸,所以是两性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知常温下,Ksp(NiS)≈1.0×10-21,Ksp(ZnS)≈1.0×10-25,pM=-lgc(M2+)。向20mL0.1mol·L-1NiCl2溶液中滴加0.1mol·L-1Na2S溶液,溶液中pM与Na2S溶液体积的关系如图所示,下列说法正确的是( )


| A.图象中,V0=40,b=10.5 |
| B.若NiCl2(aq)变为0.2mol·L-1,则b点向a点迁移 |
| C.若用同浓度ZnCl2溶液替代NiCl2溶液,则d点向f点迁移 |
| D.Na2S溶液中存在c(OH-)=c(H+)+c(HS-)+c(H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知 时,
时,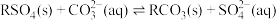 的平衡常数
的平衡常数 ,
,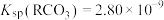 ,下列叙述中正确的是
,下列叙述中正确的是
 时,
时,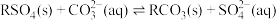 的平衡常数
的平衡常数 ,
,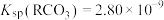 ,下列叙述中正确的是
,下列叙述中正确的是A. 时, 时, 的 的 的为 的为 |
B.将浓度均为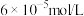 的 的 、 、 溶液等体积混合后可得到 溶液等体积混合后可得到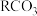 沉淀 沉淀 |
C.向 的混合液中滴加 的混合液中滴加 溶液,首先析出 溶液,首先析出 沉淀 沉淀 |
D.相同温度下,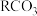 在水中的 在水中的 大于在 大于在 溶液中的 溶液中的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温时,用0.100 的标准
的标准 溶液滴定25.00mL浓度相等的
溶液滴定25.00mL浓度相等的 、
、 和
和 混合溶液,通过电位滴定法获得
混合溶液,通过电位滴定法获得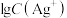 与
与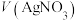 的关系曲线如图所示(忽略沉淀对离子的吸附作用)。若溶液中离子浓度小于
的关系曲线如图所示(忽略沉淀对离子的吸附作用)。若溶液中离子浓度小于 时,认为该离子沉淀完全。已知
时,认为该离子沉淀完全。已知 ,
,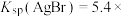
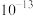 ,
, 。下列说法不正确的是
。下列说法不正确的是

 的标准
的标准 溶液滴定25.00mL浓度相等的
溶液滴定25.00mL浓度相等的 、
、 和
和 混合溶液,通过电位滴定法获得
混合溶液,通过电位滴定法获得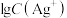 与
与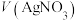 的关系曲线如图所示(忽略沉淀对离子的吸附作用)。若溶液中离子浓度小于
的关系曲线如图所示(忽略沉淀对离子的吸附作用)。若溶液中离子浓度小于 时,认为该离子沉淀完全。已知
时,认为该离子沉淀完全。已知 ,
,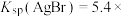
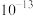 ,
, 。下列说法不正确的是
。下列说法不正确的是
| A.a点:有AgI沉淀生成 |
B.原溶液中 的浓度为0.0600 的浓度为0.0600 |
C.当 沉淀完全时,已经有部分 沉淀完全时,已经有部分 沉淀 沉淀 |
D.b点: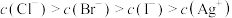 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】要除去CuCl2溶液中的Fe3+ ,甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过调节溶液pH除去Fe3+而不损失Cu2+,调节pH的取值范围
| A.3≤pH<4 | B.3≤pH≤4 |
| C.2<pH≤3 | D.2≤pH<3 |
您最近一年使用:0次

 ,
,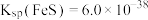 ,其沉淀溶解平衡曲线如图所示
,其沉淀溶解平衡曲线如图所示 图中R表示Ni或
图中R表示Ni或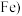 。下列说法正确的是
。下列说法正确的是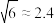 ,
,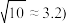

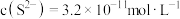
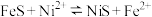 的平衡常数
的平衡常数