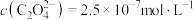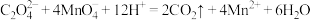要除去CuCl2溶液中的Fe3+ ,甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过调节溶液pH除去Fe3+而不损失Cu2+,调节pH的取值范围
| A.3≤pH<4 | B.3≤pH≤4 |
| C.2<pH≤3 | D.2≤pH<3 |
更新时间:2024/03/27 22:42:22
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知常温下 的某一元酸
的某一元酸 溶液中
溶液中 ,下列叙述错误的是
,下列叙述错误的是
 的某一元酸
的某一元酸 溶液中
溶液中 ,下列叙述错误的是
,下列叙述错误的是A.常温下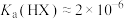 |
| B.加水稀释促进电离,溶液的pH减小 |
C.升高温度后, 均增大 均增大 |
D.加入少量NaOH固体,溶液中 减小但 减小但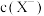 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在不同温度下的水溶液中离子浓度曲线如图所示,下列说法错误的是( )
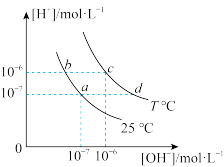

| A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH3COO-) |
B.b点对应的溶液中大量存在:K+、Ba2+、NO 、I- 、I- |
| C.T ℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
| D.加热a点对应的溶液,可能引起由a向c的变化 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。下列说法不正确的是
| A.2.8gN2与CO混合气体中含有原子数目为0.2NA |
| B.0.1mol氯气分别与足量铁和铜完全反应时转移的电子数均为0.2NA |
| C.16.9g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA |
| D.1LpH=1的H2SO4溶液中含有H+的数目为0.1NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3-),维持血液的pH保持稳定。已知在人体正常体温时,反应H2CO3 HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
 HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是| A.正常人血液内Kw=10-14 |
| B.由题给数据可算得正常人血液的pH约为7.4 |
| C.正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.当过量的碱进入血液中时,只有发生HCO3-+OH-=CO32-+H2O的反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
A.常温下, 的氨水中,由水电离出的 的氨水中,由水电离出的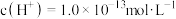 |
B. 与 与 的 的 溶液中, 溶液中, 之比为 之比为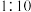 |
C.常温下, 的NaOH溶液和 的NaOH溶液和 的 的 溶液等体积混合,混合后溶液的 溶液等体积混合,混合后溶液的 . . |
D. 时,完全中和50mLpH=3的盐酸,需要25mLpH=11的 时,完全中和50mLpH=3的盐酸,需要25mLpH=11的 溶液 溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
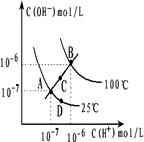
【推荐1】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lg c(SO42-)。下列说法正确的是( )
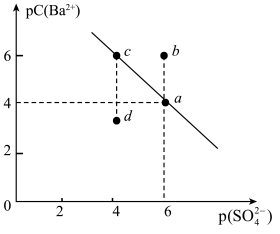

| A.加入BaCl2可以使溶液由c点变到a点 |
| B.a点的Ksp(BaSO4)小于b点的Ksp(BaSO4) |
| C.d点表示的是该温度下BaSO4的不饱和溶液 |
| D.该温度下,Ksp(BaSO4)=1.0×10-24 |
您最近半年使用:0次
【推荐2】某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白( )和黄金雨中黄色的
)和黄金雨中黄色的 。室温下
。室温下 和
和 在不同的溶液中分别达到溶解平衡时,
在不同的溶液中分别达到溶解平衡时,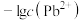 与
与 或
或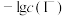 的关系如图所示:
的关系如图所示:
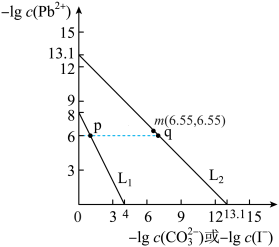
下列说法错误的是
 )和黄金雨中黄色的
)和黄金雨中黄色的 。室温下
。室温下 和
和 在不同的溶液中分别达到溶解平衡时,
在不同的溶液中分别达到溶解平衡时,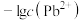 与
与 或
或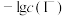 的关系如图所示:
的关系如图所示:
下列说法错误的是
A.L1对应的是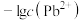 与 与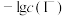 的关系变化 的关系变化 |
B.p点 的结晶速率小于其溶解速率 的结晶速率小于其溶解速率 |
C.将 浸泡到饱和KI溶液中几乎不能转化为 浸泡到饱和KI溶液中几乎不能转化为 |
| D.q点是L2对应溶液的悬浊液,通过加水可以使浊液由q点向m点方向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,在Co(NO3)2、Pb(NO3)2和HR混合液中滴加NaOH溶液,pM与pH的关系如图所示,已知: ,c(M)代表
,c(M)代表 、
、 或
或 ,
,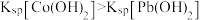 。下列叙述错误的是
。下列叙述错误的是

 ,c(M)代表
,c(M)代表 、
、 或
或 ,
,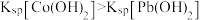 。下列叙述错误的是
。下列叙述错误的是
A.②代表 与pH的关系 与pH的关系 |
B.当溶液中c(Pb2+)=1mol/L时, |
| C.图中a点的pH为6.5 |
D.常温下, 的平衡常数K的数值为0.01 的平衡常数K的数值为0.01 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴、锂。Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.9g和1.3g。
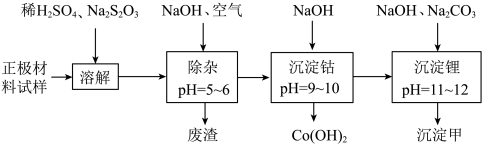
下列说法正确的是( )

下列说法正确的是( )
| A.沉淀甲是LiOH |
| B.在上述溶解过程,Na2S2O3、LiCoO2反应的化学方程式为8LiCoO2+Na2S2O3+11H2SO4===4Li2SO4+8CoSO4+Na2SO4+11H2O |
| C.已知:常温下Ksp[Co(OH)2]=1.58×10-15。沉淀钴过程中,当溶液pH=10时,溶液中c(Co2+)=1.58×10-11mol·L-1 |
| D.分离沉淀所需要的玻璃仪器主要是分液漏斗 |
您最近半年使用:0次

 ,
,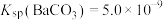 ,下列叙述中正确的是
,下列叙述中正确的是 固体的悬浊液中加入少量
固体的悬浊液中加入少量 固体,
固体,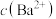 不变
不变 溶液,一定不发生
溶液,一定不发生
 溶液滴入
溶液滴入 溶液,得到白色沉淀,再滴加
溶液,得到白色沉淀,再滴加 溶液,出现红褐色沉淀,证明
溶液,出现红褐色沉淀,证明
 浓溶液使其溶解,可能是
浓溶液使其溶解,可能是 导致沉淀溶解
导致沉淀溶解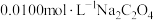 溶液的性质。
溶液的性质。 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。 溶液,出现白色沉淀。
溶液,出现白色沉淀。 溶液中滴加
溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。 ,下列说法错误的是
,下列说法错误的是