请回答下列问题。
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH=_______ (请用含有ΔH1、ΔH2的式子表示)。
(2)若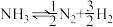 K=a,则N2+3H2
K=a,则N2+3H2 2NH3 K′=
2NH3 K′=_______ (用含a的式子表示)。
(3)在体积为3 L的恒容密闭容器中,进行合成氨N2+3H2 2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1_______ (填“>”“<”或“=”)T2。
②在T2下,经过10 min达到化学平衡状态,平衡时N2的转化率α(N2)=_______ 和K =_______ (分数表示)。
③下列图象分别代表焓变(ΔH)、混合气体平均相对分子质量(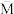 )、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是
)、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是_______ (填字母)。
A.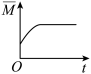 B.
B. 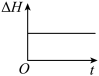 C.
C. 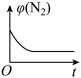 D.
D. 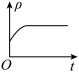
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH=
(2)若
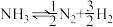 K=a,则N2+3H2
K=a,则N2+3H2 2NH3 K′=
2NH3 K′=(3)在体积为3 L的恒容密闭容器中,进行合成氨N2+3H2
 2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:| 温度/K | 平衡时NH3的物质的量/mol |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1
②在T2下,经过10 min达到化学平衡状态,平衡时N2的转化率α(N2)=
③下列图象分别代表焓变(ΔH)、混合气体平均相对分子质量(
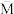 )、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是
)、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是A.
 B.
B.  C.
C.  D.
D. 
更新时间:2022-09-15 18:37:26
|
相似题推荐
【推荐1】载人航天器中,可将航天员呼出的CO2转化为 H2O,再通过电解 H2O 获得 O2,实现 O2的再 生,同时还能制备 CH4.已知:
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于_______ (填“吸热”或“放热”)反应。
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =_______ kJ/mol。
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
①已知2CH4(g)=C2H4(g)+2H2(g) ΔH =+167kJ/mol,则a=_______ 。
②已知5C2H4(g)+12 (aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为
(aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为_______ mol。(用含m、n 的代数式表示)
③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图
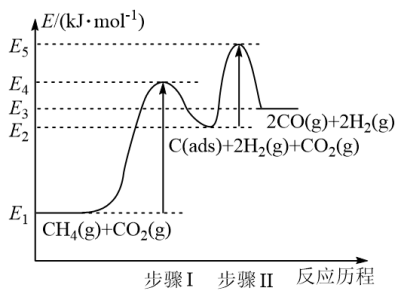
E4-E1表示步骤Ⅰ正反应的_______ ,制备合成气反应可在_______ (填“高温” 或“低温”)下自发进行。
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5C2H4(g)+12
 (aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为
(aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图

E4-E1表示步骤Ⅰ正反应的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】为缓解能源紧张,越来越多的国家开始重视生物质能源(利用能源作物和有机废料,经过加工转变为生物燃料的一种能源)的开发利用。
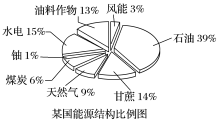
(1)如图是某国能源结构比例图,其中生物质能源所占的比例是__ 。
(2)生物柴油是由动植物油脂转化而来,其主要成分为脂肪酸酯,几乎不含硫,生物降解性好,一些国家已将其添加在普通柴油中使用。关于生物柴油及其使用,下列说法正确的是__ 。
①生物柴油是可再生资源②可减少二氧化硫的排放③与普通柴油相比易分解④与普通柴油制取方法相同
A.①②③ B.①②④ C.①③④ D.②③④
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ∙mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ∙mol-1
写出表示甲醇燃烧热的热化学方程式__ 。
(4)已知1g氢气完全燃烧生成液态水时放出热量143kJ,18g水蒸气变成液态水放出44kJ的热量。其他相关数据如表:
则表中x为( ) 。
(5)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g)⇌Y(g)+3Z(g)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为___ 。

(1)如图是某国能源结构比例图,其中生物质能源所占的比例是
(2)生物柴油是由动植物油脂转化而来,其主要成分为脂肪酸酯,几乎不含硫,生物降解性好,一些国家已将其添加在普通柴油中使用。关于生物柴油及其使用,下列说法正确的是
①生物柴油是可再生资源②可减少二氧化硫的排放③与普通柴油相比易分解④与普通柴油制取方法相同
A.①②③ B.①②④ C.①③④ D.②③④
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ∙mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ∙mol-1
写出表示甲醇燃烧热的热化学方程式
(4)已知1g氢气完全燃烧生成液态水时放出热量143kJ,18g水蒸气变成液态水放出44kJ的热量。其他相关数据如表:
| O=O | H—H | H—O(g) | |
| 1mol化学键断裂需要吸收的能量/kJ | 496 | 436 | x |
则表中x为
(5)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g)⇌Y(g)+3Z(g)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】以玉米淀粉为原料生产燃料乙醇的生产过程可由下图表示:
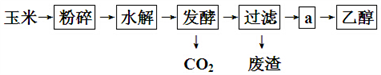
(1)乙醇分子中所含的官能团的名称为:__________________ ;
(2)过滤后得到a的主要成分为葡萄糖和乙醇,步骤a的操作是__________ ;
A.蒸发 B.萃取 C.蒸馏 D.分液
(3)生产过程中为了检验水解是否开始,可使用的试剂是______________ ;
(4)已知1g乙醇完全燃烧放出的热量为29.7kJ,请据此写出乙醇燃烧的热化学方程式:_______ 。
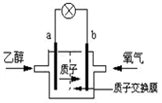
(5)为了充分利用乙醇的能量,科学家还把乙醇设计成燃料电池,如图,用磺酸类质子溶剂,在高温供电时,乙醇电池效率高且更安全。请判断,该电池的a极为电池的_______ 极(填“正”或“负”),b极的电极反应式为:____________________________ ,电池工作时,若有1mol乙醇被氧化,则转移的电子为____________ mol。

(1)乙醇分子中所含的官能团的名称为:
(2)过滤后得到a的主要成分为葡萄糖和乙醇,步骤a的操作是
A.蒸发 B.萃取 C.蒸馏 D.分液
(3)生产过程中为了检验水解是否开始,可使用的试剂是
(4)已知1g乙醇完全燃烧放出的热量为29.7kJ,请据此写出乙醇燃烧的热化学方程式:
(5)为了充分利用乙醇的能量,科学家还把乙醇设计成燃料电池,如图,用磺酸类质子溶剂,在高温供电时,乙醇电池效率高且更安全。请判断,该电池的a极为电池的

您最近一年使用:0次
【推荐1】工业上常用 和
和 合成甲醇,反应的化学方程式为
合成甲醇,反应的化学方程式为 ,该反应为放热反应。向容积为
,该反应为放热反应。向容积为 的刚性容器中通入一定量的
的刚性容器中通入一定量的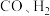 和
和 ,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。
,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。

根据上述信息回答下列问题。
(1)图中A物质为___________ ,反应开始至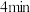 ,
, 的平均反应速率为
的平均反应速率为___________ 。
(2) 时,反应是否达到平衡状态?
时,反应是否达到平衡状态?___________ (填“是”或“否”);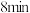 时该反应的正反应速率
时该反应的正反应速率___________ 逆反应速率(填“>”“<”或“=”,下同);该反应的反应物总能量___________ 生成物总能量。
(3)对于上述条件下的该反应,下列情况不能说明反应达到平衡状态的是_________
(4)对于反应 ,下述方法能加快反应速率的是_________
,下述方法能加快反应速率的是_________
(5)一种甲醇燃料电池的结构示意图如下:
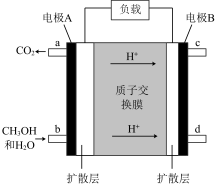
①电极 为
为___________ (填“正极”或“负极”),该电极的电极反应式为___________ 。
②若电路中转移 ,理论上正极消耗标准状况下氧气的体积为
,理论上正极消耗标准状况下氧气的体积为___________ L。
 和
和 合成甲醇,反应的化学方程式为
合成甲醇,反应的化学方程式为 ,该反应为放热反应。向容积为
,该反应为放热反应。向容积为 的刚性容器中通入一定量的
的刚性容器中通入一定量的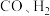 和
和 ,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。
,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。
根据上述信息回答下列问题。
(1)图中A物质为
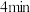 ,
, 的平均反应速率为
的平均反应速率为(2)
 时,反应是否达到平衡状态?
时,反应是否达到平衡状态?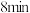 时该反应的正反应速率
时该反应的正反应速率(3)对于上述条件下的该反应,下列情况不能说明反应达到平衡状态的是_________
| A.气体的总物质的量不变 |
| B.气体的密度不变 |
| C.气体的平均相对分子质量不变 |
D.相同时间内,断裂 个 个 键,同时形成 键,同时形成 个 个 键 键 |
 ,下述方法能加快反应速率的是_________
,下述方法能加快反应速率的是_________| A.一定温度下,保持容器体积不变,通入稀有气体 |
| B.一定温度下,保持容器压强不变,通入稀有气体 |
C.一定温度下,保持容器体积不变,通入一定量的 气体 气体 |
| D.保持容器体积不变,升高温度 |

①电极
 为
为②若电路中转移
 ,理论上正极消耗标准状况下氧气的体积为
,理论上正极消耗标准状况下氧气的体积为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】工业合成氨反应为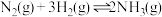 ,氨在工农业生产中应用广泛。
,氨在工农业生产中应用广泛。
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2mol 需要
需要_______ (填“放出”或“吸收”)kJ的热量。
(2)实验室中模拟合成氨过程,将1mol 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是_______ (填序号)。
a.反应不再进行,已经停止 b.单位时间内生成nmol 的同时,生成3nmol
的同时,生成3nmol
c.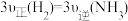 d.
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变 f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为_______ ;10min时的体系总压强与初始时的总压强之比为_______ 。
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
实际生产时,通常采用铁触媒作为催化剂、在400~500℃和10~30MPa的条件下合成氨。结合所学知识以及上述表格数据分析,工业上采用400~500℃反应的原因是_______ 。
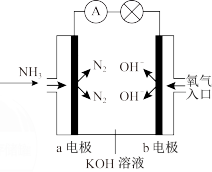
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。a电极的电极反应式是_______ 。
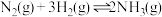 ,氨在工农业生产中应用广泛。
,氨在工农业生产中应用广泛。| 化学键 | H−H | N−H | N≡N |
键能( ) ) | 436 | 391 | 945.6 |
 需要
需要(2)实验室中模拟合成氨过程,将1mol
 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是a.反应不再进行,已经停止 b.单位时间内生成nmol
 的同时,生成3nmol
的同时,生成3nmol
c.
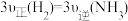 d.
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2e.混合气体的压强不再改变 f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
| 压强(MPa) 氨的平衡 含量(%) 温度(摄氏度) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。a电极的电极反应式是

您最近一年使用:0次
【推荐3】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
C(s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1。则CO还原Fe2O3(s)的热化学方程式为_____________ 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:_____________ 。
(3)①CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
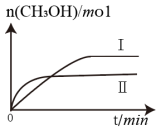
①曲线I、Ⅱ对应的温度大小关系为TⅠ__________ TⅡ(填“>”或“=”或“<”)。
②一定温度下,此反应在恒压 容器中进行,能判断该反应达到化学平衡状态的依据是______________ 。
a.容器中压强不变b.H2的体积分数不变c.c(H2)=3c(CH3OH)
d.容器中密度不变e.2个C=O断裂的同时有3个H-H断裂
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
C(s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1。则CO还原Fe2O3(s)的热化学方程式为
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:
(3)①CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。

①曲线I、Ⅱ对应的温度大小关系为TⅠ
②一定温度下,此反应在
a.容器中压强不变b.H2的体积分数不变c.c(H2)=3c(CH3OH)
d.容器中密度不变e.2个C=O断裂的同时有3个H-H断裂
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】 的回收与利用是科学家研究的热点课题,工业上有一种用
的回收与利用是科学家研究的热点课题,工业上有一种用 生产甲醇燃料的方法:
生产甲醇燃料的方法:
 kJ·mol
kJ·mol .将6 mol
.将6 mol  和8 mol
和8 mol  充入2 L的密闭容器中,测得的物质的量随时间变化如图所示(实线)。
充入2 L的密闭容器中,测得的物质的量随时间变化如图所示(实线)。
(1)已知
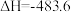 kJ·mol
kJ·mol .依据题中信息计算反应:
.依据题中信息计算反应: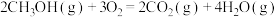

______ kJ·mol .
.
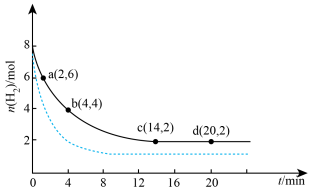
(2)a点正反应速率______ (填大于、等于或小于)逆反应速率,前4 min内,用 表示的平均反应速率为
表示的平均反应速率为______ mol·L ·min
·min 。
。
(3)平衡时氢气的转化率a=______ ,该条件下反应的平衡常数
______ 。
(4)二氧化碳催化加氢也可以合成乙烯,该反应是综合利用 的热点研究领域。
的热点研究领域。 催化加氢生成乙烯和水的反应中,产物的物质的量之比
催化加氢生成乙烯和水的反应中,产物的物质的量之比
______ 。当反应达到平衡时,若增大压强,则
______ (填“变大”“变小”或“不变”)。
 的回收与利用是科学家研究的热点课题,工业上有一种用
的回收与利用是科学家研究的热点课题,工业上有一种用 生产甲醇燃料的方法:
生产甲醇燃料的方法:
 kJ·mol
kJ·mol .将6 mol
.将6 mol  和8 mol
和8 mol  充入2 L的密闭容器中,测得的物质的量随时间变化如图所示(实线)。
充入2 L的密闭容器中,测得的物质的量随时间变化如图所示(实线)。(1)已知

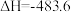 kJ·mol
kJ·mol .依据题中信息计算反应:
.依据题中信息计算反应: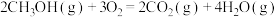

 .
.
(2)a点正反应速率
 表示的平均反应速率为
表示的平均反应速率为 ·min
·min 。
。(3)平衡时氢气的转化率a=

(4)二氧化碳催化加氢也可以合成乙烯,该反应是综合利用
 的热点研究领域。
的热点研究领域。 催化加氢生成乙烯和水的反应中,产物的物质的量之比
催化加氢生成乙烯和水的反应中,产物的物质的量之比

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】硫及其化合物在日常生活、工业生产中都非常普遍。
(1)SO2、H2S都是常见的污染性气体,具有一定的毒性。请再写出两种与酸雨、光化学烟雾和臭氧层空洞均有关的污染性气体:___________ 。
(2)变废为宝是治理污染的常用手段。以V2O5为催化剂,将SO2氧化为SO3,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
(i)SO2(g)+V2O5(s) SO3(g)+V2O4(s),活化能为Ea1。
SO3(g)+V2O4(s),活化能为Ea1。
(ii)2V2O4(s)+O2(g) 2V2O5(s),活化能为Ea2。
2V2O5(s),活化能为Ea2。
能量变化如图所示。

总反应2SO2(g)+O2(g) 2SO3(g)的
2SO3(g)的
___________ kJ∙mol−1 (用E1~E5中的合理数据组成的代数式表示)。决定SO2催化氧化的总反应速率的是步骤___________ (填(i)或(ii)),其活化能为___________ kJ∙mol−1 (用E1~E5中的合理数据组成的代数式表示)。
(3)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++ ,
,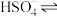 H++
H++ 。
。
①25℃时,Na2SO4溶液的pH___________ (填“>”“<”或“=”)7。
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数___________ (写出计算过程,结果保留三位有效数字)。
(4)液态水中,水存在自偶电离:H2O+H2O H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为___________ 。
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是___________ 。若保持温度不变,关于该所得溶液,下列说法正确的是___________ 。
A.加入少量冰醋酸,c( )与c(
)与c( )均减小
)均减小
B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c( )与c(
)与c( )的比值减小
)的比值减小
D.加入少量Na2SO4固体,c(Ac-)减小
(1)SO2、H2S都是常见的污染性气体,具有一定的毒性。请再写出两种与酸雨、光化学烟雾和臭氧层空洞均有关的污染性气体:
(2)变废为宝是治理污染的常用手段。以V2O5为催化剂,将SO2氧化为SO3,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
(i)SO2(g)+V2O5(s)
 SO3(g)+V2O4(s),活化能为Ea1。
SO3(g)+V2O4(s),活化能为Ea1。(ii)2V2O4(s)+O2(g)
 2V2O5(s),活化能为Ea2。
2V2O5(s),活化能为Ea2。能量变化如图所示。

总反应2SO2(g)+O2(g)
 2SO3(g)的
2SO3(g)的
(3)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++
 ,
,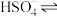 H++
H++ 。
。①25℃时,Na2SO4溶液的pH
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数
(4)液态水中,水存在自偶电离:H2O+H2O
 H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是
A.加入少量冰醋酸,c(
 )与c(
)与c( )均减小
)均减小B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c(
 )与c(
)与c( )的比值减小
)的比值减小D.加入少量Na2SO4固体,c(Ac-)减小
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】油气开采、石油化工、煤化工等行业废气普遍含有的硫化物,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①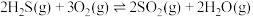
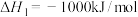
②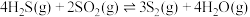
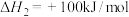
③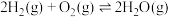
 ;
;
计算 热分解反应④
热分解反应④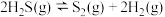 的
的
___________  ;
;
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反应④高温热分解
处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是
。相比克劳斯工艺,高温热分解方法的优点是___________ ,缺点是___________ ;
(3)在1470K、100kPa反应条件下,将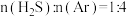 的混合气进行
的混合气进行 热分解反应④。平衡时混合气中
热分解反应④。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为___________ ,平衡常数
___________ kPa;
(4)按投料比 把
把 和
和 加到一密闭容器中发生反应
加到一密闭容器中发生反应
 ,测得平衡时
,测得平衡时 的转化率与温度T、压强p的关系如图甲所示:
的转化率与温度T、压强p的关系如图甲所示:
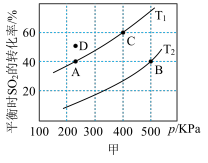
A、B两点对应的平衡常数大小关系为
___________ (填“>”“<”或“=”,下同) ;温度为
;温度为 时,D点
时,D点 与
与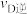 的大小关系为
的大小关系为
___________ 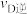 ;
;
(5)工业上脱硫感觉 可以采用电化学法,其中一种方法是内电池模式(直接法),采用内电池模式将废气中的 吸收在电池液中,并在电极反应中氧化硫酸,此反应过程可得到质量分数为40%的硫酸。写出通入
吸收在电池液中,并在电极反应中氧化硫酸,此反应过程可得到质量分数为40%的硫酸。写出通入 电极的反应式:
电极的反应式:___________ 。
(1)已知下列反应的热化学方程式:
①
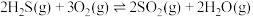
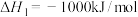
②
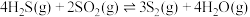
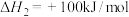
③
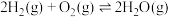
 ;
;计算
 热分解反应④
热分解反应④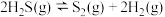 的
的
 ;
;(2)较普遍采用的
 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反应④高温热分解
处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是
。相比克劳斯工艺,高温热分解方法的优点是(3)在1470K、100kPa反应条件下,将
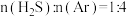 的混合气进行
的混合气进行 热分解反应④。平衡时混合气中
热分解反应④。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为
(4)按投料比
 把
把 和
和 加到一密闭容器中发生反应
加到一密闭容器中发生反应
 ,测得平衡时
,测得平衡时 的转化率与温度T、压强p的关系如图甲所示:
的转化率与温度T、压强p的关系如图甲所示:
A、B两点对应的平衡常数大小关系为

 ;温度为
;温度为 时,D点
时,D点 与
与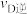 的大小关系为
的大小关系为
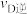 ;
;(5)工业上脱硫感觉 可以采用电化学法,其中一种方法是内电池模式(直接法),采用内电池模式将废气中的
 吸收在电池液中,并在电极反应中氧化硫酸,此反应过程可得到质量分数为40%的硫酸。写出通入
吸收在电池液中,并在电极反应中氧化硫酸,此反应过程可得到质量分数为40%的硫酸。写出通入 电极的反应式:
电极的反应式:
您最近一年使用:0次



