如图为制取氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成结晶水合物FeCl3+6H2O=FeCl3•6H2O。
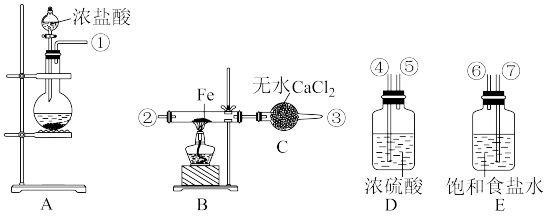
(1)气体方向从左到右,选用上述装置仪器的接口连接顺序为:____ 。
(2)实验开始前应进行的操作是____ 。
(3)欲在A装置中用某氧化剂与浓盐酸反应制取氯气,下列氧化剂可选择____ 。(填序号)
①KMnO4②Ca(ClO)2③MnO2④浓H2SO4⑤KClO3
(4)B中反应的化学方程式是____ 。
(5)容器D的作用是____ ,容器E的作用是____ 。
(6)这套实验装置还存在一个明显的缺陷是____ ,如何改进?_____ 。

(1)气体方向从左到右,选用上述装置仪器的接口连接顺序为:
(2)实验开始前应进行的操作是
(3)欲在A装置中用某氧化剂与浓盐酸反应制取氯气,下列氧化剂可选择
①KMnO4②Ca(ClO)2③MnO2④浓H2SO4⑤KClO3
(4)B中反应的化学方程式是
(5)容器D的作用是
(6)这套实验装置还存在一个明显的缺陷是
更新时间:2022-09-15 22:46:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】化学小组同学设计如下实验验证氯气的部分性质,并探究氯水的成分和性质。
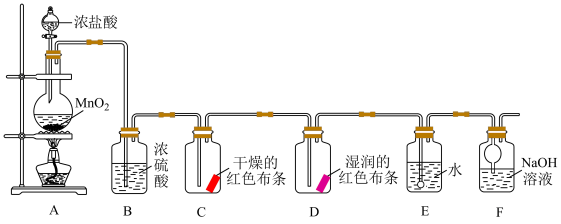
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)验证干燥的氯气没有漂白性的现象为___________ 。
(3)装置F的作用是___________ 。
(4)研究新制氯水成分和性质。
以装置E的溶液进行下列实验
资料:淀粉的特征反应一一遇 变蓝色;
变蓝色; 。
。
①根据实验1可知,氧化性:
___________ (填“>”或“<”) 。
。
②实验2中证明溶液中含有___________ (填微粒的化学式)。
③若用实验3证明氯水中含有氯离子,则实验操作为___________ 。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)验证干燥的氯气没有漂白性的现象为
(3)装置F的作用是
(4)研究新制氯水成分和性质。
以装置E的溶液进行下列实验
| 实验序号 | 实验1 | 实验2 | 实验3 |
| 实验现象 |  |  | |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 有白色沉淀生成 |
 变蓝色;
变蓝色; 。
。①根据实验1可知,氧化性:

 。
。②实验2中证明溶液中含有
③若用实验3证明氯水中含有氯离子,则实验操作为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计以下装置进行实验。
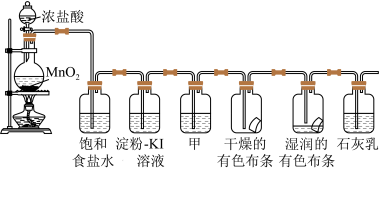
(1)圆底烧瓶内发生的化学方程式为___________ 。在该反应中,被氧化的元素是___________ ,氧化剂与还原剂的物质的量之比为___________ ,比较氧化剂和氧化产物的氧化性大小:___________ ,若产生0.1molCl2,则转移的电子数目为___________ ,该反应中浓盐酸体现了___________ 性质(选填字母编号)。
A.酸性 B.碱性 C.氧化性 D.还原性
(2)饱和食盐水的作用为___________ ,Cl2与石灰乳反应制取漂白粉的化学方程式为___________ 。
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放___________ (填名称)。
(4)某同学在实验室配制80mL质量分数为36.5%(密度为1.2g/cm3)的浓盐酸溶液用于上述实验。
①该同学应选择___________ mL的容量瓶,配制所得浓盐酸的浓度为___________ mol/L。
②若实验中出现以下情况,对所配溶液的物质的量浓度有何影响? (填“偏高”“偏低”或“无影响”)。容量瓶中原有少量蒸馏水___________ ;定容时俯视容量瓶瓶颈上的刻度线___________ ;向容量瓶中转移溶液时不慎将少量溶液溅出酒在容量瓶外面___________ 。
(5)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时反应的离子方程式为___________ 。

(1)圆底烧瓶内发生的化学方程式为
A.酸性 B.碱性 C.氧化性 D.还原性
(2)饱和食盐水的作用为
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放
(4)某同学在实验室配制80mL质量分数为36.5%(密度为1.2g/cm3)的浓盐酸溶液用于上述实验。
①该同学应选择
②若实验中出现以下情况,对所配溶液的物质的量浓度有何影响? (填“偏高”“偏低”或“无影响”)。容量瓶中原有少量蒸馏水
(5)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时反应的离子方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
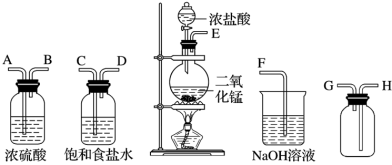
(1)连接上述仪器的正确顺序(填各接口处的字母):_______ 。盛放浓盐酸的仪器名称为:_______ 。
(2)装置中,饱和食盐水的作用是_______ 。
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到_______ ,反应的化学方程式为_______ 。
(4)写出下列反应的化学方程式:
①气体发生装置中进行的反应:_______ 。
②NaOH溶液中发生的反应:_______ 。
(5)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为_______ (填“甲”或“乙”)同学正确,原因是_______ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(4)写出下列反应的化学方程式:
①气体发生装置中进行的反应:
②NaOH溶液中发生的反应:
(5)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】无水 是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用
是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用 还原无水氯化铁制备。
还原无水氯化铁制备。
(1)实验室利用如下装置制取干燥纯净的 。
。
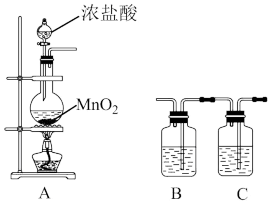
①装置A中盛放浓盐酸的仪器名称是___________ ;装置A中发生反应的离子方程式为___________ 。
②装置B中盛放的试剂为___________ (填试剂名称)。
(2)制取无水氯化铁(已知无水氯化铁易潮解,100℃以上升华)。
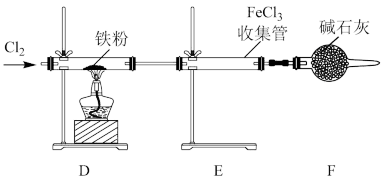
①实验过程中需用热源间歇性微热装置D和E处的连接管,其目的是___________ 。
②装置F的作用___________ 。
(3)取反应后(2)中装置E和F,用氢气还原氯化铁,制备无水氯化亚铁。

①通氢气前需先通入一段时间氮气,其目的是___________ 。
②E中装置未检验到铁单质,检测装置E管中反应产物,测得 ,则产物中
,则产物中 的物质的量分数为
的物质的量分数为___________ %。
 是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用
是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用 还原无水氯化铁制备。
还原无水氯化铁制备。(1)实验室利用如下装置制取干燥纯净的
 。
。
①装置A中盛放浓盐酸的仪器名称是
②装置B中盛放的试剂为
(2)制取无水氯化铁(已知无水氯化铁易潮解,100℃以上升华)。

①实验过程中需用热源间歇性微热装置D和E处的连接管,其目的是
②装置F的作用
(3)取反应后(2)中装置E和F,用氢气还原氯化铁,制备无水氯化亚铁。

①通氢气前需先通入一段时间氮气,其目的是
②E中装置未检验到铁单质,检测装置E管中反应产物,测得
 ,则产物中
,则产物中 的物质的量分数为
的物质的量分数为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某金属A及其化合物之间有如下的转化关系:

(1)写出A、B的化学式:A_______ ,B_________ 。
(2)写出B→D的化学方程式_______________________________ 。
(3)写出B→C的离子方程式________________________________ 。
(4)写出E→C的化学方程式________________________________ 。

(1)写出A、B的化学式:A
(2)写出B→D的化学方程式
(3)写出B→C的离子方程式
(4)写出E→C的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。
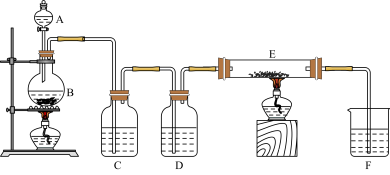
请回答下列问题:
(1)B中发生反应的化学方程式为_______ ;反应中氧化剂为_______ (填化学式)。
(2)为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是_______ ;D装置中的试剂是_______ 。
(3)E中发生的化学反应方程式为_______ 。
(4)F是尾气处理装置,反应离子方程式为_______ 。
(5)实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式_______ 。(已知MnO 被还原为Mn2+)
被还原为Mn2+)

请回答下列问题:
(1)B中发生反应的化学方程式为
(2)为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是
(3)E中发生的化学反应方程式为
(4)F是尾气处理装置,反应离子方程式为
(5)实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式
 被还原为Mn2+)
被还原为Mn2+)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
Ⅰ.查阅资料:含氰化物的废水破坏性处理方法。利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-氧化成CNO- (CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
Ⅱ.实验验证:破坏性处理CN-的效果。化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
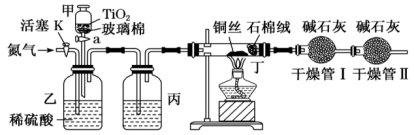
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-的废水与过量NaClO溶液的混合液倒入甲中,塞上橡胶塞。
步骤3:点燃酒精灯对丁装置加热。
步骤4:打开甲上的橡胶塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成测定干燥管Ⅰ(含碱石灰)的质量变化
回答下列问题:
(1)CNO-中C元素的化合价是___________ 。
(2)甲装置的名称为___________ 。
(3)丙装置中的试剂是___________ 。
(4)对丁装置加热放在步骤3进行的原因是___________ 。
(5)干燥管Ⅱ的作用是___________ 。
Ⅰ.查阅资料:含氰化物的废水破坏性处理方法。利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-氧化成CNO- (CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
Ⅱ.实验验证:破坏性处理CN-的效果。化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:

步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-的废水与过量NaClO溶液的混合液倒入甲中,塞上橡胶塞。
步骤3:点燃酒精灯对丁装置加热。
步骤4:打开甲上的橡胶塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成测定干燥管Ⅰ(含碱石灰)的质量变化
回答下列问题:
(1)CNO-中C元素的化合价是
(2)甲装置的名称为
(3)丙装置中的试剂是
(4)对丁装置加热放在步骤3进行的原因是
(5)干燥管Ⅱ的作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和药品制取较纯的无水氯化铁固体。
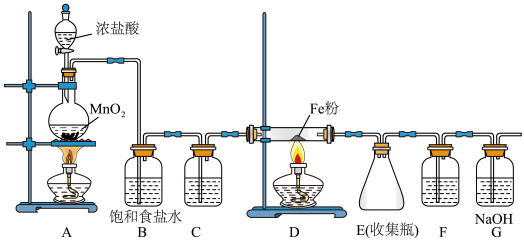
(1)制取氯化铁时,应先点燃_____ (填“A”或“D”)处的酒精灯,制取氯化铁的化学方程式为_____ 。
(2)C、F装置中所装试剂相同,试剂均为________ 。
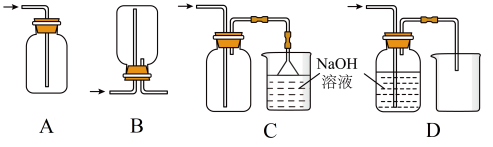
(3)下列收集Cl2的正确装置是______ 。
(4)G装置中反应的离子方程式为________________________________ 。
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为______ (选填序号,下同);写出溶液变血红色的离子方程式:_____________ ,若溶液未变血红色,推断固体物质的成分为______ 。
A. 只有 FeCl3 B.只有Fe C.一定有 FeCl3 D.一定有Fe

(1)制取氯化铁时,应先点燃
(2)C、F装置中所装试剂相同,试剂均为
(3)下列收集Cl2的正确装置是

(4)G装置中反应的离子方程式为
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为
A. 只有 FeCl3 B.只有Fe C.一定有 FeCl3 D.一定有Fe
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】为探索工业废料的再利用,某化学兴趣小组设计了如图-5实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
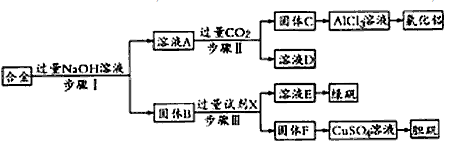
请回答:
(1)步骤I、II、III中均需进行的实验操作是________________ 。
(2)溶液A中的离子主要有_________ ;试剂X是________ 。
(3)进行步骤II时,该小组用图-6所示装置及试剂将制得的CO2气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是________ (用离子方程式表示);为了避免固体C减少,根据图-6所示,改进的措施是__________ 。
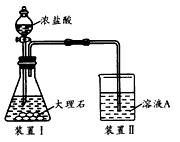
(4)从环境保护角度考虑,用固体F制备CuSO4溶液的化学方程式是___________ 。

请回答:
(1)步骤I、II、III中均需进行的实验操作是
(2)溶液A中的离子主要有
(3)进行步骤II时,该小组用图-6所示装置及试剂将制得的CO2气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是

(4)从环境保护角度考虑,用固体F制备CuSO4溶液的化学方程式是
您最近半年使用:0次



