某反应的反应机理可以分成如下两步,下列说法正确的是
| 反应机理 | 第一步反应 | 第二步反应 |
| 2NO2═NO3+NO(慢反应) | NO3+CO═NO2+CO2(快反应) |
| A.在条件相同下,反应活化能:第一步大于第二步 |
| B.NO3是该反应的催化剂 |
| C.升高温度第一步反应加快,第二步反应速率不变 |
| D.加入合适的催化剂既可加快反应速率,又能增大反应限度 |
更新时间:2022-10-07 11:14:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上在催化剂的作用下CO可以合成甲醇,用计算机模拟单个CO分子合成甲醇的反应历程如图。下列说法正确的是。
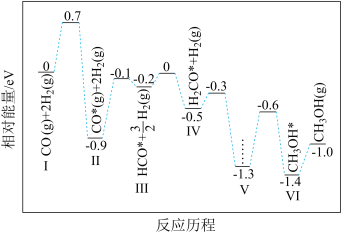

| A.反应过程中有极性键的断裂和生成 |
| B.反应的决速步骤为III→IV |
C.使用催化剂降低了反应的 |
D.反应的热化学方程式为  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用过量铁片与稀盐酸反应,为加快其反应速率而生成氢气量不变,下列措施中可行的是
①以铁屑代替铁片②用过量锌片代替铁片③在稀盐酸中加入少量CuSO4溶液④微热(不考虑HCl的挥发)⑤在稀盐酸中加入等物质的量浓度的硫酸⑥在稀盐酸中加入硫酸钾溶液
①以铁屑代替铁片②用过量锌片代替铁片③在稀盐酸中加入少量CuSO4溶液④微热(不考虑HCl的挥发)⑤在稀盐酸中加入等物质的量浓度的硫酸⑥在稀盐酸中加入硫酸钾溶液
| A.①②④ | B.①②③④ | C.①②③④⑤ | D.全部都可行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
A.反应 ,通入二氧化碳气体,溶液的漂白性增强 ,通入二氧化碳气体,溶液的漂白性增强 |
B. 可以催化双氧水的分解 可以催化双氧水的分解 |
| C.为了增加汽水中二氧化碳的溶解量,采用加压方式 |
D.对于反应 ,达到平衡后,升温使气体颜色变深 ,达到平衡后,升温使气体颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2SO2(g) + O2(g)  2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
| n(O2) / mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 / % | 80 | α1 | α2 | |
| A.甲中反应的平衡常数小于乙 |
| B.平衡时,丙中c(SO3)是甲中的2倍 |
| C.该温度下,平衡常数值为400 |
| D.平衡时,甲中O2的转化率大于乙中O2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】T℃时,向容积为2L的刚性容器中充入1 mol CO2和一定量的H2发生反应:CO2(g)+2H2(g)  HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始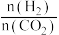 的关系如图所示。已知:初始加入2molH2时,容器内混合气体的总压强为1.2p kPa。下列说法不正确的是
的关系如图所示。已知:初始加入2molH2时,容器内混合气体的总压强为1.2p kPa。下列说法不正确的是
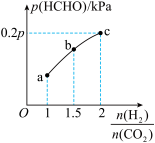
 HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始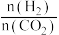 的关系如图所示。已知:初始加入2molH2时,容器内混合气体的总压强为1.2p kPa。下列说法不正确的是
的关系如图所示。已知:初始加入2molH2时,容器内混合气体的总压强为1.2p kPa。下列说法不正确的是
| A.5 min时反应到达c点,ν(H2)=0.1 mol·L-1·min-1 |
B.随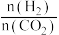 增大, HCHO(g)的平衡压强不断增大 增大, HCHO(g)的平衡压强不断增大 |
C.b点时反应的平衡常数Kp =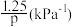 |
D.由图象可得到:Kp(a) Kp(b) Kp(b) Kp(c) Kp(c) |
您最近一年使用:0次



 时释放能量少,所以过渡态5非常稳定
时释放能量少,所以过渡态5非常稳定

