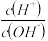常温下向90mL蒸馏水中滴入10mL2mol/LHA溶液,已知溶液中的氢离子浓度 和温度随HA溶液体积变化曲线如图所示,下列说法正确的是
和温度随HA溶液体积变化曲线如图所示,下列说法正确的是

 和温度随HA溶液体积变化曲线如图所示,下列说法正确的是
和温度随HA溶液体积变化曲线如图所示,下列说法正确的是
A.常温下 |
| B.a→b过程中温度升高是由于HA电离放热 |
| C.b点溶液导电性一定高于d点 |
| D.c→d过程中水的电离程度逐渐增大 |
22-23高二上·山东烟台·阶段练习 查看更多[2]
更新时间:2022-10-11 23:00:04
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】一定温度下,水存在H2O H++OH- ΔH>0的平衡,下列叙述一定正确的是
H++OH- ΔH>0的平衡,下列叙述一定正确的是
 H++OH- ΔH>0的平衡,下列叙述一定正确的是
H++OH- ΔH>0的平衡,下列叙述一定正确的是| A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小 |
| B.将水加热,Kw增大,pH减小 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.向水中加入少量固体硫酸钠,c(H+)=10-7mol•L-1,Kw不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】水的电离平衡为:H2O  H+ + OH— ΔH>0 ,下列叙述正确的是
H+ + OH— ΔH>0 ,下列叙述正确的是
 H+ + OH— ΔH>0 ,下列叙述正确的是
H+ + OH— ΔH>0 ,下列叙述正确的是| A.向水中加入稀氨水,c(OH—)降低 |
| B.恒温下,向水中加入少量固体硫酸氢钠,Kw不变 |
| C.恒温下,向水中加入少量固体CH3COONa,平衡逆向移动 |
| D.将水加热,Kw不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列因素能影响水的电离平衡,且能使水的电离平衡向右移动的是
| A.CH3COOH | B. | C.升高温度 | D.NaHSO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下表是常温下某些一元弱酸的平衡常数:
则0.01 mol·L-1的下列物质的溶液中,c(H+)最小的是
| 弱酸 | H2CO3 | CH3COOH | HF | HNO2 |
| 电离常数 | K1=4.4×10-7 | 1.8×10-5 | 6.8×10-4 | 6.4×10-6 |
| A.HNO2 | B.CH3COOH | C.HF | D.H2CO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25℃时,以0.10 mol∙L−1盐酸滴定0.10 mol∙L−1一元碱YOH的滴定曲线如图所示,下列表述错误的是
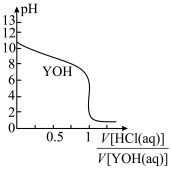

| A.YOH的电离方程式为YOH=Y++OH- | B.此实验可选用甲基橙作指示剂 |
| C.YOH的电离平衡常数Kb≈1×10−5 | D.滴定时盐酸盛放在带活塞的滴定管中 |
您最近一年使用:0次