已知甲、乙中进行的反应是: ;丙、丁中进行的反应是:
;丙、丁中进行的反应是:
 。实验条件和起始投料如下表所示,下列说法正确的是
。实验条件和起始投料如下表所示,下列说法正确的是
 ;丙、丁中进行的反应是:
;丙、丁中进行的反应是:
 。实验条件和起始投料如下表所示,下列说法正确的是
。实验条件和起始投料如下表所示,下列说法正确的是| 甲 | 外界条件 | 实验组别 | 起始投料(mol) | 乙 | 外界条件 | 实验组别 | 起始投料(mol) | ||||
 |  |  |  |  |  | ||||||
| 恒温恒容 | Ⅰ | 1 | 3 | 0 | 恒温恒压 | Ⅰ | 1 | 3 | 0 | ||
| Ⅱ | 0 | 0 | 4 | Ⅱ | 2 | 6 | 0 | ||||
| 丙 | 外界条件 | 实验组别 | 起始投料(mol) | 丁 | 外界条件 | 实验组别 | 起始投料(mol) | ||||
 |  | HI |  |  | HI | ||||||
| 恒温恒容 | Ⅰ | 1 | 1 | 0 | 恒温恒压 | Ⅰ | 1 | 2 | 0 | ||
| Ⅱ | 0 | 0 | 2 | Ⅱ | 2 | 4 | 0 | ||||
A.甲组中,若平衡时 和 和 的转化率分别为 的转化率分别为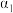 和 和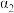 ,则 ,则 |
B.乙组中,平衡Ⅱ中 的浓度是平衡Ⅰ的二倍。 的浓度是平衡Ⅰ的二倍。 |
C.丙组中,若平衡时Ⅰ中放热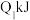 ,Ⅱ中吸热 ,Ⅱ中吸热 ,则 ,则 |
D.丁组中,建立平衡的时间: |
22-23高二上·山东烟台·阶段练习 查看更多[2]
更新时间:2022-10-11 23:00:04
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】将固体NH4I置于某体积不变的密闭容器中,在某温度下发生下列反应:①NH4I(s)⇌NH3(g)+HI(g);②2HI(g)⇌H2(g)+I2(g),平衡时,c(HI)=6mol•L﹣1,c(H2)=1mol•L﹣1,则此温度下反应①的平衡常数为( )
| A.36 | B.49 | C.48 | D.64 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
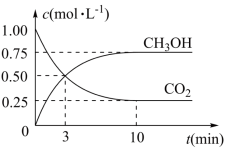

A.升高温度能使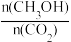 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075mol·L-1·min-1 |
您最近一年使用:0次
【推荐1】分别向容积固定的2L密闭容器中充入A和6molB,发生反应:2A(g)+B(s) 2D(g) △H<0,测得相关数据如表,下列说法正确的是
2D(g) △H<0,测得相关数据如表,下列说法正确的是
 2D(g) △H<0,测得相关数据如表,下列说法正确的是
2D(g) △H<0,测得相关数据如表,下列说法正确的是| 实验I | 实验II | 实验III | |
| c(A)起始/mol•L-1 | 1 | 2 | 1.2 |
| c(A)平衡/mol•L-1 | 0.5 | 1 | 0.95 |
| 放出的热量/kJ | a | b | c |
| A.放出的热量关系为b=2a=4c |
| B.实验I、II、III均在同一温度下进行反应 |
| C.依据实验I中的数据,计算出该温度下实验I的平衡常数为4 |
| D.实验I、II、III初始反应速率最大的一定是II |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在一固定容积的密闭容器中,充入2molA和1molB发生反应:2A(g)+B(g)⇌xC(g),达到平衡时,C的物质的量浓度为0.9mol/L。若维持容器体积和温度不变,按0.6molA,0.3molB和1.4molC为起始物质,达到平衡后,C的物质的量浓度也为0.9mol/L,则x的值为
| A.只能为2 | B.只能为3 | C.只能为4 | D.可能为2或3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:2NO(g)+O2(g) 2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图),下列说法不正确的是
2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图),下列说法不正确的是
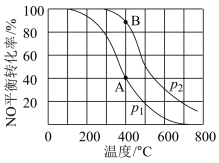
 2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图),下列说法不正确的是
2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图),下列说法不正确的是
| A.p1<p2 |
| B.其它条件不变,通入一定量的NO,可使A点到B点 |
| C.A、B两点的平衡常数:K(A)=K(B) |
| D.该反应的ΔH<0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】关于平衡常数,下列说法不正确的是( )
| A.平衡常数不随反应物或生成物的浓度的改变而改变 |
| B.平衡常数随温度的改变而改变 |
| C.平衡常数不随压强的改变而改变 |
| D.使用催化剂能使平衡常数增大 |
您最近一年使用:0次

 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是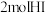 ,②
,② ,③
,③ 与
与 ,发生反应
,发生反应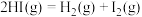
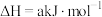 ,均达到平衡时,三个容器中的焓变分别是
,均达到平衡时,三个容器中的焓变分别是 、
、 、
、 ,下列关系正确的是
,下列关系正确的是 的浓度:②>①>③
的浓度:②>①>③


