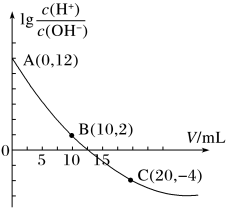
25℃时,用0.10 mol/L的氨水滴定10.00 mL0.05 mol/LH2A溶液,加入氨水的体积(V)与溶液中 的关系如图所示(忽略溶液体积变化)。下列说法
的关系如图所示(忽略溶液体积变化)。下列说法不正确 的是
 的关系如图所示(忽略溶液体积变化)。下列说法
的关系如图所示(忽略溶液体积变化)。下列说法
| A.A点溶液的pH等于1 | B.由图中数据可知,H2A为弱酸 |
| C.B点水电离出的H+浓度为1.0×10-6 mol/L | D.水的电离程度为:B>C>A |
更新时间:2022-11-05 20:24:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.与Fe反应能放出H2的溶液中: 、 、 、 、 、 、 |
C.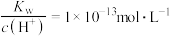 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.水电离的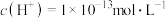 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】为了维持正常的生理活动,人体各种体液的pH都要保持在一定的范围。例如,血液的正常pH范围是7.35~7.45。当血浆的pH降到7.2以下会引起酸中毒,升到7.5以上会引起碱中毒,降到6.8以下或升到7.8以上,会危及生命安全。血浆中 /
/ 缓冲体系对稳定体系的酸碱度发挥着重要作用。
缓冲体系对稳定体系的酸碱度发挥着重要作用。 /
/ 的缓冲作用可用下列平衡表示:
的缓冲作用可用下列平衡表示: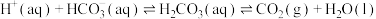 。
。
下列有关溶液的说法正确的是
 /
/ 缓冲体系对稳定体系的酸碱度发挥着重要作用。
缓冲体系对稳定体系的酸碱度发挥着重要作用。 /
/ 的缓冲作用可用下列平衡表示:
的缓冲作用可用下列平衡表示: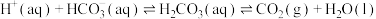 。
。下列有关溶液的说法正确的是
A.由于血浆中存在 / / 缓冲体系,加入酸或碱,pH一定无明显变化 缓冲体系,加入酸或碱,pH一定无明显变化 |
B.人体发生碱中毒时注射 溶液可以缓解症状 溶液可以缓解症状 |
C.已知 在水溶液中可以形成二聚体,可分析出 在水溶液中可以形成二聚体,可分析出 通过氢键形成八元环结构 通过氢键形成八元环结构 |
D.实验测得0.1 mol·L-1 溶液在25~60℃升温过程中(不考虑水挥发)溶液的pH先减小后增大,减小的原因是升温抑制了 溶液在25~60℃升温过程中(不考虑水挥发)溶液的pH先减小后增大,减小的原因是升温抑制了 的水解 的水解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列溶液因盐的水解而呈酸性的是
| A.柠檬水 | B.洁则灵 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关溶液的酸碱性与pH的说法错误的是
| A.溶液pH越小,酸性越强,反之,碱性越强 |
| B.pH<7的溶液可能呈酸性 |
| C.当溶液中的c(H+)或c(OH-)较小时,用pH表示其酸碱度更为方便 |
| D.不存在pH<0或pH>14的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】H2C2O4 是二元弱酸,常温下,Ka1(H2C2O4)=5.4×10-2,Ka2(H2C2O4)=5.4×10-5,下列溶液的离子浓度关系式正确的是
A.pH=2的H2C2O4溶液中,c(H+)=c( )=10-2 mol/L )=10-2 mol/L |
B.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)=c(OH- )+ c( ) ) |
C.将NaOH溶液滴加到H2C2O4溶液中至混合溶液呈中性:c( )>c( )>c( ) ) |
D.NaHC2O4溶液中:c(Na+)>c(H2C2O4 )>c( )>c( )>c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃下,向20mL0.1mol/LH2A溶液中滴加0.1mol/LNaOH 溶液,有关粒子物质的量的变化如图所示。下列有关说法正确的是


| A.H2A 电离方程式 H2A=2H++A2- |
| B.V[NaOH(aq)]="20mL" 时,溶液显碱性 |
| C.已知25℃时 K2(H2A)=1.0×10-9.1,则V[NaOH(aq)]="VmL" 时,pH=9.1 |
| D.V[NaOH(aq)]=20mL时,溶液中存在关系:(HA-)+C(A2-)+C(H2A)="0.1mol/L" |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】以酚酞为指示剂,用0.1000mol/LNaOH溶液滴定20.00mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数δ随滴加NaOH溶液VNaOH的变化关系如图所示。
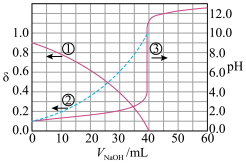
比如A2-的分布系数:[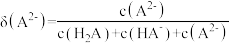 ]下列说法正确的是
]下列说法正确的是

比如A2-的分布系数:[
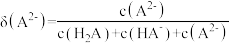 ]下列说法正确的是
]下列说法正确的是| A.H2A的电离方程式为:H2A⇌H++HA-,HA-⇌H++A2- |
| B.HA-的电离常数Ka=1.0×10-2 |
| C.H2A的浓度为0.2000mol/L |
| D.滴定终点时,溶液中2c(Na+)=c(A2-)+c(HA-)+c(H2A) |
您最近一年使用:0次


 、Fe2+、SO
、Fe2+、SO 、Cl-
、Cl- )=0.1mol•L-1的溶液中:Na+、K+、CO
)=0.1mol•L-1的溶液中:Na+、K+、CO 、Br-
、Br-

