某厂利用废旧铅蓄电池中的铅膏(主要成分为 、
、 、PbO和Pb,还有少量铁、铝的氧化物)回收PbO,工艺流程如下:
、PbO和Pb,还有少量铁、铝的氧化物)回收PbO,工艺流程如下:

一些难溶电解质的溶度积常数如下表。
溶液中可溶组分浓度c≤1.0×10-5mol/L时,可认为已除尽。回答下列问题:
(1)“脱硫”时 反应的离子方程式为
反应的离子方程式为_______ ;结合数据分析该反应能否进行完全_______ 。
(2)常温下,溶液中各形态铅的浓度分数α与溶液pH变化的关系如下图所示:
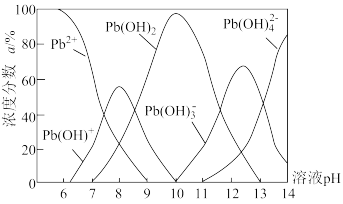
①“酸浸”时除加入醋酸,还要加入 。
。
(ⅰ) 促进了金属Pb在醋酸中转化为
促进了金属Pb在醋酸中转化为 ;
;
(ⅱ) 也能使
也能使 转化为
转化为 ,
, 的作用是
的作用是_______ ;
(ⅲ) 能氧化溶液中的
能氧化溶液中的_______ 离子。
②流程中多步操作均需控制溶液pH。
i.“除杂”时,需调节溶液pH的理论范围为_______ 。
ⅱ.“沉铅”时,若溶液pH由10增大到了11,发生反应的离子方程式为_______ 。
③含铅废水的处理:某科研小组用一种新型试剂(DH)去除废水中的痕量铅,脱铅反应为: 。脱铅时最合适的pH约为
。脱铅时最合适的pH约为_______ (填标号)。
A.6 B.8 C.10 D.12
 、
、 、PbO和Pb,还有少量铁、铝的氧化物)回收PbO,工艺流程如下:
、PbO和Pb,还有少量铁、铝的氧化物)回收PbO,工艺流程如下:
一些难溶电解质的溶度积常数如下表。
| 难溶电解质 |  |  |  |  |  |
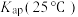 | 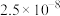 | 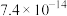 |  | 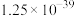 | 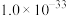 |
(1)“脱硫”时
 反应的离子方程式为
反应的离子方程式为(2)常温下,溶液中各形态铅的浓度分数α与溶液pH变化的关系如下图所示:

①“酸浸”时除加入醋酸,还要加入
 。
。(ⅰ)
 促进了金属Pb在醋酸中转化为
促进了金属Pb在醋酸中转化为 ;
;(ⅱ)
 也能使
也能使 转化为
转化为 ,
, 的作用是
的作用是(ⅲ)
 能氧化溶液中的
能氧化溶液中的②流程中多步操作均需控制溶液pH。
i.“除杂”时,需调节溶液pH的理论范围为
ⅱ.“沉铅”时,若溶液pH由10增大到了11,发生反应的离子方程式为
③含铅废水的处理:某科研小组用一种新型试剂(DH)去除废水中的痕量铅,脱铅反应为:
 。脱铅时最合适的pH约为
。脱铅时最合适的pH约为A.6 B.8 C.10 D.12
更新时间:2022-11-10 17:41:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氢氧化氧镍( )难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含
)难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含 ,以及少量
,以及少量 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图: 的性质较稳定。
的性质较稳定。
回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
(2)“浸取渣”的主要成分为______ (填化学式)。
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:______ 。
(4)“转化”时 的作用是
的作用是______ ,实际生产中发现 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是______ 。
(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的 如下表所示:
如下表所示:
则“沉铁”过程中加入 溶液调节
溶液调节 的范围应为
的范围应为______ 。
(6)“氧化”时发生反应的离子方程式为______ 。若用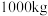 废料(其中
废料(其中 的质量分数为
的质量分数为 )经该流程制得
)经该流程制得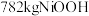 固体,则
固体,则 的产率为
的产率为______ 。( )
)
 )难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含
)难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含 ,以及少量
,以及少量 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图: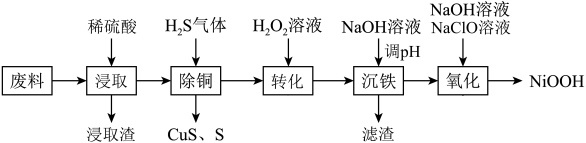
 的性质较稳定。
的性质较稳定。回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.使用 浓硫酸浸取 浓硫酸浸取 |
(2)“浸取渣”的主要成分为
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:
(4)“转化”时
 的作用是
的作用是 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的
 如下表所示:
如下表所示:金属阳离子 |
|
|
|
开始沉淀时的pH | 1.5 | 6.5 | 7.2 |
沉淀完全时的pH | 3.2 | 9.7 | 9.2 |
 溶液调节
溶液调节 的范围应为
的范围应为(6)“氧化”时发生反应的离子方程式为
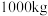 废料(其中
废料(其中 的质量分数为
的质量分数为 )经该流程制得
)经该流程制得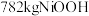 固体,则
固体,则 的产率为
的产率为 )
)
您最近一年使用:0次
【推荐2】铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态,铈的合金耐高温,可以用来制造喷气推进器零件。
请回答下列问题:
(1)雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物质的量之比为1:1),该反应氧化剂与还原剂的物质的量之比为________ 。
(2)可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。
①Ce4+从电解槽的______ (填字母序号)口流出。
②写出阴极的电极反应式________________ 。
(3)铈元素在自然界中主要以氟碳矿形式存在。主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:

①焙烧过程中发生的主要反应方程式为__________________ 。
②有同学认为酸浸过程中用稀硫酸和H2O2替换盐酸更好,他的理由是_________ 。
③Ce(BF4)3、KBF4的Ksp分别为a、b,则Ce(BF4)3(s)+3KCl(aq) 3KBF4(s)+CeCl3(aq)平衡常数为
3KBF4(s)+CeCl3(aq)平衡常数为________ (用a、b的代数式表示)。
④加热CeCl3·6H2O和NH4Cl的固体混合物可得固体无水CeCl3,其中NH4Cl的作用是______ 。
请回答下列问题:
(1)雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物质的量之比为1:1),该反应氧化剂与还原剂的物质的量之比为
(2)可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。
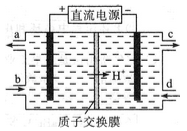
①Ce4+从电解槽的
②写出阴极的电极反应式
(3)铈元素在自然界中主要以氟碳矿形式存在。主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:

①焙烧过程中发生的主要反应方程式为
②有同学认为酸浸过程中用稀硫酸和H2O2替换盐酸更好,他的理由是
③Ce(BF4)3、KBF4的Ksp分别为a、b,则Ce(BF4)3(s)+3KCl(aq)
 3KBF4(s)+CeCl3(aq)平衡常数为
3KBF4(s)+CeCl3(aq)平衡常数为④加热CeCl3·6H2O和NH4Cl的固体混合物可得固体无水CeCl3,其中NH4Cl的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分 )为原料制备氯化亚铜的路线如下:
)为原料制备氯化亚铜的路线如下:
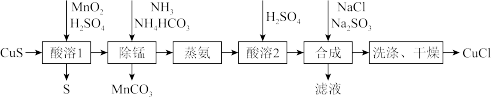
(1)“酸溶1”步骤中发生反应的化学方程式为_______ 。
(2)“除锰”步骤中 转化为
转化为 沉淀,
沉淀, 转变为
转变为 留在溶液中。则“除锰”步骤中发生反应的离子方程式为
留在溶液中。则“除锰”步骤中发生反应的离子方程式为_______ 。
(3)“合成”步骤加入 的速率不宜过快,否则会产生
的速率不宜过快,否则会产生_______ 气体(写化学式),除可能与酸溶时硫酸过量有关,还可能的原因是_______ 。(用离子方程式表示)
(4)“洗涤”步骤先用盐酸洗,再用无水乙醇洗涤。用无水乙醇洗涤除可洗去杂质,减少 的溶解外,还可以
的溶解外,还可以_______ 。
 )为原料制备氯化亚铜的路线如下:
)为原料制备氯化亚铜的路线如下: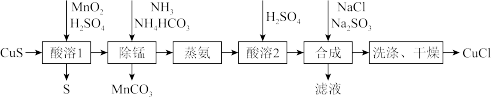
(1)“酸溶1”步骤中发生反应的化学方程式为
(2)“除锰”步骤中
 转化为
转化为 沉淀,
沉淀, 转变为
转变为 留在溶液中。则“除锰”步骤中发生反应的离子方程式为
留在溶液中。则“除锰”步骤中发生反应的离子方程式为(3)“合成”步骤加入
 的速率不宜过快,否则会产生
的速率不宜过快,否则会产生(4)“洗涤”步骤先用盐酸洗,再用无水乙醇洗涤。用无水乙醇洗涤除可洗去杂质,减少
 的溶解外,还可以
的溶解外,还可以
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】镍氢电池是一种性能良好的蓄电池,电池容量大,充电过程快,具有很好的应用前景。
Ⅰ.已知某镍氢二次电池放电时的总反应式为NiOOH + MH Ni(OH)2 + M,电解质溶液为KOH溶液,其中MH被称为储氢电极。充电时储氢电极为
Ni(OH)2 + M,电解质溶液为KOH溶液,其中MH被称为储氢电极。充电时储氢电极为_____ 极,请写出充电时阳极反应式:____________ 。
Ⅱ.废旧电池对环境有一定的危害,某种型号镍电池的电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。研究小组设计如下工艺流程,对该电池的电极材料进行资源回收:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②某温度下:Ksp[Ni(OH)2] = 5.0×10-16、Ksp[NiC2O4] = 4.0×10-10
Ksp[Fe(OH)3] = 4.0×10-38、Ksp[Al(OH)3] = 3.0×10-34
回答下列问题:
(1)第②步调节溶液的pH,最佳的试剂为________
a.NaOH b.NiO c.CO2 d.HCl
(2)写出步骤④中反应的化学方程式_____________ ,请从沉淀转化的角度,解释该反应能发生的原因_______________ 。
(3)第⑤步电解滤液的阴极产物为___________ ,另一电极产物全部用于氧化沉淀Ⅲ,该反应的离子方程式为:_____________ ,理论上当电解池转移10mol电子时,能得到产物Ni(OH)3 ________ kg。
Ⅰ.已知某镍氢二次电池放电时的总反应式为NiOOH + MH
 Ni(OH)2 + M,电解质溶液为KOH溶液,其中MH被称为储氢电极。充电时储氢电极为
Ni(OH)2 + M,电解质溶液为KOH溶液,其中MH被称为储氢电极。充电时储氢电极为Ⅱ.废旧电池对环境有一定的危害,某种型号镍电池的电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。研究小组设计如下工艺流程,对该电池的电极材料进行资源回收:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②某温度下:Ksp[Ni(OH)2] = 5.0×10-16、Ksp[NiC2O4] = 4.0×10-10
Ksp[Fe(OH)3] = 4.0×10-38、Ksp[Al(OH)3] = 3.0×10-34
回答下列问题:
(1)第②步调节溶液的pH,最佳的试剂为
a.NaOH b.NiO c.CO2 d.HCl
(2)写出步骤④中反应的化学方程式
(3)第⑤步电解滤液的阴极产物为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
解题方法
【推荐2】氯碱工业中电解饱和食盐水的原理示意图如右图所示

(1)溶液A的溶质是___________________ ;
(2)电解饱和食盐水的离子方程式是____________________________
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用______________
(4)电解所用的盐水需精制。去除有影响的 、
、 ,
, ,
, ,[
,[ >
> ]。
]。
精致流程如下(淡盐水和溶液A来电解池):
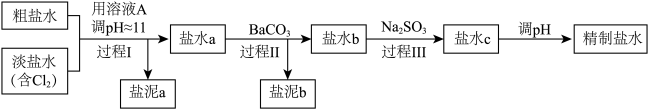
①盐泥a除泥沙外,还含有的物质是____ 。
②过程Ⅰ中将 转化为N2的离子方程式是
转化为N2的离子方程式是___
③ 的溶解度比
的溶解度比 的小,过程Ⅱ中除去的离子有
的小,过程Ⅱ中除去的离子有______
④经过程Ⅲ处理,要求盐水中c 中剩余 的含量小于5mg /L,若盐水b中
的含量小于5mg /L,若盐水b中 的含量是7.45 mg /L,则处理10m3盐水b,至多添加10%
的含量是7.45 mg /L,则处理10m3盐水b,至多添加10% 溶液
溶液_______ kg(溶液体积变化忽略不计)。

(1)溶液A的溶质是
(2)电解饱和食盐水的离子方程式是
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用
(4)电解所用的盐水需精制。去除有影响的
 、
、 ,
, ,
, ,[
,[ >
> ]。
]。精致流程如下(淡盐水和溶液A来电解池):

①盐泥a除泥沙外,还含有的物质是
②过程Ⅰ中将
 转化为N2的离子方程式是
转化为N2的离子方程式是③
 的溶解度比
的溶解度比 的小,过程Ⅱ中除去的离子有
的小,过程Ⅱ中除去的离子有④经过程Ⅲ处理,要求盐水中c 中剩余
 的含量小于5mg /L,若盐水b中
的含量小于5mg /L,若盐水b中 的含量是7.45 mg /L,则处理10m3盐水b,至多添加10%
的含量是7.45 mg /L,则处理10m3盐水b,至多添加10% 溶液
溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】煤粉灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如图:
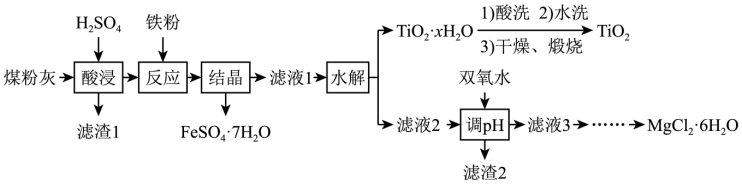
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离出SO 和一种阳离子。
和一种阳离子。
②常温下,Ksp[Al(OH)3]=1.0×10-32,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mg(OH)2]=1×10-11。
请回答下列问题:
(1)向Mg(OH)2的悬浊液中,加入几滴FeCl3溶液,出现红褐色沉淀,请用离子方程式表示这一过程_____ 。
(2)“酸浸”时TiO2发生反应的离子方程式为____ ;“反应”时加入铁粉的作用是____ 。
(3)“结晶”需控制在70℃左右,温度过高会导致的后果是____ 。
(4)“水解”反应的离子方程式是____ 。所得TiO2·xH2O沉淀进行酸洗的目的为____ 。
(5)为使滤渣2沉淀完全(溶液中离子浓度小于10-5mol·L-1)需“调pH”最小为____ 。
(6)实验室用MgCl2溶液制备MgCl2·6H2O,需进行的操作是____ 、降温结晶、过滤、洗涤、干燥。

已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离出SO
 和一种阳离子。
和一种阳离子。②常温下,Ksp[Al(OH)3]=1.0×10-32,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mg(OH)2]=1×10-11。
请回答下列问题:
(1)向Mg(OH)2的悬浊液中,加入几滴FeCl3溶液,出现红褐色沉淀,请用离子方程式表示这一过程
(2)“酸浸”时TiO2发生反应的离子方程式为
(3)“结晶”需控制在70℃左右,温度过高会导致的后果是
(4)“水解”反应的离子方程式是
(5)为使滤渣2沉淀完全(溶液中离子浓度小于10-5mol·L-1)需“调pH”最小为
(6)实验室用MgCl2溶液制备MgCl2·6H2O,需进行的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某科研课题小组研究利用含H+、Na+、Zn2+、Mn2+、Fe2+、Fe3+、SO 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:

回答下列问题:
(1)加入双氧水的目的是___________ 。
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程___________ 。
第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
(3)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq)=ZnS(s)+Mn2+(aq),其平衡常数K=___________ 。(填数值)
 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
回答下列问题:
(1)加入双氧水的目的是
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程
第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
| 浓度/(mol·L-1) | 氢氧化物的Ksp | 开始沉淀的pH | 沉淀完全的pH | |
| Zn2+ | 0.12 | 1.2×10-17 | 6.0 | 8.1 |
| Mn2+ | 0.10 | 4.0×10-14 | 7.8 | 9.8 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】碲(Te)是一种第VIA族分散稀有元素,主要伴生于铜、镍、铅等金属矿藏中。TeO2属于两性氧化物,难溶于水,易溶于强酸和强碱。工业上可从电解精炼铜的阳极泥(主要成分Cu2Te,还有少量的Ag、Au)中提取碲。其工艺流程如下:
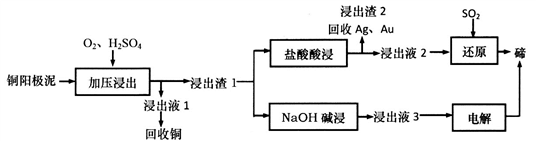
(1)“加压浸出”生成TeO2的离子方程式为________________________ ,“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是_________________________________ 。
(2)“盐酸酸浸”后将SO2通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之比为________________ ,该流程中可循环利用的物质是_____________ (填化学式)。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgC1)=1.80×10-10。盐酸酸浸时,“浸出渣1”中Ag2SO4可充分转化为AgC1。通过计算说明为什么可以实现充分转化_________________ 。
(4)NaOH碱浸时反应的离子方程式为__________________ 。流程中,电解过程用石墨为电极得到碲,阴极的电极反应式为__________________________________ 。
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。随时间变化,不同固液比对镍浸出率的影响曲线如图所示。
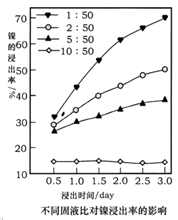

①由图可知,固液比与镍浸出率的关系是______________________ 。
②除固液比之外,你认为影响金属浸出率的因素还有____________________ (至少两项)。

(1)“加压浸出”生成TeO2的离子方程式为
(2)“盐酸酸浸”后将SO2通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之比为
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgC1)=1.80×10-10。盐酸酸浸时,“浸出渣1”中Ag2SO4可充分转化为AgC1。通过计算说明为什么可以实现充分转化
(4)NaOH碱浸时反应的离子方程式为
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。随时间变化,不同固液比对镍浸出率的影响曲线如图所示。


①由图可知,固液比与镍浸出率的关系是
②除固液比之外,你认为影响金属浸出率的因素还有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】草酸钻用途广泛,可用于指示剂和催化剂制备。
(1)向硫酸钴溶液中加入草酸铵溶液后,当溶液中 浓度为
浓度为 时,
时, 浓度为
浓度为_______ 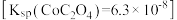 。
。
(2)在空气中加热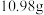 草酸钻晶体
草酸钻晶体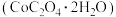 ,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
经测定,加热到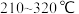 过程中的生成物只有
过程中的生成物只有 和钴的氧化物,此过程发生反应的化学方程式为
和钴的氧化物,此过程发生反应的化学方程式为_______ 。
(3)钴有多种氧化物,其中 可用作电极,若选用
可用作电极,若选用 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为 ,其电极反应式为
,其电极反应式为_______ 。
(4)为测定某草酸钻样品中草酸钴晶体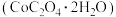 的质量分数进行如下实验:
的质量分数进行如下实验:
①取草酸钴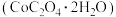 样品
样品 ,加入
,加入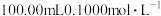 酸性
酸性 溶液,加热(该条件下
溶液,加热(该条件下 不被氧化)。
不被氧化)。
②充分反应后将溶液冷却至室温,加入 容量瓶中,定容。
容量瓶中,定容。
③取 溶液,用
溶液,用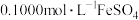 溶液滴定。
溶液滴定。
④重复步骤③的实验2次。三次测定数据如下表:
计算样品中草酸钴晶体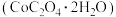 的质量分数:
的质量分数:_______ (写出计算过程)。
(1)向硫酸钴溶液中加入草酸铵溶液后,当溶液中
 浓度为
浓度为 时,
时, 浓度为
浓度为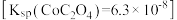 。
。(2)在空气中加热
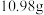 草酸钻晶体
草酸钻晶体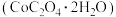 ,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。| 温度范围/℃ | 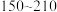 | 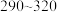 | 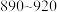 |
| 固体质量/g | 8.82 | 4.82 | 4.50 |
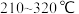 过程中的生成物只有
过程中的生成物只有 和钴的氧化物,此过程发生反应的化学方程式为
和钴的氧化物,此过程发生反应的化学方程式为(3)钴有多种氧化物,其中
 可用作电极,若选用
可用作电极,若选用 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为 ,其电极反应式为
,其电极反应式为(4)为测定某草酸钻样品中草酸钴晶体
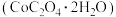 的质量分数进行如下实验:
的质量分数进行如下实验:①取草酸钴
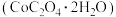 样品
样品 ,加入
,加入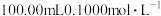 酸性
酸性 溶液,加热(该条件下
溶液,加热(该条件下 不被氧化)。
不被氧化)。②充分反应后将溶液冷却至室温,加入
 容量瓶中,定容。
容量瓶中,定容。③取
 溶液,用
溶液,用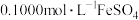 溶液滴定。
溶液滴定。④重复步骤③的实验2次。三次测定数据如下表:
| 实验序号 | 1 | 2 | 3 |
消耗 标准溶液体积/ 标准溶液体积/ | 18.32 | 18.02 | 17.98 |
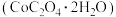 的质量分数:
的质量分数:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】电脑和手机等电子产品产业蓬勃发展,推动了高纯硅的生产与应用。工业上用“西门子法”以硅石SiO2为原料制备冶金级高纯硅的工艺流程如下:
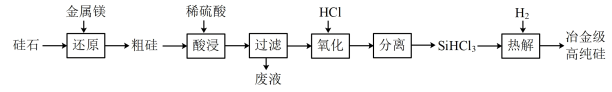
请回答下列问题:
(1)硅元素在周期的位置为_______ 。
(2)“还原”过程需在高温下进行,该反应的生成物除硅和MgO外,还可能有_______ 。
(3)加快“酸浸”速率的方法有_______ (写两种)。
(4)“氧化”过程发生的主要反应为Si+3HCl=SiHCl3 +H2,该反应中还原产物为_______ 。(已知:SiHCl3中Si为+4价)。
(5)在还原炉中H2与SiHCl3加热到1100~1200℃发生“热解”反应即制取冶金级高纯硅,还原炉中发生反应的化学方程式为_______ 。上述工艺生产中循环利用的物质有_______ 。

请回答下列问题:
(1)硅元素在周期的位置为
(2)“还原”过程需在高温下进行,该反应的生成物除硅和MgO外,还可能有
(3)加快“酸浸”速率的方法有
(4)“氧化”过程发生的主要反应为Si+3HCl=SiHCl3 +H2,该反应中还原产物为
(5)在还原炉中H2与SiHCl3加热到1100~1200℃发生“热解”反应即制取冶金级高纯硅,还原炉中发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用铝土矿(主要成分是 ,还含有
,还含有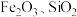 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的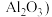 ,某研究性学习小组设计了如图提取流程:
,某研究性学习小组设计了如图提取流程:
(1)固体①、③的化学式分别为___________ 、___________ 。
(2)操作①的名称是___________ ,操作③用到的仪器有酒精灯、泥三角、___________ 。
(3)流程中的 最好选用
最好选用___________ ,发生反应的主要离子方程式为___________ 。
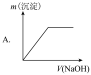
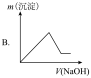
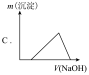
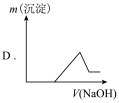
(4)若向滤液(1)中逐滴滴入 溶液至过量,产生沉淀随
溶液至过量,产生沉淀随 滴入关系正确的是___________。
滴入关系正确的是___________。
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为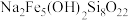 ,该物质中+2价铁与+3价铁的物质的量之比为。将
,该物质中+2价铁与+3价铁的物质的量之比为。将 该矿石用足量硫酸溶解后,加入过量铜粉使溶液中的铁元素全部变为
该矿石用足量硫酸溶解后,加入过量铜粉使溶液中的铁元素全部变为 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去VmL溶液。该的石中铁元素的质量分数为
反应,用去VmL溶液。该的石中铁元素的质量分数为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 ,还含有
,还含有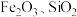 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的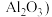 ,某研究性学习小组设计了如图提取流程:
,某研究性学习小组设计了如图提取流程: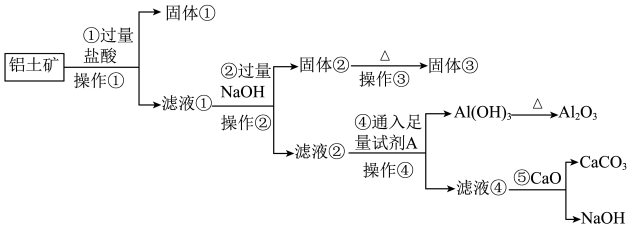
(1)固体①、③的化学式分别为
(2)操作①的名称是
(3)流程中的
 最好选用
最好选用(4)若向滤液(1)中逐滴滴入
 溶液至过量,产生沉淀随
溶液至过量,产生沉淀随 滴入关系正确的是___________。
滴入关系正确的是___________。
|
|
|
|
| A.A | B.B | C.C | D.D |
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为
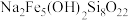 ,该物质中+2价铁与+3价铁的物质的量之比为。将
,该物质中+2价铁与+3价铁的物质的量之比为。将 该矿石用足量硫酸溶解后,加入过量铜粉使溶液中的铁元素全部变为
该矿石用足量硫酸溶解后,加入过量铜粉使溶液中的铁元素全部变为 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去VmL溶液。该的石中铁元素的质量分数为
反应,用去VmL溶液。该的石中铁元素的质量分数为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】川菜之魂在味,然而在“七味八滋”中,盐应是百味之首。自贡市位于四川盆地南部,智慧的自贡人早在2000年前就开始了用盐井采盐,在咸丰、同治年间自贡逐渐成为四川盐业中心之一。但刚从盐井中采出的粗盐水因含有Na2SO4、MgCl2、CaCl2和泥沙等,需经过提纯才能被食用。图中展示了一种在实验室用该粗盐水制取NaCl晶体的操作流程:

请回答下列问题:
(1)加BaCl2溶液涉及到的离子方程式:_______ ;
(2)加Na2CO3溶液涉及到的离子方程式_______ ; _______ ;
(3)试剂I和试剂II分别为_______ 、 _______ ;添加试剂II涉及到的离子方程式_______ ; _______ ;
(4)第⑥的实验操作为_______ ;操作流程中,BaCl2溶液和Na2CO3溶液的添加顺序可不可以调换,理由是_______ 。

请回答下列问题:
(1)加BaCl2溶液涉及到的离子方程式:
(2)加Na2CO3溶液涉及到的离子方程式
(3)试剂I和试剂II分别为
(4)第⑥的实验操作为
您最近一年使用:0次