下列说法正确的是
| A.增大压强,活化分子百分数增大,化学反应速率一定增大 |
| B.升高温度,活化分子百分数增大,化学反应速率一定增大 |
| C.加入反应物,使活化分子百分数增大,化学反应速率一定增大 |
| D.所有的催化剂都可以降低反应的活化能,但一定不改变反应的历程 |
更新时间:2022-10-26 22:44:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体②H2O③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
①NaOH固体②H2O③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
| A.②④⑥ |
| B.①② |
| C.②③⑤ |
| D.②④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。
据表中的递变规律,推测O3分别在条件①40℃、pH=3.0,②10℃、pH=4.0,③30℃、pH=7.0下,分解速率依次增大的顺序为
| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
| A.①②③ | B.③②① | C.②①③ | D.③①② |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验操作中,对应的实验现象以及实验结论都正确,且两者具有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有浓氨水的锥形瓶中缓慢通入O2,用红热的Pt丝在液面上轻轻挥动 | Pt丝保持红热 | NH3和O2的反应是放热反应 |
| B | 向稀硝酸中加入过量铁粉,充分反应后,再滴加KSCN溶液 | 溶液无明显现象 | 稀硝酸只能将Fe氧化为Fe2+ |
| C | 向NaCl和NaI混合溶液中,滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgC1)>Ksp(AgI) |
| D | 向两支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%双氧水 | 产生气泡快慢不同 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家研究了不同含金化合物催化乙烯加氢[C2H4(g)+H2(g)=C2H6(g) △H=akJ·mol-1]的反应历程如下图所示,下列说法正确的是


| A.1molC2H4(g)与1molH2(g)具有的能量之和小于1molC2H6(g)的能量 |
| B.过渡态物质的稳定性:过渡态1>过渡态2 |
| C.该反应的焓变:ΔH=—129.6kJ·mol-1 |
D.相应的活化能:催化剂AuF<催化剂AuPF |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是( )
| A.活化分子之间的碰撞不一定都是有效碰撞 |
| B.升高温度,可使单位体积内活化分子增多,反应速率加快 |
| C.对于有气体参加的反应增大压强,可使单位体积内活化分子百分数增加,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。

下列说法正确的是

下列说法正确的是
| A.HAP能降低HCHO与O2的反应的活化能,增大了平衡转化率 |
| B.该历程中有非极性键的断裂,没有非极性键形成 |
| C.HCHO分子中σ键与π键之比为2:1 |
| D.根据图示信息,CO2分子中的氧原子全部来自O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应A+B→P符合Arrhenius公式,[已知Arrhenius经验公式为Rlnk=–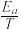 +C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
+C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
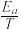 +C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
+C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。| A.2×105 | B.1014 | C.5000 | D.29×1012 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某反应A(g)+B(g)→C(g)+D(g) 的速率方程为v=kcm(A)·cn(B), 其中k是反应速率常数,受温度、催化剂的影响。其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为 0.8/k。改变反应物浓度时,反应的瞬时速率如表所示;
下列说法不正确的是
| c(A)/(mol·L-1) | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 | c1 |
| c(B)/(mol·L-1) | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 | c2 |
| v/(10-3mol·L-1·min-1) | 1.6 | 3.2 | v1 | 3.2 | v2 | 4.8 |
| A.上述表格中的c1=0.75、v1=6.4 |
| B.该反应的速率常数k=6.4×10-3min-1 |
| C.在过量的B 存在时,反应掉75%的A 所需的时间是250 min |
| D.升温、加入催化剂、缩小容积(加压),均可使k增大导致反应的瞬时速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2和H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列说法错误的是


| A.HAP能提高HCHO与O2的反应速率的原因是降低了反应的活化能 |
| B.HCHO在反应过程中,有C—H键的断裂和C=O键形成 |
| C.根据图示信息,CO2分子中的氧原子全部来自O2 |
| D.HCHO和CO2均只含有极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O的分解速率方程v=k·c(N2O)·c0.5(I2)(k为速率常数)。下列表述正确的是
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O的分解速率方程v=k·c(N2O)·c0.5(I2)(k为速率常数)。下列表述正确的是
| A.I2浓度与N2O分解速率无关 | B.第三步对总反应速率起决定作用 |
| C.IO为反应的中间产物 | D.第二步活化能比第三步小 |
您最近一年使用:0次

 。已知:
。已知: ,
, (R、C为常数,k为速率常数,Ea为活化能,T为温度)。实验测得 Rlnk 与
(R、C为常数,k为速率常数,Ea为活化能,T为温度)。实验测得 Rlnk 与 的关系如图所示。
的关系如图所示。


