在CH3COOH CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
 CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是| A.升高温度 | B.增大压强 | C.加少量NaOH固体 | D.通入HCl |
更新时间:2022-11-16 20:09:17
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,向10mL0.1mol·L-1氨水(pH约为8)中加入蒸馏水,将其稀释到1L后,下列说法不正确的是
| A.NH3·H2O的电离程度增大 | B.稀释后的溶液pH<7 |
C.n( )增大 )增大 | D. 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
A.常温下,由水电离产生的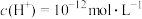 的溶液中: 的溶液中: 、 、 、 、 、 、 大量共存 大量共存 |
| B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a>b+1 |
C.次氯酸钠溶液中通少量 : : |
D.电解氯化镁溶液: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
| D.将水加热,KW增大,pH不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】设NA为阿伏加 德罗常数值。关于常温下pH=2的H3PO4溶液,下列说法正确的是
| A.每升溶液中的H+数目为0.02NA |
B.c(H+)= c( )+2c( )+2c( )+3c( )+3c( )+ c(OH−) )+ c(OH−) |
| C.加水稀释使电离度增大,溶液pH减小 |
| D.加入NaH2PO4固体,溶液酸性增强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下表是几种弱酸常温下的电离平衡常数:
则下列说法中不正确的是( )
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
| A.碳酸的酸性强于氢硫酸 |
| B.多元弱酸的酸性主要由第一步电离决定 |
| C.常温下,加水稀释醋酸,电离平衡常数增大 |
| D.向弱酸溶液中加少量NaOH溶液,电离平衡常数不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】醋酸溶液中存在电离平衡 CH3COOH H++ CH3COO-,下列叙述不正确的是( )
H++ CH3COO-,下列叙述不正确的是( )
 H++ CH3COO-,下列叙述不正确的是( )
H++ CH3COO-,下列叙述不正确的是( )| A.升高温度,平衡正向移动,醋酸的电离常数 Ka 值增大 |
| B.0.10 mol·L-1 的 CH3 COOH 溶液中加水稀释,溶液中 c(H+)减小 |
| C.CH3COOH 溶液中加少量的 CH3COONa 固体,平衡逆向移动 |
| D.25℃时,欲使醋酸的电离常数 Ka 和电离程度都减小,可加入少量冰醋酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】20℃时H2S饱和溶液1L,其浓度为0.1mol/L,其电离方程式为H2S HS-+H+,HS-
HS-+H+,HS- H++S2-,若要使溶液中c(H+)和c(S2-)都减小,可采用的措施是
H++S2-,若要使溶液中c(H+)和c(S2-)都减小,可采用的措施是
 HS-+H+,HS-
HS-+H+,HS- H++S2-,若要使溶液中c(H+)和c(S2-)都减小,可采用的措施是
H++S2-,若要使溶液中c(H+)和c(S2-)都减小,可采用的措施是| A.加入适量的水 | B.加入适量的NaOH固体 |
| C.通入少量CO2 | D.加入适量的CuSO4固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,将 的盐酸与
的盐酸与 的氨水等体积混合,关于该溶液酸碱性的描述正确的是
的氨水等体积混合,关于该溶液酸碱性的描述正确的是
 的盐酸与
的盐酸与 的氨水等体积混合,关于该溶液酸碱性的描述正确的是
的氨水等体积混合,关于该溶液酸碱性的描述正确的是| A.可能显中性 | B.一定显碱性 | C.不可能显碱性 | D.可能显酸性 |
您最近一年使用:0次

 保持不变
保持不变 H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是(
H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是(

