高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
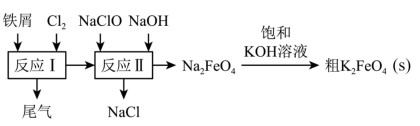
下列叙述不正确的是

下列叙述不正确的是
| A.反应I产生的尾气可通入碱液中吸收 |
| B.反应I生成的FeCl2,在碱性条件下会被NaClO氧化成Na2FeO4 |
| C.反应II中每转移6mol电子会生成166gNa2FeO4 |
| D.Na2FeO4转化成K2FeO4的化学方程式为Na2FeO4+2KOH=K2FeO4↓+2NaOH |
更新时间:2022-11-23 18:19:06
|
相似题推荐
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】工业生产中高锰酸钾广泛用作氧化剂。以二氧化锰为原料制取高锰酸钾晶体的流程如下:
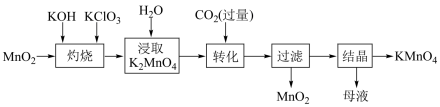
下列说法正确的是

下列说法正确的是
| A.“灼烧”时使用石英坩埚 |
| B.“转化”过程生成KMnO4和MnO2的物质的量之比为2:1 |
| C.母液中含有的溶质主要是KHCO3 |
| D.上述流程中可以循环利用的物质有3种 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】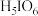 是一种弱酸,可通过下列方法制备:
是一种弱酸,可通过下列方法制备:

下列说法正确的是
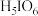 是一种弱酸,可通过下列方法制备:
是一种弱酸,可通过下列方法制备:
下列说法正确的是
A.室温下, 的溶解度比 的溶解度比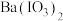 的小 的小 |
B.反应②的化学方程式为 |
C.反应③的产物中 |
| D.反应④中酸X可选用盐酸或硝酸 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】向含Fe2+、I-、Br-的溶液中通入过量的氯气。溶液中四种粒子的物质的量变化如图所示。已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法正确的是
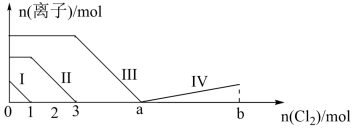

| A.线段Ⅱ表示Br-的变化情况 | B.原溶液中n(FeI2):n(FeBr2)=3:1 |
| C.根据图象可以计算出b的值为11 | D.线段Ⅳ表示IO 的变化情况 的变化情况 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量Cl2,溶液中某些离子的物质的量变化如图所示,下列说法正确的是( )


| A.三种离子的还原性强弱关系是:Br->Fe2+>I- |
| B.A点表示Fe2+正好反应了一半 |
| C.原溶液中:n(Fe2+)︰n(I-)︰n(Br-)=2︰1︰3 |
| D.当通入2.5molCl2时,溶液中已发生的离子反应可表示为:6Fe2++4I-+5Cl2=6Fe3++2I2+10Cl- |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】氟锑酸( )属于超强酸,可通过
)属于超强酸,可通过 与HF反应制得。实验室以
与HF反应制得。实验室以 、
、 为原料制备
为原料制备 的装置如图所示,反应原理为
的装置如图所示,反应原理为 。其他信息如下:
。其他信息如下:
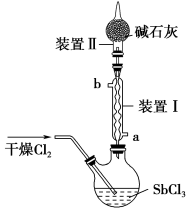
下列说法错误的是
 )属于超强酸,可通过
)属于超强酸,可通过 与HF反应制得。实验室以
与HF反应制得。实验室以 、
、 为原料制备
为原料制备 的装置如图所示,反应原理为
的装置如图所示,反应原理为 。其他信息如下:
。其他信息如下:
| 物质 | 性质 |
 | 熔点73.4℃,沸点220.3℃,易水解 |
 | 熔点3.5℃,140℃时沸腾并分解,易水解 |
| A.装置Ⅰ中的b为冷凝水的出水口 |
B.装置Ⅱ可吸收 和空气中的水蒸气 和空气中的水蒸气 |
C. 制备完成后,将通 制备完成后,将通 改通HF,完成 改通HF,完成 的制备 的制备 |
D. 制备完成后,对 制备完成后,对 进行提纯时可采用常压蒸馏分离 进行提纯时可采用常压蒸馏分离 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为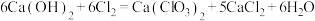 。充分反应后过滤。
。充分反应后过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为
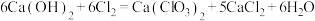 。充分反应后过滤。
。充分反应后过滤。步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
A.控制通入 的速率,可以提高 的速率,可以提高 的利用率 的利用率 |
B.25℃时, 的溶解度比 的溶解度比 的溶解度大 的溶解度大 |
C.步骤2中,过滤所得滤液中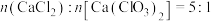 |
D.生成 的化学方程式为 的化学方程式为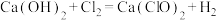 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】 是锂离子电池正极材料,晶体中
是锂离子电池正极材料,晶体中 围绕
围绕 形成八面体,八面体共棱形成层状空间结构,与
形成八面体,八面体共棱形成层状空间结构,与 层交替排列。在充放电过程中,
层交替排列。在充放电过程中, (Ⅲ)与
(Ⅲ)与 (Ⅳ)相互转化,
(Ⅳ)相互转化, 在层间脱出或嵌入,晶胞组成变化如图所示。下列说法正确的是
在层间脱出或嵌入,晶胞组成变化如图所示。下列说法正确的是
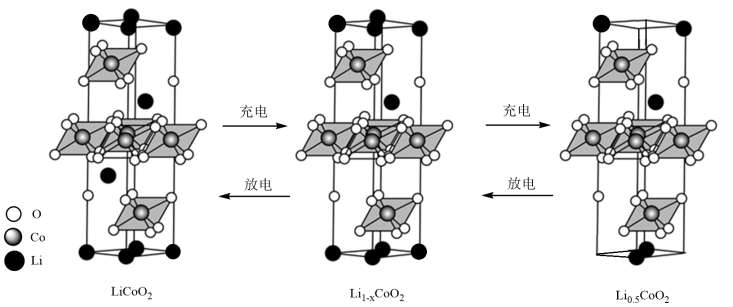
 是锂离子电池正极材料,晶体中
是锂离子电池正极材料,晶体中 围绕
围绕 形成八面体,八面体共棱形成层状空间结构,与
形成八面体,八面体共棱形成层状空间结构,与 层交替排列。在充放电过程中,
层交替排列。在充放电过程中, (Ⅲ)与
(Ⅲ)与 (Ⅳ)相互转化,
(Ⅳ)相互转化, 在层间脱出或嵌入,晶胞组成变化如图所示。下列说法正确的是
在层间脱出或嵌入,晶胞组成变化如图所示。下列说法正确的是
A. 中 中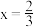 |
B.每个 晶胞中 晶胞中 与Co(Ⅳ)个数比为 与Co(Ⅳ)个数比为 |
C.每个 晶胞转化为 晶胞转化为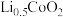 晶胞转移的电子数为4 晶胞转移的电子数为4 |
D.相同质量的 分别转化为 分别转化为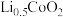 与 与 转移电子数之比为 转移电子数之比为 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2,其过程如下。
过程I:Fe3O4→FeO+O2(未配平);
过程II:FeO+H2O→H2+Fe3O4(未配平)。
下列说法不正确的是
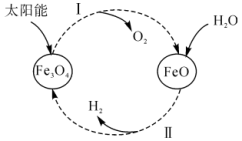
过程I:Fe3O4→FeO+O2(未配平);
过程II:FeO+H2O→H2+Fe3O4(未配平)。
下列说法不正确的是

| A.过程Ⅰ的反应中还原产物是FeO |
| B.过程Ⅰ的反应中每生成12mol FeO转移8mol电子 |
| C.FeO在分解水制H2的过程中作催化剂 |
| D.过程Ⅱ的反应中FeO和H2O的化学计量数之比为2:1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】F2和Xe在一定条件下生成氧化性极强且极易与水反应的XeF2、XeF4和XeF6三种化合物。其中XeF4与H2O可以发生如下反应:6XeF4+12H2O=2XeO3+4Xe↑+24HF+3O2↑。下列判断正确的是
| A.XeF2加入水中,在水分子的作用下,将重新生成Xe和F2 |
| B.XeF4按以上方式与水反应,每生成3mol O2转移12mol电子 |
| C.上述反应中氧化剂和还原剂的物质的量之比为1:2 |
| D.XeF2、XeF4和XeF6在空气中都不能长期存放 |
您最近一年使用:0次

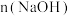 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断正确的是
三种溶质。下列判断正确的是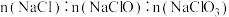 可能为
可能为
 ,则
,则
 可能为
可能为


