以粉煤灰(主要成分:Al2O3、SiO2、少量Fe2O3)为原料,制取Al2O3的部分工艺流程如下:

完成下列填空:
(1)铝原子核外有_______ 种不同能量的电子,最外层电子的轨道式是_______ ,上述流程涉及第二周期元素的原子半径由小到大的顺序是_______ 。
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为_______ ,检验溶液中Fe3+是否除尽的方法是_______ 。
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。_______
(4)上述流程可循环的物质是_______ 。
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是_______ 。

完成下列填空:
(1)铝原子核外有
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。
(4)上述流程可循环的物质是
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是
更新时间:2022-11-24 09:10:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上常用铝土矿(主要成分为Al2O3,SiO2和Fe2O3等杂质)为原料制备铝氢化钠,铝氢化钠(NaAlH4)是有机合成的重要还原剂,工艺流程如下:

已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。
(1)过量NaOH溶液溶解铝土矿时为了提高浸出率可采取的措施是_______ 。(任写一种)
(2)电解I的化学方程式_______ 。
(3)“灼烧”操作用到的主要仪器有_______ 、_______ 、三脚架、玻璃棒、酒精灯、坩埚钳。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。

物质A为_______ 。(填化学式)
(5)反应III的化学方程式为_______ ,某同学经过分析认为可以再设计一个电解槽,电解_______ (填物质名称)溶液,更能实现副产物的循环利用。
(6)某同学认为该制备工艺也可以先酸溶,再加入NaOH溶液,当溶液中铁离子沉淀完全时,此时溶液pH是_______ 。(一般认为室温下离子浓度小于10-5mol/L时沉淀完全;Ksp[Fe(OH)3]=1×10-35,Ksp[Al(OH)3]=3×10-34)

已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。
(1)过量NaOH溶液溶解铝土矿时为了提高浸出率可采取的措施是
(2)电解I的化学方程式
(3)“灼烧”操作用到的主要仪器有
(4)“电解II”是电解Na2CO3溶液,原理如图所示。

物质A为
(5)反应III的化学方程式为
(6)某同学认为该制备工艺也可以先酸溶,再加入NaOH溶液,当溶液中铁离子沉淀完全时,此时溶液pH是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为___________
(2)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)取金属铝的流程如下:
,不考虑其他杂质)取金属铝的流程如下:
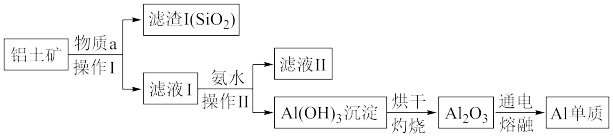
①操作Ⅰ所加物质a为___________ (选填 或NaOH),
或NaOH), 与a反应的离子方程式为
与a反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
③工业上在电解熔融的 时,还加入了冰晶石
时,还加入了冰晶石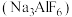 作熔剂,其作用是降低
作熔剂,其作用是降低 的熔点。冰晶石在物质的分类中属于
的熔点。冰晶石在物质的分类中属于___________ (填字母)。
a.酸 b.碱 c.盐 d.氧化物
(3)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,完善并配平该反应:
,完善并配平该反应: ,
,___________ 。每消耗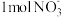 ,转移的电子数目为
,转移的电子数目为___________ 。
(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化 ,也能氧化
,也能氧化 。
。
①取 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性: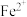
___________  (填“>”或“<”)。
(填“>”或“<”)。
②若在 溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈___________ 色,写出该反应的离子方程式___________ 。
(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为
(2)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)取金属铝的流程如下:
,不考虑其他杂质)取金属铝的流程如下:
①操作Ⅰ所加物质a为
 或NaOH),
或NaOH), 与a反应的离子方程式为
与a反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
③工业上在电解熔融的
 时,还加入了冰晶石
时,还加入了冰晶石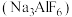 作熔剂,其作用是降低
作熔剂,其作用是降低 的熔点。冰晶石在物质的分类中属于
的熔点。冰晶石在物质的分类中属于a.酸 b.碱 c.盐 d.氧化物
(3)铝与
 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,完善并配平该反应:
,完善并配平该反应: ,
,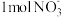 ,转移的电子数目为
,转移的电子数目为(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化
 ,也能氧化
,也能氧化 。
。①取
 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性: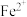
 (填“>”或“<”)。
(填“>”或“<”)。②若在
 溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为_______ 。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式_______ 、_______ 、_______ ;Ⅲ中通入足量CO2气体发生反应的离子方程式为_______ 。
(3)由Ⅲ中得到滤液c的实验操作为_______ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_______ 、冷却结晶、过滤洗涤。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______ 。

请回答下列问题:
(1)固体a的化学式为
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式
(3)由Ⅲ中得到滤液c的实验操作为
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①—⑧在表中的位置,用化学用语回答下列问题:
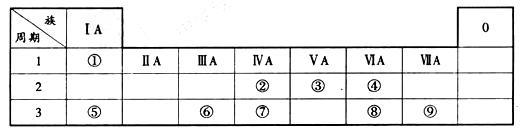
(1)④、⑤、⑥的原子半径由大到小的顺序为(填元素符号)________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式)________ 。
(3)①、④,⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中任意一种化合物的电子式:________ 。
(4)由②和④组成,且②和④的质量比为3:8的化合物的结构式是________ 。
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为_________ 。
(6)⑧、⑨两元素非金属性较强的是(写元素符号)_____ ,举二个例子说明推断依据:_______ 。

(1)④、⑤、⑥的原子半径由大到小的顺序为(填元素符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)①、④,⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中任意一种化合物的电子式:
(4)由②和④组成,且②和④的质量比为3:8的化合物的结构式是
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为
(6)⑧、⑨两元素非金属性较强的是(写元素符号)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】针对下表中的9种元素,用化学用语回答下列问题:
(1)写出⑧的原子结构示意图:_________________________ 。
(2)形成物质种类最多的元素是__________________ 。
(3)用电子式表示⑤和⑨形成化合物的过程__________________ 。
(4)⑤⑥⑦最高正价氧化物对应水化物碱性由强至弱的顺序是_____________ 。
(5)④的单质与甲醇(CH3OH)形成的碱性燃料电池的负极方程式:________________ 。
(6)写出⑦的单质与三氧化二铁反应的化学方程式____________________ 。
(7)③和④的气态氢化物的稳定性顺序为:______________ 。④和⑧的气态氢化物的沸点顺序为:_____________ ,出现这种变化的原因是:_____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
(2)形成物质种类最多的元素是
(3)用电子式表示⑤和⑨形成化合物的过程
(4)⑤⑥⑦最高正价氧化物对应水化物碱性由强至弱的顺序是
(5)④的单质与甲醇(CH3OH)形成的碱性燃料电池的负极方程式:
(6)写出⑦的单质与三氧化二铁反应的化学方程式
(7)③和④的气态氢化物的稳定性顺序为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:___________ ,其最高能层的电子占据的原子轨道电子云轮廓为___________ 形。若将其最高价氧化物的水化物溶于氨水中可得到一种透明的深蓝色溶液,写出反应的化学方程式为:___________ 。
(2)第二周期所有元素中第一电离能介于①②之间的有___________ 种。由②③④形成的简单离子半径由小到大顺序是___________ (填化学用语)。
(3)元素⑦⑧可形成原子个数比为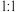 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子为
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子为___________ (填“极性分子”或“非极性分子”)。
(4)元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式___________ ,它的熔点高,硬度大,电绝缘性好,化学性质稳定,它的晶体类型是___________ 。
(5)下列有关性质的比较正确且能用元素周期律解释的是___________(填标号)
(6)⑩可形成的卤化物的熔点如下表:
⑩的氟化物熔点比氯化物熔点高很多的原因是___________ 。
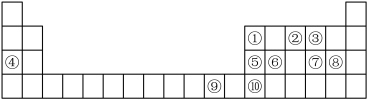
(2)第二周期所有元素中第一电离能介于①②之间的有
(3)元素⑦⑧可形成原子个数比为
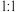 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子为
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子为(4)元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式
(5)下列有关性质的比较正确且能用元素周期律解释的是___________(填标号)
| A.电负性:②>③ | B.氢化物的稳定性:③>⑦ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ | D.氢化物的沸点:③>⑦ |
(6)⑩可形成的卤化物的熔点如下表:
| 卤化物 | 氟化物 | 氯化物 | 溴化物 |
| 熔点℃ | >1000 | 77.75 | 122.3 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知a、b、c、d、e、f是中学化学中常见的七种元素,其结构或者性质信息如下表所示:
(1)元素a的原子核外有___________ 种不同能级的电子。
(2)b、c的第一电离能的大小顺序为___________ (填元素符号),a、c的简单气态氢化物中,更稳定的是___________ (填化学式)。
(3)e元素基态原子的价电子轨道表示式为___________ 。
(4)元素f位于周期表中___________ 区,在f元素的同主族元素中,最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
(5)b元素与氢元素形成的10电子分子的的空间构型为___________ 。
| 元素 | 结构或者性质信息 |
| a | 原子的L层上s能级电子数等于p能级电子数 |
| b | 非金属元素,其单质为气态,有多种氧化物且都是大气污染物 |
| c | 原子的最外层电子数是内层电子数的3倍 |
| d | 元素的正三价离子的3d能级为半充满 |
| e | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
| f | 单质常温、常压下是易挥发的液体,基态原子的N层上有1个未成对的p电子 |
(2)b、c的第一电离能的大小顺序为
(3)e元素基态原子的价电子轨道表示式为
(4)元素f位于周期表中
(5)b元素与氢元素形成的10电子分子的的空间构型为
您最近一年使用:0次
【推荐2】铜是人类最早使用的金属之一。回答下列问题:
(1)基态铜原子的价层电子排布图为___________ 。
(2)向 溶液中加入足量氨水得到深蓝色
溶液中加入足量氨水得到深蓝色 溶液,再向其中加入盐酸羟胺(
溶液,再向其中加入盐酸羟胺(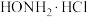 )至溶液变为无色,再通入
)至溶液变为无色,再通入 后析出
后析出 红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是
红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是___________ (填元素符号); 的空间结构名称为
的空间结构名称为___________ ; 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为___________ ; 在水中的溶解度较小的原因是
在水中的溶解度较小的原因是___________ ; 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为___________ 。
(3)上述 、
、 的晶体类型都属于下列中的___________(填标号)。
的晶体类型都属于下列中的___________(填标号)。
(4)铜和氧形成的一种离子化合物的晶体结构如图所示。若其晶胞边长为a pm,阿伏加德罗常数值为 ,则该晶体密度为
,则该晶体密度为___________  。
。
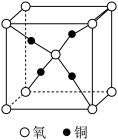
(1)基态铜原子的价层电子排布图为
(2)向
 溶液中加入足量氨水得到深蓝色
溶液中加入足量氨水得到深蓝色 溶液,再向其中加入盐酸羟胺(
溶液,再向其中加入盐酸羟胺(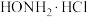 )至溶液变为无色,再通入
)至溶液变为无色,再通入 后析出
后析出 红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是
红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是 的空间结构名称为
的空间结构名称为 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为 在水中的溶解度较小的原因是
在水中的溶解度较小的原因是 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为(3)上述
 、
、 的晶体类型都属于下列中的___________(填标号)。
的晶体类型都属于下列中的___________(填标号)。| A.分子晶体 | B.共价晶体 | C.金属晶体 | D.离子晶体 |
 ,则该晶体密度为
,则该晶体密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】有A,B,C,D,E五种元素,其中A,B,C,D为短周期元素,A元素的周期数、主族数、原子序数相同;B原子核外有3种能量不同的原子轨道且每种轨道中的电子数相同;C原子的价电子构型为csccpc+1,D元素的原子最外层电子数比次外层电子数少2个,D的阴离子与E的阳离子电子层结构相同,D和E可形成化合物E2D。
回答下列问题:
(1) C原子的价电子构型为csccpc+1,其中c为________ , C原子的名称为__________ ;
(2)上述元素中,第一电离能最小的元素的原子结构示意图为__________________ ;
D的价电子排布图为______________________ ;E2D的电子式为__________________ ;
(3) 下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.
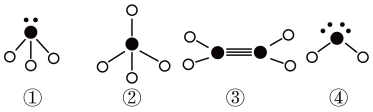
则在以上分子中,中心原子采用sp3杂化形成化学键的是___________ (填写分子的化学式);
②分子中的键角是_____________ ; 在③的分子中有_______ 个σ键和_______ 个π键。
回答下列问题:
(1) C原子的价电子构型为csccpc+1,其中c为
(2)上述元素中,第一电离能最小的元素的原子结构示意图为
D的价电子排布图为
(3) 下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是
②分子中的键角是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验室把学生做完实验后的废液(含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下:
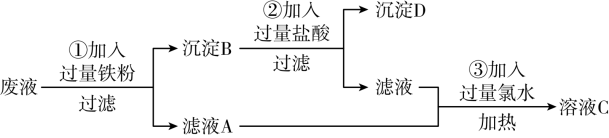
(1)沉淀D的化学式为_________________ 。
(2)反应③中Cl2属于_______________ (填“氧化剂”或“还原剂”)。
(3)写出①反应中的离子方程式________________________ ,___________________________ 。
(4)溶液C中的溶质是_______________ (提示:加热后,溶液中没有了HCl和Cl2),若要进一步进行分离,方法是____________________ 。
(5)萃取实验所用到的玻璃仪器:_______________ 、____________________ 。

(1)沉淀D的化学式为
(2)反应③中Cl2属于
(3)写出①反应中的离子方程式
(4)溶液C中的溶质是
(5)萃取实验所用到的玻璃仪器:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学实验兴趣小组学生为探究苯与溴发生反应的原理,用如图所示装置进行了实验。根据相关知识回答下列问题:
(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,写出Ⅱ中发生反应的化学方程式(有机物写结构简式):_______ ,反应类型为_______ 。过一会儿,在装置Ⅲ中可能观察到的现象是_______ 。
(2)整套实验装置中能防止倒吸的装置有_______ (填装置序号)。
(3)本实验能不能用溴水代替液溴?_______ 。
(4)采用冷凝装置,其作用是_______ 。
(5)装置Ⅲ中小试管内苯的作用是_______ 。
(6)向Ⅱ中分离出的油状液体中加入少量无水氯化钙,静置、过滤。加入无水氯化钙的目的是_______ 。
(7)经以上分离操作后、粗溴苯中还含有的主要杂质为_______ ,要进一步提纯,下列操作中必需的是_______ (填字母)。
A.蒸发 B.过滤 C.蒸馏 D.萃取

| 苯 | 溴 | 溴苯 | |
| 密度/(g·cm-3) | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水溶性 | 微溶 | 微溶 | 微溶 |
(2)整套实验装置中能防止倒吸的装置有
(3)本实验能不能用溴水代替液溴?
(4)采用冷凝装置,其作用是
(5)装置Ⅲ中小试管内苯的作用是
(6)向Ⅱ中分离出的油状液体中加入少量无水氯化钙,静置、过滤。加入无水氯化钙的目的是
(7)经以上分离操作后、粗溴苯中还含有的主要杂质为
A.蒸发 B.过滤 C.蒸馏 D.萃取
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】溴化钙是一种重要的化工原料,常见有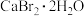 和
和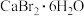 等结晶形式。某兴趣小组以废铁屑为原料制备的主要流程如下:
等结晶形式。某兴趣小组以废铁屑为原料制备的主要流程如下:

已知:34℃时结晶得到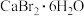 ,
,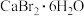 加热至210℃得到
加热至210℃得到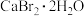 。
。
请回答:
(1)步骤①中加 溶液是为了除去废铁屑表面的油污(主要成分为油脂),加热的目的是
溶液是为了除去废铁屑表面的油污(主要成分为油脂),加热的目的是___ (用简要文字和必要的离子方程式说明)。
(2)步骤④调 所用的试剂应选择
所用的试剂应选择_______ 。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
(3)步骤⑤多步操作包括_______ 、_______ 、过滤、洗涤、_______ 。
(4)下列有关说法不正确 的是_______ 。
A.步骤②反应控制在40℃左右的原因是防止反应过于剧烈并减少液溴挥发
B.为充分利用铁屑,应加入稍过量的液溴使铁屑完全溶解
C. 步骤③过滤时,应用玻璃纤维代替滤纸
D.下图装置过滤结束时可先打开止水夹a后直接关闭水龙头;

(5)兴趣小组模拟海水提取溴的过程,用苯萃取稀溴水中的溴,选出其正确操作并按顺序列出字母:
涂凡士林→检漏→ → → → → →清洗干净,________ 。
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和苯转移至分液漏斗中,塞上玻璃塞
d.右手压住玻璃塞,左手握住旋塞,将分液漏斗上下颠倒振荡
e.右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下口放出溴的苯溶液
h.从上口倒出溴的苯溶液
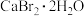 和
和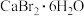 等结晶形式。某兴趣小组以废铁屑为原料制备的主要流程如下:
等结晶形式。某兴趣小组以废铁屑为原料制备的主要流程如下:
已知:34℃时结晶得到
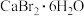 ,
,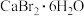 加热至210℃得到
加热至210℃得到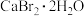 。
。请回答:
(1)步骤①中加
 溶液是为了除去废铁屑表面的油污(主要成分为油脂),加热的目的是
溶液是为了除去废铁屑表面的油污(主要成分为油脂),加热的目的是(2)步骤④调
 所用的试剂应选择
所用的试剂应选择A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液(3)步骤⑤多步操作包括
(4)下列有关说法
A.步骤②反应控制在40℃左右的原因是防止反应过于剧烈并减少液溴挥发
B.为充分利用铁屑,应加入稍过量的液溴使铁屑完全溶解
C. 步骤③过滤时,应用玻璃纤维代替滤纸
D.下图装置过滤结束时可先打开止水夹a后直接关闭水龙头;

(5)兴趣小组模拟海水提取溴的过程,用苯萃取稀溴水中的溴,选出其正确操作并按顺序列出字母:
涂凡士林→检漏→ → → → → →清洗干净,
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和苯转移至分液漏斗中,塞上玻璃塞
d.右手压住玻璃塞,左手握住旋塞,将分液漏斗上下颠倒振荡
e.右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下口放出溴的苯溶液
h.从上口倒出溴的苯溶液
您最近一年使用:0次



