室温下,依次进行如下实验:
①取一定量冰醋酸,配制成100mL0.1mol/L醋酸溶液
②取20mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
③继续滴加a mL0.1mol/L稀盐酸,至溶液的pH=7;
④再取10mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
⑤向①中剩余醋酸溶液中逐滴加入0.1mol/L氨水至过量,用电导率传感器实时测量该过程中溶液的电导率(溶液导电性越强,电导率越大)。
(1)用化学用语解释醋酸溶液pH<7的原因:_______ ,另外配制100mL与①中醋酸溶液等pH的盐酸,分别取10mL上述两种溶液,各加入10mL蒸馏水,稀释后醋酸溶液的pH_______ 盐酸(>、=或<)。
(2)②中反应后的溶液中离子浓度由大到小 的顺序为_______ (用离子符号表示即可)。
(3)a___ 20mL(>、=或<,下同);③中反应后的溶液:
____  。
。
(4)④中反应后的溶液中各微粒浓度存在如下关系: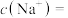
_____ 
____ 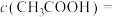
_____ mol/L。
(5)请你预测⑤中滴入氨水过程中电导率的变化情况:_______ 。
①取一定量冰醋酸,配制成100mL0.1mol/L醋酸溶液
②取20mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
③继续滴加a mL0.1mol/L稀盐酸,至溶液的pH=7;
④再取10mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
⑤向①中剩余醋酸溶液中逐滴加入0.1mol/L氨水至过量,用电导率传感器实时测量该过程中溶液的电导率(溶液导电性越强,电导率越大)。
(1)用化学用语解释醋酸溶液pH<7的原因:
(2)②中反应后的溶液中离子浓度由
(3)a

 。
。(4)④中反应后的溶液中各微粒浓度存在如下关系:
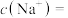

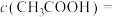
(5)请你预测⑤中滴入氨水过程中电导率的变化情况:
22-23高三上·北京顺义·期中 查看更多[2]
更新时间:2022-11-24 23:06:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填空:
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水,
a.其中能导电的是(填编号,下同):_______ ;属于电解质的是_______ ;属于非电解质的是:_______ 。
b.请写出③和⑨反应的离子方程式_______
c.过量的①和少量的④在水溶液中的离子方程式为_______
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,把方程式补充完整并配平:______
_______ClO-+_______Fe3++_______=_______ _______Cl-+_______H2O
_______Cl-+_______H2O
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水,
a.其中能导电的是(填编号,下同):
b.请写出③和⑨反应的离子方程式
c.过量的①和少量的④在水溶液中的离子方程式为
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,把方程式补充完整并配平:
_______ClO-+_______Fe3++_______=_______
 _______Cl-+_______H2O
_______Cl-+_______H2O
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在下列物质中,可以导电的是___________ (填序号,下同),是电解质的有___________ 。
①干燥的氯化钠晶体 ②干燥的碳酸氢钠固体 ③蔗糖晶体 ④酒精 ⑤NaHSO4溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧Ba(OH)2溶液
(2)向盛有⑧的烧杯中逐滴加入⑤,当溶液中的Ba2+恰好沉淀完全时,发生反应的离子方程式为___________ 。
(3)向一定量②的水溶液中加入少量⑧,发生反应的离子方程式为___________ 。
(4)某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、 、
、 、
、 。现进行如下实验:
。现进行如下实验:
①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定有___________ ,肯定没有___________ 。
(1)在下列物质中,可以导电的是
①干燥的氯化钠晶体 ②干燥的碳酸氢钠固体 ③蔗糖晶体 ④酒精 ⑤NaHSO4溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧Ba(OH)2溶液
(2)向盛有⑧的烧杯中逐滴加入⑤,当溶液中的Ba2+恰好沉淀完全时,发生反应的离子方程式为
(3)向一定量②的水溶液中加入少量⑧,发生反应的离子方程式为
(4)某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、
 、
、 、
、 。现进行如下实验:
。现进行如下实验:①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知表数据:
(1))25 ℃时,等浓度的四种溶液:a.NaCN溶液;b.Na2CO3溶液;c.CH3COONa 溶液;d.NaHCO3溶液。pH由大到小的顺序为______ (填写字母标号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为__________ ;
(3)将0.2mol/L HCN溶液和0.1mol/L的NaOH溶液等体积混合后,溶液显碱性,则混合溶液中c(HCN)、c(H+)、c(OH-)、c(CN-)、c(Na+)浓度从大到小的排序为__________ ,
c(HCN)+c(CN-)=__________ mol/L(忽略混合后溶液的体积变化)。
(4)写出NaHCO3溶液中的质子守恒式:______________________ 。
(5)相同条件下,取等体积等pH的:a.HCN溶液;b.CH3COOH溶液;c.H2CO3溶液。
各稀释100倍,稀释后的溶液,其pH从大到小的排序为__________ (填字母标号)。
(6)25 ℃时,将体积为Va、pH=13的某一元强碱与体积为Vb、pH=2的某二元强酸混合,若所得溶液的pH=11,则Va:Vb=__________ (忽略混合后溶液的体积变化)。
| 化学式 | 电离平衡常数(25 ℃) |
| HCN | K=5.0×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1))25 ℃时,等浓度的四种溶液:a.NaCN溶液;b.Na2CO3溶液;c.CH3COONa 溶液;d.NaHCO3溶液。pH由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为
(3)将0.2mol/L HCN溶液和0.1mol/L的NaOH溶液等体积混合后,溶液显碱性,则混合溶液中c(HCN)、c(H+)、c(OH-)、c(CN-)、c(Na+)浓度从大到小的排序为
c(HCN)+c(CN-)=
(4)写出NaHCO3溶液中的质子守恒式:
(5)相同条件下,取等体积等pH的:a.HCN溶液;b.CH3COOH溶液;c.H2CO3溶液。
各稀释100倍,稀释后的溶液,其pH从大到小的排序为
(6)25 ℃时,将体积为Va、pH=13的某一元强碱与体积为Vb、pH=2的某二元强酸混合,若所得溶液的pH=11,则Va:Vb=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】维持pH的稳定对生命体的生理活动、化学电源的高效工作等具有重要意义。
(1)若25℃时, 的醋酸与0.1mol/L的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的醋酸与0.1mol/L的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为___________ (用含a的代数式表示)。
(2)常温下,在不同试剂中加入酸或碱后体系pH的变化如表所示。
①
___________ (忽略加入NaOH前后体系的体积变化)。
②结合化学用语解释试剂ⅱ显酸性的原因:___________ 。
③试剂ⅱ中微粒浓度关系正确的有___________ (填序号)。
a.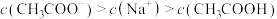
b.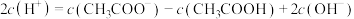
c.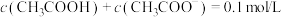
④由表中数据可知,试剂ⅱ的pH受一定量的酸和碱的影响不大。溶液的这种能对抗外来少量强酸、强碱或适当稀释,而保持溶液的pH几乎不变的作用称为缓冲作用。下列溶液具有缓冲作用的是_______ (填序号)。
a.NaCN—HCN b.H2SO4—NaHSO4 c.NH3·H2O—NH4Cl d.NaCl—HCl
(1)若25℃时,
 的醋酸与0.1mol/L的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的醋酸与0.1mol/L的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为(2)常温下,在不同试剂中加入酸或碱后体系pH的变化如表所示。
| 试剂 | pH | ||
| 初始 | 通入0.01molHCl气体 | 加入0.01molNaOH固体 | |
| ⅰ。1LH2O | 7 | 2 | a |
| ⅱ。0.10molCH3COOH、0.10molCH3COONa配制成1L的溶液 | 4.76 | 4.67 | 4.85 |

②结合化学用语解释试剂ⅱ显酸性的原因:
③试剂ⅱ中微粒浓度关系正确的有
a.
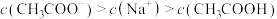
b.
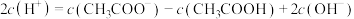
c.
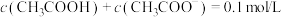
④由表中数据可知,试剂ⅱ的pH受一定量的酸和碱的影响不大。溶液的这种能对抗外来少量强酸、强碱或适当稀释,而保持溶液的pH几乎不变的作用称为缓冲作用。下列溶液具有缓冲作用的是
a.NaCN—HCN b.H2SO4—NaHSO4 c.NH3·H2O—NH4Cl d.NaCl—HCl
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3 -)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液
A.HCOONa B.NaCN C.Na2CO3,
其物质的量浓度由大到小的顺序是________ (填编号)。
③已知25℃时,HCOOH( aq) +OH -( aq)=HCOO-(aq) +H2O(1) △H=-a kJ/mol
H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol
甲酸电离的热化学方程式为__________________________________ 。
④将少量CO2通入NaCN溶液,反应的离子方程式是______________________ 。
⑤室温下,—定浓度的HCOONa溶液pH =9,用离子方程式表示溶液呈碱性的原因是:
______________________________ ,溶液中 =
=___________ 。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。
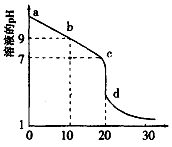
①d点所示的溶液中离子浓度由大到小的顺序依次为_______________ 。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=_____ (用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为____ 。
(3)已知Ksp(BaCO3) =2.6×l0-9,Ksp( BaSO4)=1.1×10-10.
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为____ mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中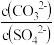 =
=___________ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka = 1.77×10 -4 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②常温下,pH相同的三种溶液
A.HCOONa B.NaCN C.Na2CO3,
其物质的量浓度由大到小的顺序是
③已知25℃时,HCOOH( aq) +OH -( aq)=HCOO-(aq) +H2O(1) △H=-a kJ/mol
H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol
甲酸电离的热化学方程式为
④将少量CO2通入NaCN溶液,反应的离子方程式是
⑤室温下,—定浓度的HCOONa溶液pH =9,用离子方程式表示溶液呈碱性的原因是:
 =
=(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。

①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为
(3)已知Ksp(BaCO3) =2.6×l0-9,Ksp( BaSO4)=1.1×10-10.
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
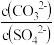 =
=
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】在常温下,下列五种溶液:①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4③0.1mol/L NH4HSO4④0.1mol/L NH3·H2O和 0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3·H2O请根据要求填写下列空白:
(1)溶液①呈_______ 性(填“酸”、“碱”或“中”),其原因是________________________ (用离子方程式表示)
(2)在上述五种溶液中,pH最小的是_______ ;c(NH4+)最小的是_______ ﹝填序号﹞
(3)比较溶液②、③中c(NH4+)的大小关系是②_______ ③﹝填“>”、“<”或“=”)
(4)在溶液④中NH3·H2O和_________ 离子的物质的量浓度之和为0.2 mol/L。
(1)溶液①呈
(2)在上述五种溶液中,pH最小的是
(3)比较溶液②、③中c(NH4+)的大小关系是②
(4)在溶液④中NH3·H2O和
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,草酸( )的
)的 ,
,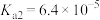 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:
(1)写出 的第二步电离方程式
的第二步电离方程式___________ 。
(2)相同浓度的 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是________ 溶液。用 的NaOH溶液滴定
的NaOH溶液滴定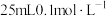 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
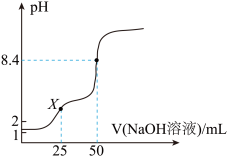
①X点溶液显___________ (填“酸性”“中性”或“碱性”),若向该溶液中滴加少量 ,反应的离子方程式为
,反应的离子方程式为___________ , 值
值___________ (填“增大”或“减小”)。
②滴定过程中所得混合溶液中 时,
时,
___________ 。
(3)反应 的平衡常数K的数量级为
的平衡常数K的数量级为___________ 。
 )的
)的 ,
,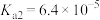 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:(1)写出
 的第二步电离方程式
的第二步电离方程式(2)相同浓度的
 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是 的NaOH溶液滴定
的NaOH溶液滴定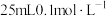 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
①X点溶液显
 ,反应的离子方程式为
,反应的离子方程式为 值
值②滴定过程中所得混合溶液中
 时,
时,
(3)反应
 的平衡常数K的数量级为
的平衡常数K的数量级为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知25℃时部分弱电解质的电离平衡常数如表所示,请回答下列有关问题:
(1)25℃时,NaHC2O4溶液显_______ 性(填“酸”“中”或“碱”),原因是_______ 。
(2)25℃时,若向氨水中加入少量硫酸铵固体,下列表达式的数据变小的是_______。
(3)常温下,体积均为10 ml、pH=2的盐酸溶液与醋酸溶液分别加蒸馏水稀释a倍和b倍到pH=4,a_______ b(填“>”“<”或“=”)。
(4)请写出在次氯酸钠溶液中通入少量二氧化碳气体的离子方程式:_______ 。
(5)常温下,将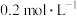 HCN溶液和
HCN溶液和 的NaOH溶液等体积混合后,此时溶液显
的NaOH溶液等体积混合后,此时溶液显_______ 性(填“酸”“中”或“碱”),该溶液中的质子守恒关系式为:_______ 。
| 化学式 | CH3COOH | H2C2O4 | HCN | HClO | H2CO3 |  |
 |  |  |  |  | 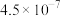 |  |
 | —— | 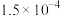 | —— | —— | 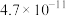 | —— |
(2)25℃时,若向氨水中加入少量硫酸铵固体,下列表达式的数据变小的是_______。
A. | B. | C. | D. |
(4)请写出在次氯酸钠溶液中通入少量二氧化碳气体的离子方程式:
(5)常温下,将
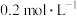 HCN溶液和
HCN溶液和 的NaOH溶液等体积混合后,此时溶液显
的NaOH溶液等体积混合后,此时溶液显
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性。向10mL 0.01mol·L-1的H2C2O4溶液滴加0.01mol·L-1KOH溶液V(mL),回答下列问题。
(1)当V<10mL时,反应的离子方程式为___ 。
(2)当V=10mL时,溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为___ 。
(3)当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+(HC2O4-);当V=b mL时,溶液中离子浓度有如下关系:c(K+)= c(C2O42-)+c(HC2O4-)+c(H2C2O4);则a___ b(填“<”“=”或“>”)。
(4)当V=20mL时,再滴入NaOH溶液,则溶液中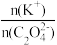 的值将
的值将___ (填“变大”“变小”或“不变”)。
(1)当V<10mL时,反应的离子方程式为
(2)当V=10mL时,溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为
(3)当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+(HC2O4-);当V=b mL时,溶液中离子浓度有如下关系:c(K+)= c(C2O42-)+c(HC2O4-)+c(H2C2O4);则a
(4)当V=20mL时,再滴入NaOH溶液,则溶液中
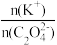 的值将
的值将
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室(室温下)存放着如下几种试剂:
①0.1mol/LCH3COOH溶液②0.1mol/LCH3COONa溶液③0.1mol/LNaOH溶液④0.1mol/L盐酸⑤0.1mol/L氨水⑥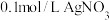 溶液⑦
溶液⑦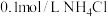 溶液⑧
溶液⑧ 溶液
溶液
回答下列问题:
(1)溶液的 ,且促进水的电离的试剂是
,且促进水的电离的试剂是___________ (填序号,下同)。
(2)试剂①、④、⑥中由水电离的氢离子浓度 由大到小的顺序是
由大到小的顺序是___________ 。
(3)试剂⑤、⑦、⑧溶液中 由大到小的顺序是
由大到小的顺序是___________ 。
(4)将试剂⑤和试剂⑦等体积混合后测得混合溶液显碱性,则混合溶液中离子浓度由大到小的顺序是___________ 。试剂⑦中某离子M的浓度为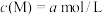 ,将试剂④和试剂⑦等体积混合后测得
,将试剂④和试剂⑦等体积混合后测得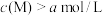 ,则该离子M是
,则该离子M是___________ (填序号)。
A. B.
B. C.
C. D.
D.
(5)试剂⑧中电荷守恒的表达式是___________ 。
(6)已知醋酸的电离常数 ,将试剂①和试剂②等体积混合后,
,将试剂①和试剂②等体积混合后, 的水解常数
的水解常数
___________ 。已知亚硫酸的电离常数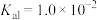 ,
,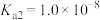 。向
。向 溶液中加入过量试剂①发生反应的离子方程式是
溶液中加入过量试剂①发生反应的离子方程式是___________ 。
①0.1mol/LCH3COOH溶液②0.1mol/LCH3COONa溶液③0.1mol/LNaOH溶液④0.1mol/L盐酸⑤0.1mol/L氨水⑥
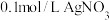 溶液⑦
溶液⑦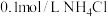 溶液⑧
溶液⑧ 溶液
溶液回答下列问题:
(1)溶液的
 ,且促进水的电离的试剂是
,且促进水的电离的试剂是(2)试剂①、④、⑥中由水电离的氢离子浓度
 由大到小的顺序是
由大到小的顺序是(3)试剂⑤、⑦、⑧溶液中
 由大到小的顺序是
由大到小的顺序是(4)将试剂⑤和试剂⑦等体积混合后测得混合溶液显碱性,则混合溶液中离子浓度由大到小的顺序是
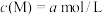 ,将试剂④和试剂⑦等体积混合后测得
,将试剂④和试剂⑦等体积混合后测得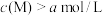 ,则该离子M是
,则该离子M是A.
 B.
B. C.
C. D.
D.
(5)试剂⑧中电荷守恒的表达式是
(6)已知醋酸的电离常数
 ,将试剂①和试剂②等体积混合后,
,将试剂①和试剂②等体积混合后, 的水解常数
的水解常数
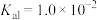 ,
,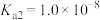 。向
。向 溶液中加入过量试剂①发生反应的离子方程式是
溶液中加入过量试剂①发生反应的离子方程式是
您最近半年使用:0次

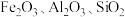 )出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁:
)出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁: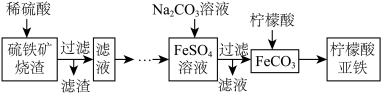
 (开始沉淀的
(开始沉淀的 计算)
计算)




