汽车尾气主要含有二氧化碳、一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一。请回答下列问题。
(1)汽车尾气中的一氧化碳来自_____ ,一氧化氮来自_____ 。汽车尾气对环境的危害主要有_____ (至少填两种)。
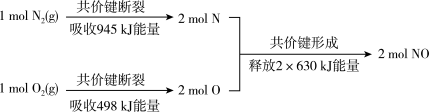
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应_____ (填“释放”或“吸收”)____ kJ能量。
(1)汽车尾气中的一氧化碳来自
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应

更新时间:2022-11-26 13:51:40
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应中的能量变化是人类获取能量的重要途径。
(1)液化气是一种重要的家庭燃料,下列示意图与液化气在燃烧过程中的能量变化最相符的是___
A.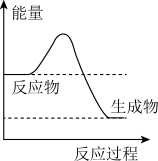 B.
B.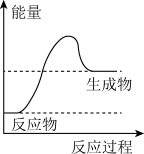 C.
C.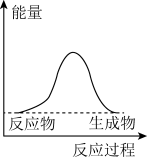
(2)人们普遍使用的干电池工作时是将化学能转化为___ 。
(3)已知拆开1molH2中的化学键要吸收436kJ的能量,拆开1molO2中的化学键要吸收496kJ的能量,形成水分子中的1molH—O键要放出463 kJ的能量,试计算2H2+O2=2H2O反应中的ΔH=___ kJ·mol-1。
(4)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
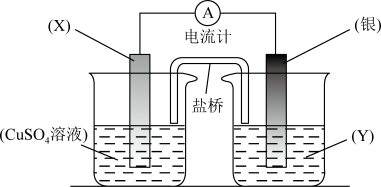
①电极X的材料是___ ;电解质溶液Y是___ ;
②银电极为电池的___ 极,发生的电极反应为___ ;X电极上发生的电极反应为___ ;
③如果闭合电路前X电极与银电极质量相等,当电路中通过0.1mol电子时,两电极质量差为___ g。(原子量Cu:64;Ag:108)
(1)液化气是一种重要的家庭燃料,下列示意图与液化气在燃烧过程中的能量变化最相符的是
A.
 B.
B. C.
C.
(2)人们普遍使用的干电池工作时是将化学能转化为
(3)已知拆开1molH2中的化学键要吸收436kJ的能量,拆开1molO2中的化学键要吸收496kJ的能量,形成水分子中的1molH—O键要放出463 kJ的能量,试计算2H2+O2=2H2O反应中的ΔH=
(4)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

①电极X的材料是
②银电极为电池的
③如果闭合电路前X电极与银电极质量相等,当电路中通过0.1mol电子时,两电极质量差为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。白磷和 的分子结构如图所示,现提供以下化学键的键能(
的分子结构如图所示,现提供以下化学键的键能( ):P—O:360 O=O:498,已知反应:
):P—O:360 O=O:498,已知反应: (白磷)
(白磷)
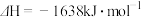 ,则P—P的键能为:
,则P—P的键能为:__________ 。
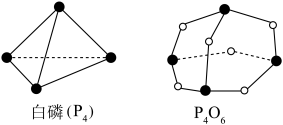
(2)工业合成氨的反应为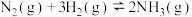 。设在容积为2.0L的密闭容器中充入等物质量的
。设在容积为2.0L的密闭容器中充入等物质量的 和
和 ,反应在一定条件下达到平衡时,
,反应在一定条件下达到平衡时, 的物质的量分数为
的物质的量分数为 。计算:该条件下
。计算:该条件下 的平衡转化率
的平衡转化率__________ 。
 的分子结构如图所示,现提供以下化学键的键能(
的分子结构如图所示,现提供以下化学键的键能( ):P—O:360 O=O:498,已知反应:
):P—O:360 O=O:498,已知反应: (白磷)
(白磷)
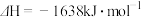 ,则P—P的键能为:
,则P—P的键能为:
(2)工业合成氨的反应为
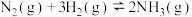 。设在容积为2.0L的密闭容器中充入等物质量的
。设在容积为2.0L的密闭容器中充入等物质量的 和
和 ,反应在一定条件下达到平衡时,
,反应在一定条件下达到平衡时, 的物质的量分数为
的物质的量分数为 。计算:该条件下
。计算:该条件下 的平衡转化率
的平衡转化率
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据要求写出下列反应的热化学方程式
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量______________________ .
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)_____________________ .

(3)某反应的平衡常数 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式_______________ .
(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为____________________ .
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)

(3)某反应的平衡常数
 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
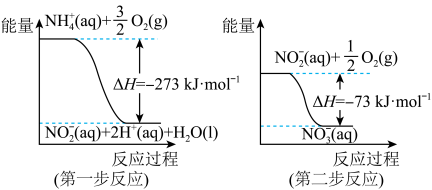
(1)第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
(2)1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为___________ 。
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=___________ (用ΔH1、ΔH3、ΔH4表示) 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
(1)第一步反应是
(2)1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=
您最近一年使用:0次
【推荐2】CO2的减排、捕集和利用是人类可持续发展的重要战略之一。利用CO2和H2生成CH3OH来捕集CO2的反应是CO2(g)+3H2(g) CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
(1)下列有关上述反应的图象合理的是__________ (填标号)。
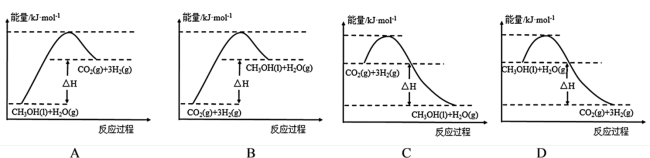
(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量__________ (填“>”“<”或“=”)8.9 kJ。
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为________ ,转移的电子数为________ NA。
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为__________ %,氢气的体积分数ω(H2)=__________ %。
 CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:(1)下列有关上述反应的图象合理的是

(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】天然气的主要成分为 ,一般还含有
,一般还含有 、
、 等烃类,是重要的燃料和化工原料。
等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:
 ,相关物质的摩尔燃烧焓数据如表所示:
,相关物质的摩尔燃烧焓数据如表所示:
则
_____ 
(2)甲烷是常见的燃料, 加氢可制备甲烷,其反应为
加氢可制备甲烷,其反应为
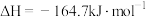 。
。
①
_____ 。
②对于 加氢制备甲烷的反应,有关说法错误的是
加氢制备甲烷的反应,有关说法错误的是_____ 。
A.该反应理论上可以设计成原电池
B.该反应过程中有旧键断裂吸收的能量大于新键形成释放的能量
C.反应结束,体系中物质的总能量降低
D.此反应可以变废为宝,有利于碳中和和碳达峰的实现
③已知:标准摩尔生成焓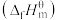 是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
则
_____ 。
(3)丙烷燃烧可以通过以下两种途径:
途径I:
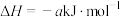
途径Ⅱ: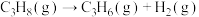
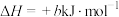

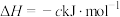

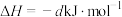 (a、b、c、d均为正值)
(a、b、c、d均为正值)
按途径Ⅱ反应,常温下,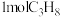 完全燃烧时放出的热量为
完全燃烧时放出的热量为_____ kJ(用含b、c、d的代数式表示);相同条件下,等量的丙烷通过两种途径完全燃烧时,途径I放出的热量_____ (填“大于”、“小于”或“等于”)途径Ⅱ放出的热量。
 ,一般还含有
,一般还含有 、
、 等烃类,是重要的燃料和化工原料。
等烃类,是重要的燃料和化工原料。(1)乙烷在一定条件可发生如下反应:

 ,相关物质的摩尔燃烧焓数据如表所示:
,相关物质的摩尔燃烧焓数据如表所示:| 物质 | 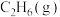 |  |  |
摩尔燃烧焓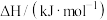 | -1560 | -1411 | -286 |


(2)甲烷是常见的燃料,
 加氢可制备甲烷,其反应为
加氢可制备甲烷,其反应为
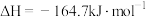 。
。| 物质 |  |  |  |  |
| 键能:1mol化学键断裂时需要吸收的能量/kJ | 436 | 465 | 413 | a |

②对于
 加氢制备甲烷的反应,有关说法错误的是
加氢制备甲烷的反应,有关说法错误的是A.该反应理论上可以设计成原电池
B.该反应过程中有旧键断裂吸收的能量大于新键形成释放的能量
C.反应结束,体系中物质的总能量降低
D.此反应可以变废为宝,有利于碳中和和碳达峰的实现
③已知:标准摩尔生成焓
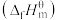 是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:| 物质 |  |  |  |  |
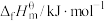 | -393.5 | -241.5 | x | 0 |

(3)丙烷燃烧可以通过以下两种途径:
途径I:

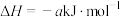
途径Ⅱ:
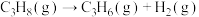
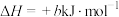

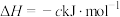

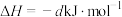 (a、b、c、d均为正值)
(a、b、c、d均为正值)按途径Ⅱ反应,常温下,
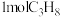 完全燃烧时放出的热量为
完全燃烧时放出的热量为
您最近一年使用:0次
【推荐1】(1)反应2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中,氧化产物是___________ ,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ Cl2(填>、<或=)。
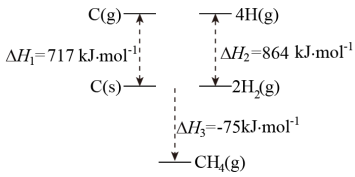
(2)根据下图中的能量关系,可求得C-H键的键能___________ kJ/mol。
(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:___________ 。
(2)根据下图中的能量关系,可求得C-H键的键能

(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:
您最近一年使用:0次
【推荐2】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与化学键形成时放出的能量不同引起的,如图是N2和O2反应生成NO过程中的能量变化

请回答下列有关问题:
(1)反应物断键吸收的总能量为___________ 。
(2)生成物成键放出的总能量为___________ 。
(3)判断反应N2+O2=2NO是___________ (填“吸收”或“放出”)能量。
(4)反应物的总能量___________ (填“>”,“=”或“<”)生成物的总能量。

请回答下列有关问题:
(1)反应物断键吸收的总能量为
(2)生成物成键放出的总能量为
(3)判断反应N2+O2=2NO是
(4)反应物的总能量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g) 2C1NO(g),
2C1NO(g),
(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):
则2NO(g)+C12(g) 2C1NO(g)反应的△H和a的关系为△H=
2C1NO(g)反应的△H和a的关系为△H=____ kJ/mol。
(2)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:
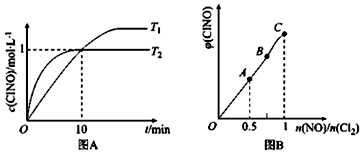
① 由图A可判断T1____ T2,该反应的△H____ 0 (填“>”“<”或“=”)。
② 反应开始到10min时NO的平均反应速率v(NO)=______ mol/(L·min)。
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是________ 点。
 2C1NO(g),
2C1NO(g),(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):
| 化学键 | N≡O | Cl-Cl | Cl-N | N=O |
| 键能(kJ/mol) | 630 | 243 | a | 607 |
 2C1NO(g)反应的△H和a的关系为△H=
2C1NO(g)反应的△H和a的关系为△H=(2)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:

① 由图A可判断T1
② 反应开始到10min时NO的平均反应速率v(NO)=
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是
您最近一年使用:0次




