钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)K和 属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属
属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属 低,试解释原因。
低,试解释原因。_____
(2) 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为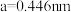 ,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有_____ 个?试说明分析思路。_____
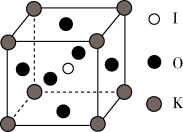
(3)计算K与O间的最短距离_____ 。
(1)K和
 属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属
属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属 低,试解释原因。
低,试解释原因。(2)
 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为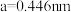 ,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
(3)计算K与O间的最短距离
更新时间:2022-11-28 15:42:33
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y电子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)XZ2与YZ2分子的立体构型分别是_______ 和_______ ,中心原子的杂化方式分别为_______ 和_______
(2)写出YZ2分子的电子式_______ ,YZ2晶体中,属于一个晶胞的分子_______ 个。
(3)Q的元素符号是_______ ,它的基态原子的核外电子排布式为_______ ,在形成化合物时它的最高化合价为_______ 。
(4)E的氢化物溶液中存在的所有氢键共_______ 种。
(1)XZ2与YZ2分子的立体构型分别是
(2)写出YZ2分子的电子式
(3)Q的元素符号是
(4)E的氢化物溶液中存在的所有氢键共
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】C、N、Si、Ni等元素在新型材料的研制中有着重要应用,请回答下列问题:
(1)Ni元素的价层电子排布式为______ ,C、N、Si的第一电离能由大到小的顺序为______ 。
(2)研究发现, 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为______ ; 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是______ 。
(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为______ 。已知石墨的密度为 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为______ cm。

(1)Ni元素的价层电子排布式为
(2)研究发现,
 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为
 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型的非金属元素到典型的金属元素的过渡。回答下列问题:
(1)①基态N原子含有___________ 种不同能量的电子。
② 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为___________ (填化学式,下同),微粒的空间结构相同的为___________ 和___________ ;键角:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
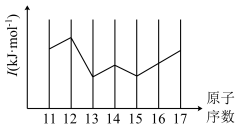
(2)第三周期主族元素某一级电离能如图所示,该电离能是第___________ (填“一”“二”或“三”)电离能,其中P的该级电离能比Si小的原因为___________ 。
(3) 和
和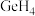 的沸点如下表:
的沸点如下表:
 的沸点比
的沸点比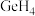 的沸点高的主要原因为
的沸点高的主要原因为___________ 。
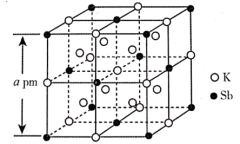
(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为___________ 。若该合金的密度为 ,该合金的摩尔质量为
,该合金的摩尔质量为___________  (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
(1)①基态N原子含有
②
 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)第三周期主族元素某一级电离能如图所示,该电离能是第

(3)
 和
和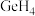 的沸点如下表:
的沸点如下表:| 物质 |  | 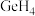 |
| 沸点 | -62℃ | -90℃ |
 的沸点比
的沸点比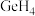 的沸点高的主要原因为
的沸点高的主要原因为(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为
 ,该合金的摩尔质量为
,该合金的摩尔质量为 (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】原子序数小于等于36的Q、W、X、Y、Z五种元素,它们的原子序数依次增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含未成对电子数均为2,Z的基态原子核外电子有26种运动状态。回答下列问题(涉及元素时用对应的元素符号表示):
(1)Z的基态原子的电子排布式___________ ;从结构角度来看,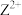 易被氧化成
易被氧化成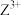 的原因是
的原因是___________ 。
(2)化合物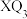 的沸点比化合物
的沸点比化合物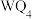 的高,其主要原因是
的高,其主要原因是___________ 。
(3)1molQWX与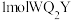 所含
所含 键数目之比为
键数目之比为___________ 。
(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为___________ 。
②预测该化合物熔点应___________ (填“高于”或“低于”)金刚石,理由是___________ 。
(5)写出少量Z单质和X的最高价氧化物的水化物的稀溶液反应的离子方程式:___________ 。
(1)Z的基态原子的电子排布式
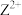 易被氧化成
易被氧化成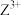 的原因是
的原因是(2)化合物
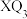 的沸点比化合物
的沸点比化合物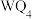 的高,其主要原因是
的高,其主要原因是(3)1molQWX与
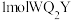 所含
所含 键数目之比为
键数目之比为(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为
②预测该化合物熔点应
(5)写出少量Z单质和X的最高价氧化物的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】镓(Ga)是一种重要的金属,镓的化合物广泛应用于半导体、太阳能、液态合金、医疗化工等诸多领域,被称为电子工业的“脊梁”。
(1)基态Ga原子的价层电子的轨道表示式是___________________ 。
(2) 在270°C左右以二聚体
在270°C左右以二聚体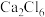 存在,结构式如图。
存在,结构式如图。
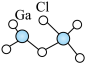
① 可以形成二聚体的原因是
可以形成二聚体的原因是__________________________ 。
② 和
和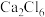 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是_________________ 。
③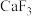 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,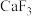 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因_____ 。
(3) 可与
可与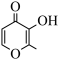 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是______________ ,甲基麦芽酚中,与 形成配位键的原子是
形成配位键的原子是________ 。
(1)基态Ga原子的价层电子的轨道表示式是
(2)
 在270°C左右以二聚体
在270°C左右以二聚体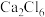 存在,结构式如图。
存在,结构式如图。
①
 可以形成二聚体的原因是
可以形成二聚体的原因是②
 和
和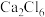 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是③
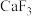 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,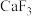 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因(3)
 可与
可与 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是 形成配位键的原子是
形成配位键的原子是
您最近一年使用:0次



