红蓝宝石、祖母绿、金绿猫眼、钻石为举世公认的珍贵宝石。
(1)红宝石是刚玉的一种,主要成分为氧化铝( ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为_______ 。
(2)祖母绿主要成分的化学式为 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)_______ I(Al)。Be能与NaOH溶液反应,请简单说明判断依据:_______ 。
(3)金绿猫眼主要成分的化学式为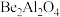 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为_______ 。 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:_______ 。
(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为_______ 。金刚石晶胞结构如图所示,与晶胞面心处碳原子距离最近且等距离的碳原子数为_______ 。

(1)红宝石是刚玉的一种,主要成分为氧化铝(
 ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为(2)祖母绿主要成分的化学式为
 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)(3)金绿猫眼主要成分的化学式为
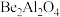 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为

22-23高三上·浙江·阶段练习 查看更多[2]
更新时间:2022-12-07 10:22:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】结合元素周期表回答下列问题:
(1)周期表中所列元素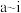 ,属于短周期元素的有
,属于短周期元素的有___________ 种,属于主族元素的有___________ 种;族序数等于周期数的元素有___________ 种;f元素原子结构示意图为___________ ;h元素的元素名称为___________ ;i元素位于第___________ 周期第___________ 族。
(2)f2-原子核内有x个中子,其质量数为m,则n g f 2-所含电子的物质的量为___________ mol。
(3)写出e的最高价氧化物以及该氧化物对应的水化物分别与c的最高价氧化物对应的水化物反应的离子方程式:___________ ;___________ 。
(4)C久置于空气中,最终变成产物是___________ 。
| a | |||||||||||||||||
| b | |||||||||||||||||
| c | d | e | f | g | |||||||||||||
| h | i | ||||||||||||||||
(1)周期表中所列元素
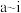 ,属于短周期元素的有
,属于短周期元素的有(2)f2-原子核内有x个中子,其质量数为m,则n g f 2-所含电子的物质的量为
(3)写出e的最高价氧化物以及该氧化物对应的水化物分别与c的最高价氧化物对应的水化物反应的离子方程式:
(4)C久置于空气中,最终变成产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】锌是一种过渡金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置:第________ 周期,第________ 族,________ 区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式__________________ ;葡萄糖分子中碳原子的杂化方式为______________ 。
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于________________ (填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,NH3位于正四面体的顶点,则[Zn(NH3)4]2+中中心离子的杂化轨道类型是_____________ 。

(4)上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为___________________ ;该化合物晶体的熔点比干冰高得多,原因是______________________________________________ 。
(5)与锌同周期,最外层有3个未成对电子的元素名称是________________ ,该元素最高价氧化物对应水化物的酸性比溴的最高价氧化物对应水化物的酸性___________ (填“强”或“弱”)。
(1)指出锌在周期表中的位置:第
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于

(4)上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为
(5)与锌同周期,最外层有3个未成对电子的元素名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】含氟化合物被用于预防龋齿、饮水加氟及其他口腔卫生产品中。起初是用氟化钠(NaF)来为饮用水加氟,但后来逐渐被氟硅酸(H2SiF6)及其盐氟硅酸钠(Na2SiF6)代替。完成下列填空:
(1)写出F原子的电子排布式_____________ ,F原子有_______ 种能量不同的电子。
(2)和硅元素位于同主族的另外一个短周期元素的最高氧化物的结构简式是__________ ,其熔点_____ SiO2(填“高于”或“低于”)。
(3)F的非金属性比Cl强,①请用一个事实来证明:________________________________ 。
②并从原子结构角度进行解释:______________ 。
(1)写出F原子的电子排布式
(2)和硅元素位于同主族的另外一个短周期元素的最高氧化物的结构简式是
(3)F的非金属性比Cl强,①请用一个事实来证明:
②并从原子结构角度进行解释:
您最近一年使用:0次
填空题
|
适中
(0.65)
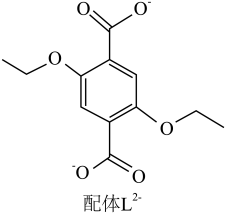
【推荐1】配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn4O]6+构成。
(1)基态Zn2+的电子排布式为______ 。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为______ 形;每个L2-中采取sp2杂化的C原子数目为______ 个,C与O之间形成σ键的数目为______ 个。

(1)基态Zn2+的电子排布式为
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为
您最近一年使用:0次
【推荐2】回答下列问题
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是________ ,基态Mo原子核外有________ 种不同运动状态的电子,其中核外电子占据最高电子层的符号是________ 。
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知: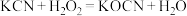 ,回答下列问题:
,回答下列问题:
 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为________ (用元素符号表示,下同),电负性从大到小的顺序为________ ,基态氮原子外围电子排布式为________ 。
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知:
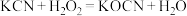 ,回答下列问题:
,回答下列问题: 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_______ 。
⑵已知反应:
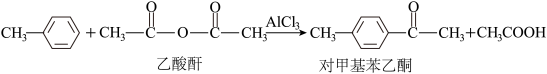
①乙酸酐分子中碳原子轨道的杂化类型为______ 。
②1 mol对甲基苯乙酮分子中含有的σ键的数目为_____ 。
③甲苯分子难溶于水的原因是______ 。
④单个AlCl3气态分子的空间构型为______ ,AlCl3可与Cl-形成AlCl ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为______ 。
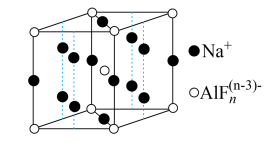
(3)某遮光剂的晶胞如右图所示,则n=______ 。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为
⑵已知反应:

①乙酸酐分子中碳原子轨道的杂化类型为
②1 mol对甲基苯乙酮分子中含有的σ键的数目为
③甲苯分子难溶于水的原因是
④单个AlCl3气态分子的空间构型为
 ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为(3)某遮光剂的晶胞如右图所示,则n=

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NH3在工农业生产中具有重要的作用,可以用来生产尿素(结构简式为: )等化学肥料,也可以用来制备一些配位化合物。
)等化学肥料,也可以用来制备一些配位化合物。
(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子的电子排布式:_______ 。
(2)工业上生产尿素的化学反应: ,则CO(NH2)2分子中C原子的杂化方式为
,则CO(NH2)2分子中C原子的杂化方式为_______ 。C、N、O三种元素的第一电离能由小到大的顺序为_______ 。
(3)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的 晶体,与该物质中的配体互为等电子体的阴离子的化学式为
晶体,与该物质中的配体互为等电子体的阴离子的化学式为_______ 。
(4)写出将过量氨水缓慢滴入硫酸铜溶液中发生反应的离子方程式:_______ 、_______ 。
 )等化学肥料,也可以用来制备一些配位化合物。
)等化学肥料,也可以用来制备一些配位化合物。(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子的电子排布式:
(2)工业上生产尿素的化学反应:
 ,则CO(NH2)2分子中C原子的杂化方式为
,则CO(NH2)2分子中C原子的杂化方式为(3)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的
 晶体,与该物质中的配体互为等电子体的阴离子的化学式为
晶体,与该物质中的配体互为等电子体的阴离子的化学式为(4)写出将过量氨水缓慢滴入硫酸铜溶液中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)某元素原子的价电子构型为4s24p1,该元素的符号为________ 。
(2)某元素+3价离子的3d轨道半充满,该元素的符号为________ 。
(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A的离子结构示意图为________ ,B的元素名称为________ 。
(4)如图,第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。
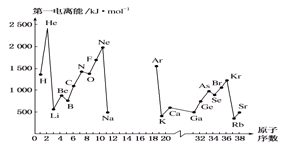
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为________ <Al<________ ;(填元素符号)。
②图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族。
(2)某元素+3价离子的3d轨道半充满,该元素的符号为
(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A的离子结构示意图为
(4)如图,第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中第一电离能最小的元素在周期表中的位置是第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据要求填空
(1)选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤CaBr2 ⑥NaH ⑦ K3C60 ⑧石墨 ⑨氯化铵 ⑩铜晶体 熔化时不破坏化学键的有_______ ;含有非极性共价键的有_______ 。
(2)性质比较:(填“>”、“=”或“<”,下同)
①第一电离能Mg_______ Al,解释原因_______
②酸性强弱HClO4_______ HClO3,解释原因_______
(3)下图为几种晶体或晶胞的示意图(用名称填写)
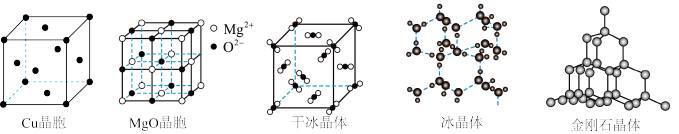
①上述晶体中,粒子之间以共价键结合形成的晶体是_______ 。
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为_______ 。
(1)选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤CaBr2 ⑥NaH ⑦ K3C60 ⑧石墨 ⑨氯化铵 ⑩铜晶体 熔化时不破坏化学键的有
(2)性质比较:(填“>”、“=”或“<”,下同)
①第一电离能Mg
②酸性强弱HClO4
(3)下图为几种晶体或晶胞的示意图(用名称填写)

①上述晶体中,粒子之间以共价键结合形成的晶体是
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为
您最近一年使用:0次



