浙江省强基联盟2022-2023学年高三上学期12月联考化学试题
浙江
高三
阶段练习
2022-12-09
683次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、物质结构与性质、常见无机物及其应用、化学实验基础、认识化学科学
浙江省强基联盟2022-2023学年高三上学期12月联考化学试题
浙江
高三
阶段练习
2022-12-09
683次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、物质结构与性质、常见无机物及其应用、化学实验基础、认识化学科学
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 疫情的防控离不开化学知识,新型冠状病毒肺炎疫情终将过去。下列说法正确的是
| A.漂白粉、75%酒精都是利用强氧化性杀灭细菌和病毒的 |
| B.制作口罩的无纺布(聚酯纤维)是加聚产物 |
| C.制作口罩的熔喷布(聚丙烯)可在自然界被微生物降解 |
| D.制作口罩鼻梁定型条的铁丝通常根据电化学原理镀锌防锈 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 下列表示正确的是
A. 分子的VSEPR模型: 分子的VSEPR模型: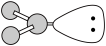 |
B.氨分子的球棍模型: |
C.双氧水分子的电子式: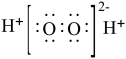 |
D.基态硼原子的轨道表示式: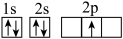 |
您最近一年使用:0次
单选题
|
较易(0.85)
3. 下列说法不正确的是
| A.氯气可杀灭细菌、病毒,常用于室内空气消毒 |
| B.硫酸铁、氯化铝常用作污水处理的混凝剂 |
| C.亚硝酸钠可用作肉制品的防腐剂和护色剂 |
D.工业生产中用 还原 还原 制备高纯硅 制备高纯硅 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
4. 下列说法正确的是
| A.煤的主要成分为焦炭,此外还含有一些有机化合物 |
| B.护肤品和医用软膏中的“凡士林”的主要成分是烷烃 |
| C.汽油、煤油是石油的裂解产品,属于不可再生能源 |
| D.天然气、煤气、煤层气和沼气的主要成分都是甲烷 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 下列说法不正确的是
| A.麦芽糖、乳糖和蔗糖都属于寡糖 |
| B.1mol丙氨酸钠可与2molHCl反应 |
| C.核酸、蛋白质和超分子都属于高分子化合物 |
| D.食品工业常使用有机溶剂来提取植物种子里的油 |
【知识点】 淀粉和纤维素组成与结构 淀粉、纤维素的水解
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 下列选用的仪器和药品能达到实验目的的是
| A | B | C | D |
 | 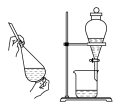 |  | 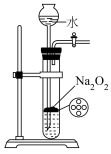 |
| 实验室制备少量氨气 | 用酒精萃取水中的溴 | 吸收尾气中的 | 制备少量氧气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 与 与 的混合物中O原子数为 的混合物中O原子数为 |
B.pH=14的 溶液中 溶液中 离子数为 离子数为 |
C.100g36.5%盐酸中HCl分子数为 |
D.4.48L乙烯中σ键数目为 |
【知识点】 阿伏加德罗常数的应用解读 结合气体物质与NA相关推算解读
您最近一年使用:0次
单选题
|
适中(0.65)
8. 误食白磷中毒,曾通过口服 溶液解毒:
溶液解毒: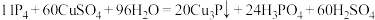 。关于该反应的下列说法不正确的是
。关于该反应的下列说法不正确的是
 溶液解毒:
溶液解毒: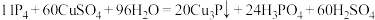 。关于该反应的下列说法不正确的是
。关于该反应的下列说法不正确的是A.不可服用浓 溶液 溶液 |
B. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
C.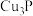 中Cu元素化合价为+1 中Cu元素化合价为+1 |
D.生成6mol 时,被 时,被 氧化的 氧化的 为0.6mol 为0.6mol |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 下列判断不正确的是
A.键角: |
| B.电负性:Li>Na |
C.电离常数: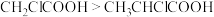 |
| D.水中溶解度:邻羟基苯甲酸>对羟基苯甲酸 |
【知识点】 电负性概念解读 键能、键长、键角及应用解读 氢键对物质性质的影响解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下列有关物质性质说法不正确的是
A. 与水反应生成两种强酸 与水反应生成两种强酸 |
B. 可通过干燥的 可通过干燥的 与 与 在催化剂作用下反应得到 在催化剂作用下反应得到 |
C. 可用作由 可用作由 制取无水 制取无水 的脱水剂 的脱水剂 |
D. 与足量 与足量 作用可得到 作用可得到 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
11. 能正确表示下列反应的离子方程式是
A.石灰乳吸收废气中的二氧化氮: |
B.亚硫酸氢钠溶液中滴加少量碘酸钾溶液: |
C.氧化银( )溶于浓氨水: )溶于浓氨水: |
D.乙二酸使酸性高锰酸钾溶液褪色: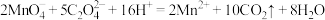 |
您最近一年使用:0次
单选题
|
适中(0.65)
12. 关于2-(3-氯-2-羟基)异吲哚啉-1,3-二酮,下列说法不正确的是


| A.分子中有1个手性碳原子 |
| B.苯环上的一氯代物有4种 |
| C.1mol该物质可消耗3molNaOH |
D.能使酸性 稀溶液褪色 稀溶液褪色 |
【知识点】 分子的手性解读 多官能团有机物的结构与性质解读
您最近一年使用:0次
单选题
|
适中(0.65)
13. X、Y、Z、W、Q五种短周期主族元素,原子序数依次增大。Z的核电荷数等于X、Y原子核外电子数之和,W与X同主族且其核外电子空间运动状态有6种,Y元素的最高价氧化物对应水化物能与其氢化物水溶液发生反应,YX3气体分子的Y原子采用sp3杂化,Q是同周期主族元素中原子半径最小的元素。下列说法正确的是
| A.X与Y不能形成具有18电子的分子 |
| B.简单离子的半径大小:Q>Z>W |
| C.最高价氧化物对应水化物的酸性:Y>Q |
D.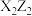 和 和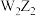 中含有的化学键类型相同 中含有的化学键类型相同 |
您最近一年使用:0次
2022-12-07更新
|
346次组卷
|
4卷引用:浙江省强基联盟2022-2023学年高三上学期12月联考化学试题
浙江省强基联盟2022-2023学年高三上学期12月联考化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题6-10)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(选择题6-10)浙江省杭州市富阳区场口中学2023-2024学年高二下学期3月月考化学试题
单选题
|
较难(0.4)
解题方法
14. 下列说法正确的是
A.室温下,将pH=a的HCl溶液加水稀释 倍,所得溶液的pH=a+b 倍,所得溶液的pH=a+b |
B.NaOH溶液滴定醋酸溶液时,离子浓度大小关系可能为 |
| C.生成盐的弱酸酸性越弱,盐的水解程度越大,所以醋酸钠溶液的pH不可能大于碳酸钠溶液 |
D.室温下,醋酸溶液稀释过程中,电离度逐渐增大, 逐渐增大 逐渐增大 |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
15. 某温度下,将A和B各0.15mol充入10L恒容密闭容器中,发生反应
 ,反应过程中,B的物质的量n(B)随时间t的变化如图所示。下列说法正确的是
,反应过程中,B的物质的量n(B)随时间t的变化如图所示。下列说法正确的是


 ,反应过程中,B的物质的量n(B)随时间t的变化如图所示。下列说法正确的是
,反应过程中,B的物质的量n(B)随时间t的变化如图所示。下列说法正确的是
| A.当v(A)=v(X)时,反应达到平衡 |
B.前2min的平均速率 |
| C.9min时,改变的反应条件为降温或加催化剂 |
D.若起始充入A和B各0.30mol,平衡时 |
【知识点】 化学平衡图像分析
您最近一年使用:0次
单选题
|
较易(0.85)
16. 航天员呼吸产生的 通过反应
通过反应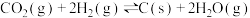
 ,再电解水可实现
,再电解水可实现 的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准摩尔生成焓(
的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准摩尔生成焓(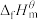 ),最稳定单质的标准生成焓规定为0.已知上述反应式中:
),最稳定单质的标准生成焓规定为0.已知上述反应式中: ;
; ;
;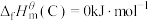 ;
; 。则
。则 的数值为
的数值为
 通过反应
通过反应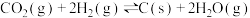
 ,再电解水可实现
,再电解水可实现 的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准摩尔生成焓(
的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准摩尔生成焓(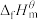 ),最稳定单质的标准生成焓规定为0.已知上述反应式中:
),最稳定单质的标准生成焓规定为0.已知上述反应式中: ;
; ;
; ;
; 。则
。则 的数值为
的数值为A.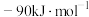 | B.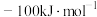 | C.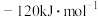 | D.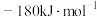 |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
17. 利用如图所示装置可以将非氧化还原反应设计成原电池——浓差电池。两侧半电池中的特定物质存在浓度差,导致半电池上发生的氧化还原反应程度不同,从而产生电势差。下列说法正确的是


| 编号 | 电极A | 电解质A | 电解质B | 电极B |
| ① | 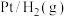 | 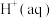 | 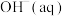 | 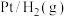 |
| ② | 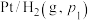 |  |  | 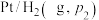 |
| ③ | 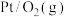 | 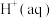 | 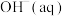 | 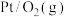 |
A.①号电池中,电极B上产生 |
| B.①号电池中,电解质A中阳离子通过盐桥流入电解质B |
C.②号电池中,若氢气压强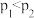 ,则A为负极 ,则A为负极 |
D.③号电池中,电池总反应为 ,电极B为负极 ,电极B为负极 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
18. 常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图像如图所示(
溶液,所得的沉淀溶解平衡图像如图所示(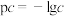 ,不考虑离子的水解)。下列叙述正确的是
,不考虑离子的水解)。下列叙述正确的是

 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图像如图所示(
溶液,所得的沉淀溶解平衡图像如图所示(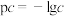 ,不考虑离子的水解)。下列叙述正确的是
,不考虑离子的水解)。下列叙述正确的是
| A.横坐标x为6.54 |
B.P点表示 的饱和溶液 的饱和溶液 |
C.上述两溶液混合后,滴入 溶液先生成AgCl沉淀 溶液先生成AgCl沉淀 |
D. 平衡体系中 平衡体系中 |
您最近一年使用:0次
2022-12-07更新
|
350次组卷
|
3卷引用:浙江省强基联盟2022-2023学年高三上学期12月联考化学试题
浙江省强基联盟2022-2023学年高三上学期12月联考化学试题 浙江省宁波市余姚中学2022-2023学年高二下学期3月月考化学试题 (已下线)【2023】【高二上】【源清中学】【期末考】【高中化学】【廖汨平收集】
单选题
|
较难(0.4)
解题方法
19. 工业上用铝土矿(主要成分为 ,含有
,含有 、
、 等杂质)制取无水氯化铝的一种工艺流程如下:
等杂质)制取无水氯化铝的一种工艺流程如下:

已知:①
 、
、 ;
;
② 、
、 、
、 、
、 的沸点分别为57.6℃、1023℃、300℃(升华)、180℃(升华)。下列说法不正确的是
的沸点分别为57.6℃、1023℃、300℃(升华)、180℃(升华)。下列说法不正确的是
 ,含有
,含有 、
、 等杂质)制取无水氯化铝的一种工艺流程如下:
等杂质)制取无水氯化铝的一种工艺流程如下:
已知:①

 、
、 ;
;②
 、
、 、
、 、
、 的沸点分别为57.6℃、1023℃、300℃(升华)、180℃(升华)。下列说法不正确的是
的沸点分别为57.6℃、1023℃、300℃(升华)、180℃(升华)。下列说法不正确的是A.步骤I中300℃焙烧可将 还原为Al 还原为Al |
B.步骤II中加入的原料气应为 和 和 |
C.步骤II的尾气经足量NaOH溶液吸收,生成物中有 、NaClO 、NaClO |
D.步骤V中加入铝粉的目的是除去 ,提高 ,提高 纯度 纯度 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
20. 下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 比较H2O2和Fe3+的氧化性 | 取适量H2O2溶液于试管中,滴入Fe2(SO4)3溶液,振荡,观察现象 | 若产生气体使带火星木条复燃,说明Fe3+的氧化性强于H2O2 |
| B | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 若溶液红色变浅,证明Na2CO3溶液中存在水解平衡 |
| C | 检验某有机物是否含有酰胺键 | 将适量有机物放入试管,加入足量NaOH溶液,加热,试管口放置湿润的红色石蕊试纸,观察现象 | 若红色石蕊试纸未变蓝,说明待测样品中不含酰胺键 |
| D | 探究电石与水的反应 | 将电石与饱和食盐水反应产生的气体先通过NaOH溶液,再通入酸性高锰酸钾溶液,观察现象 | 若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
21. 红蓝宝石、祖母绿、金绿猫眼、钻石为举世公认的珍贵宝石。
(1)红宝石是刚玉的一种,主要成分为氧化铝( ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为_______ 。
(2)祖母绿主要成分的化学式为 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)_______ I(Al)。Be能与NaOH溶液反应,请简单说明判断依据:_______ 。
(3)金绿猫眼主要成分的化学式为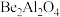 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为_______ 。 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:_______ 。
(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为_______ 。金刚石晶胞结构如图所示,与晶胞面心处碳原子距离最近且等距离的碳原子数为_______ 。

(1)红宝石是刚玉的一种,主要成分为氧化铝(
 ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为(2)祖母绿主要成分的化学式为
 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)(3)金绿猫眼主要成分的化学式为
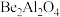 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为

您最近一年使用:0次
三、解答题 添加题型下试题
解答题-无机推断题
|
较难(0.4)
解题方法
22. X通常状况下是一种红黄色气体,相对分子质量小于100,含有三种常见短周期元素。为研究X的组成,5.895g的X分三等份进行实验,过程如下(气体体积已折算至标准状况):

请回答:
(1)X的化学式为_______ 。溶液A的成分为_______ 。
(2)X与 反应的化学方程式为
反应的化学方程式为_______ 。
(3)金(Au)可溶于浓B溶液生成C和金的一价配离子(与 具有相同的空间结构),写出该反应的化学方程式:
具有相同的空间结构),写出该反应的化学方程式:_______ 。
(4)设计一个实验方案,探究溶液F中溶质的阳离子成分:_______ 。

请回答:
(1)X的化学式为
(2)X与
 反应的化学方程式为
反应的化学方程式为(3)金(Au)可溶于浓B溶液生成C和金的一价配离子(与
 具有相同的空间结构),写出该反应的化学方程式:
具有相同的空间结构),写出该反应的化学方程式:(4)设计一个实验方案,探究溶液F中溶质的阳离子成分:
您最近一年使用:0次
23. 以“水煤气”为原料合成氨,需在变换塔中将CO变换成 ,变换塔中主要发生的反应为:
,变换塔中主要发生的反应为:
主反应:
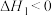
副反应:
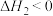
(1)关于合成氨工艺的下列理解,正确的有_______。
(2)相对压力平衡常数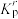 的表达式就是在浓度平衡常数表达式中,用相对分压代替浓度。气体B的相对分压等于其分压p(B)(单位为kPa)除以标准压强
的表达式就是在浓度平衡常数表达式中,用相对分压代替浓度。气体B的相对分压等于其分压p(B)(单位为kPa)除以标准压强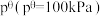 ,其分压p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。
,其分压p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。
变换塔中恒容条件下充入1.0molCO、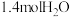 、
、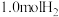 、
、 ,T℃下,反应达到平衡后,测得
,T℃下,反应达到平衡后,测得 0.7mol和
0.7mol和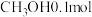 。则T℃时,主反应的相对压力平衡常数
。则T℃时,主反应的相对压力平衡常数
_______ 。
(3)变换塔中主反应正逆反应速率可以表示为: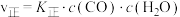 ,
,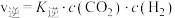 ,
,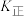 和
和 都是温度的函数。在图中画出
都是温度的函数。在图中画出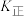 、
、 随温变化的趋势。
随温变化的趋势。_______

(4)以煤为原料生产水煤气,反应过程如下:
为维持炉温,送风发热和制气交替进行,但实际送风发热产生的热量远远多于制气所需热量,其原因是_______ 。
(5)研究发现在以 为主的催化剂上
为主的催化剂上 也可还原NO(需
也可还原NO(需 参与反应),可能发生的反应过程如下,用化学方程式补充该催化反应历程(反应机理):(a)
参与反应),可能发生的反应过程如下,用化学方程式补充该催化反应历程(反应机理):(a) ,(b)
,(b)_______ ,(c)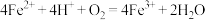 。
。
 ,变换塔中主要发生的反应为:
,变换塔中主要发生的反应为:主反应:

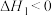
副反应:

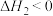
(1)关于合成氨工艺的下列理解,正确的有_______。
| A.在合成氨时,控制温度远高于室温,是为了保证尽可能高平衡转化率和反应速率 |
B.在一定压强下,随着温度的升高,变换塔中CO与 的物质的量之比增大 的物质的量之比增大 |
C.为提高原料中 转化率,应向反应器中加入适当过量的空气 转化率,应向反应器中加入适当过量的空气 |
| D.体系温度升高,可能导致催化剂失活,用热交换器将原料气可预热并使反应体系冷却 |
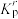 的表达式就是在浓度平衡常数表达式中,用相对分压代替浓度。气体B的相对分压等于其分压p(B)(单位为kPa)除以标准压强
的表达式就是在浓度平衡常数表达式中,用相对分压代替浓度。气体B的相对分压等于其分压p(B)(单位为kPa)除以标准压强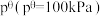 ,其分压p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。
,其分压p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。变换塔中恒容条件下充入1.0molCO、
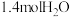 、
、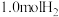 、
、 ,T℃下,反应达到平衡后,测得
,T℃下,反应达到平衡后,测得 0.7mol和
0.7mol和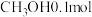 。则T℃时,主反应的相对压力平衡常数
。则T℃时,主反应的相对压力平衡常数
(3)变换塔中主反应正逆反应速率可以表示为:
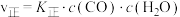 ,
,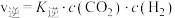 ,
,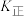 和
和 都是温度的函数。在图中画出
都是温度的函数。在图中画出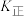 、
、 随温变化的趋势。
随温变化的趋势。
(4)以煤为原料生产水煤气,反应过程如下:
| 反应过程 | 化学方程式 | 焓变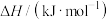 |
| 送风(空气)发热 |  | 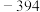 |
| 通水(蒸气)制气 | 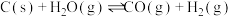 | 131 |
| 副反应 | 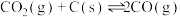 | 172 |
为维持炉温,送风发热和制气交替进行,但实际送风发热产生的热量远远多于制气所需热量,其原因是
(5)研究发现在以
 为主的催化剂上
为主的催化剂上 也可还原NO(需
也可还原NO(需 参与反应),可能发生的反应过程如下,用化学方程式补充该催化反应历程(反应机理):(a)
参与反应),可能发生的反应过程如下,用化学方程式补充该催化反应历程(反应机理):(a) ,(b)
,(b)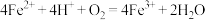 。
。
【知识点】 化学平衡的移动及其影响因素 化学平衡常数的有关计算解读
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
解题方法
24. 四羟甲基盐酸鏻(THPC)是一种高效、广谱、低毒、易生物降解的杀菌剂。某小组用白磷、锌粉、甲醛和盐酸为原料,以如下流程和装置开展实验(夹持仪器、加热装置等已省略)。

已知:①锌与酸生成的强还原性的新生态氢与白磷反应生成活化的磷化氢,再与甲醛及酸反应得到四羟甲基盐酸鏻: 。
。
② 熔点为150℃,难溶于乙醇,与水以任意比例互溶,酸性环境中较稳定,pH在6.5~9.0时开始大量解离。
熔点为150℃,难溶于乙醇,与水以任意比例互溶,酸性环境中较稳定,pH在6.5~9.0时开始大量解离。
③强酸型阳离子交换树脂含有大量强酸性基团,如磺酸基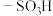 等,可以吸附溶液中的阳离子,同时释放出等量的氢离子。
等,可以吸附溶液中的阳离子,同时释放出等量的氢离子。
请回答:
(1)仪器a的名称是_______ 。
(2)步骤I需要在四口烧瓶中进行反应,第4个瓶口连接的装置X的作用是_______ 。

(3)下列说法不正确的是_______。
(4)用离子交换法和滴定分析法确定产品纯度。

①从下列选项选择合适操作并排序,将实验步骤补充完整:______
准确称取2.00g产品于烧杯中,加入50mL蒸馏水稀释,转入100mL容量瓶,定容、摇匀。将已经用乙醇、蒸馏水、盐酸浸泡预处理的25g强酸型阳离子交换树脂装入离子交换柱,用蒸馏水洗至流出液呈中性。移取20.00mL溶液加入离子交换柱→(_______)→(_______)→(_______)→用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积 mL→另取20.00mL产品溶液做空白实验→选择指示剂→直接用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积
mL→另取20.00mL产品溶液做空白实验→选择指示剂→直接用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积 mL。
mL。
a.控制流出液滴速约40滴/min;
b.控制流出液滴速约20滴/min;
c.弃去前面的20mL流出液,于锥形瓶中,得到50mL流出液;
d.弃去前面的50mL流出液,于锥形瓶中,得到20mL流出液;
e.加入几滴甲基橙作指示剂;
f.加入几滴石蕊作指示剂;
g.加入几滴酚酞作指示剂。
②若NaOH标准液浓度为c,则该产品纯度为_______ 。
③空白实验的指示剂选择酚酞是否合适?理由是_______ 。

已知:①锌与酸生成的强还原性的新生态氢与白磷反应生成活化的磷化氢,再与甲醛及酸反应得到四羟甲基盐酸鏻:
 。
。②
 熔点为150℃,难溶于乙醇,与水以任意比例互溶,酸性环境中较稳定,pH在6.5~9.0时开始大量解离。
熔点为150℃,难溶于乙醇,与水以任意比例互溶,酸性环境中较稳定,pH在6.5~9.0时开始大量解离。③强酸型阳离子交换树脂含有大量强酸性基团,如磺酸基
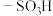 等,可以吸附溶液中的阳离子,同时释放出等量的氢离子。
等,可以吸附溶液中的阳离子,同时释放出等量的氢离子。请回答:
(1)仪器a的名称是
(2)步骤I需要在四口烧瓶中进行反应,第4个瓶口连接的装置X的作用是

(3)下列说法不正确的是_______。
| A.步骤I中温度计水银球应在液面下,不接触烧瓶底部 |
| B.步骤II、IV、V中蒸出的主要物质均为水 |
| C.步骤VI重结晶应选用无水乙醇作溶剂,冷却结晶,得到产品 |
| D.步骤VI重结晶应选用蒸馏水作溶剂,减压脱水,得到产品 |

①从下列选项选择合适操作并排序,将实验步骤补充完整:
准确称取2.00g产品于烧杯中,加入50mL蒸馏水稀释,转入100mL容量瓶,定容、摇匀。将已经用乙醇、蒸馏水、盐酸浸泡预处理的25g强酸型阳离子交换树脂装入离子交换柱,用蒸馏水洗至流出液呈中性。移取20.00mL溶液加入离子交换柱→(_______)→(_______)→(_______)→用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积
 mL→另取20.00mL产品溶液做空白实验→选择指示剂→直接用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积
mL→另取20.00mL产品溶液做空白实验→选择指示剂→直接用NaOH标准溶液滴定至终点,记录消耗NaOH溶液体积 mL。
mL。a.控制流出液滴速约40滴/min;
b.控制流出液滴速约20滴/min;
c.弃去前面的20mL流出液,于锥形瓶中,得到50mL流出液;
d.弃去前面的50mL流出液,于锥形瓶中,得到20mL流出液;
e.加入几滴甲基橙作指示剂;
f.加入几滴石蕊作指示剂;
g.加入几滴酚酞作指示剂。
②若NaOH标准液浓度为c,则该产品纯度为
③空白实验的指示剂选择酚酞是否合适?理由是
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
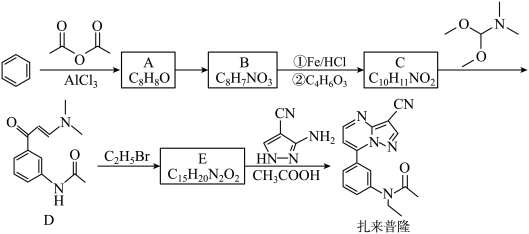
25. 某研究小组按下列路线合成安眠药扎来普隆:
已知: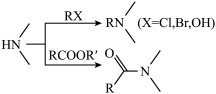
请回答:
(1)下列说法不正确的是_______。
(2)化合物E的结构简式是_______ 。
(3)C→D的化学方程式:_______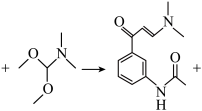 _______。
_______。_______
(4)写出同时符合下列条件的化合物C的同分异构体的结构简式:_______ 。
①1H-NMR谱和IR谱检测表明:分子中有6种不同化学环境的H原子,无甲基,含碳氮双键;
②包含 和另一个六元环。
和另一个六元环。
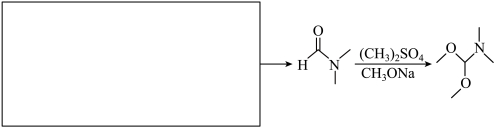
(5)补充完整从甲醇合成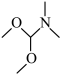 的路线(用流程图表示,注明反应条件,无机试剂任选)。
的路线(用流程图表示,注明反应条件,无机试剂任选)。______

已知:

请回答:
(1)下列说法不正确的是_______。
| A.A→B的反应所需试剂为浓硝酸、浓硫酸 |
| B.化合物B中含氧官能团是醛基、硝基 |
| C.B→C的反应过程中发生了还原反应、取代反应 |
D.扎来普隆的分子式是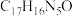 |
(3)C→D的化学方程式:_______
 _______。
_______。(4)写出同时符合下列条件的化合物C的同分异构体的结构简式:
①1H-NMR谱和IR谱检测表明:分子中有6种不同化学环境的H原子,无甲基,含碳氮双键;
②包含
 和另一个六元环。
和另一个六元环。(5)补充完整从甲醇合成
 的路线(用流程图表示,注明反应条件,无机试剂任选)。
的路线(用流程图表示,注明反应条件,无机试剂任选)。
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、有机化学基础、化学与STSE、物质结构与性质、常见无机物及其应用、化学实验基础、认识化学科学
试卷题型(共 25题)
题型
数量
单选题
20
填空题
1
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电镀 蛋白质的变性 高分子材料 | |
| 2 | 0.65 | 轨道表示式 价层电子对互斥理论的应用 利用杂化轨道理论判断分子的空间构型 | |
| 3 | 0.85 | 氯气 硅的制备 明矾的净水作用及原理 食品添加剂 | |
| 4 | 0.65 | 化学科学对人类文明发展的意义 石油分馏 煤的干馏 | |
| 5 | 0.65 | 淀粉和纤维素组成与结构 淀粉、纤维素的水解 | |
| 6 | 0.65 | 氯气与碱溶液反应 氨气的实验室制法 过氧化钠的物理性质、组成、结构及用途 萃取和分液 | |
| 7 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 | |
| 8 | 0.65 | 氧化还原反应有关计算 氧化还原反应的规律 基于氧化还原反应守恒规律的计算 电子转移计算 | |
| 9 | 0.65 | 电负性概念 键能、键长、键角及应用 氢键对物质性质的影响 | |
| 10 | 0.65 | 氧化还原反应的规律 二氧化硫与其他强氧化剂的反应 盐类水解在生活、生产中的应用 | |
| 11 | 0.85 | 离子方程式的书写 离子方程式的正误判断 氧化还原反应方程式的配平 亚硫酸及其盐 | |
| 12 | 0.65 | 分子的手性 多官能团有机物的结构与性质 | |
| 13 | 0.65 | 元素金属性与非金属性递变规律的理解及应用 根据原子结构进行元素种类推断 电子排布式 利用杂化轨道理论判断化学键杂化类型 | |
| 14 | 0.4 | 弱电解质的电离平衡 盐类水解规律理解及应用 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 15 | 0.4 | 化学平衡图像分析 | |
| 16 | 0.85 | 盖斯定律理解 盖斯定律与热化学方程式 盖斯定律的应用 | |
| 17 | 0.4 | 原电池原理的应用 原电池正负极判断 新型电池 | |
| 18 | 0.65 | 沉淀溶解平衡的应用 溶度积常数相关计算 | |
| 19 | 0.4 | 含氧化铝的混合物的提纯 物质分离、提纯综合应用 常见无机物的制备 | |
| 20 | 0.65 | 氧化性、还原性强弱的比较 盐类水解规律理解及应用 化学实验方案的设计与评价 酰胺的性质与应用 | |
| 二、填空题 | |||
| 21 | 0.65 | 物质结构与性质综合考查 电子排布式 电离能变化规律 | |
| 三、解答题 | |||
| 22 | 0.4 | 根据n=m/M进行相关计算 氧化还原反应方程式的配平 无机综合推断 | 无机推断题 |
| 23 | 0.65 | 化学平衡的移动及其影响因素 化学平衡常数的有关计算 | 原理综合题 |
| 24 | 0.4 | 常见无机物的制备 物质含量的测定 | 实验探究题 |
| 25 | 0.4 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



