现有下列物质 ①熔化的NaCl ②盐酸 ③氯气 ④冰醋酸 ⑤铜 ⑥酒精 ⑦硫酸氢钠 ⑧液氨 ⑨SO2,请按要求回答下列问题。
(1)属于强电解质的是_______ (填序号)
(2)在上述状态下能导电的是_______ (填序号)
(3)属于弱电解质的是_______ (填序号)
(4)属于非电解质,但溶于水后的水溶液能导电的是_______ (填序号)
(5)可以证明④是弱酸的事实是_______(填序号)
(6)有下列物质的溶液:a.CH3COOH、b.HCl、c.H2SO4、d.NaHSO4,若四种溶液的物质的量浓度相同,其由水电离c(H+)由大到小顺序为_______ (用字母序号表示,下同)。若四种溶液的c(H+)相同,其物质的量浓度由大到小顺序为_______ 。
(7)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
a.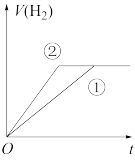 b.
b. 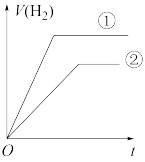 c.
c. 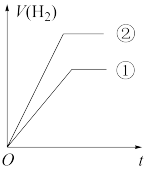 d.
d. 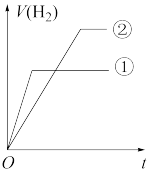
(1)属于强电解质的是
(2)在上述状态下能导电的是
(3)属于弱电解质的是
(4)属于非电解质,但溶于水后的水溶液能导电的是
(5)可以证明④是弱酸的事实是_______(填序号)
| A.乙酸和水能以任意比例混溶 |
| B.在乙酸水溶液中含有未电离的乙酸分子 |
| C.乙酸与Na2CO3溶液反应放出CO2气体 |
| D.1 mol·L-1的乙酸水溶液能使紫色石蕊溶液变红色 |
(7)常温下,有
 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是a.
 b.
b.  c.
c.  d.
d. 
21-22高二下·宁夏银川·阶段练习 查看更多[7]
宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题(已下线)1.2.1 电解质及其电离(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)(已下线)3.1.1 电离平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)湖北省武汉市武钢三中2022-2023学年高二上学期第一次月考化学试题广东省清远市四校联盟2022-2023学年高二上学期期中考试化学试题广东省广州市第三中学2022-2023学年高二上学期期末测试化学试题四川省成都市第八中学校2022-2023学年高二上学期11月期中考试化学试题
更新时间:2022-12-06 20:41:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。
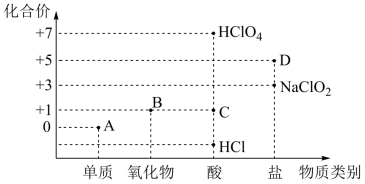
(1)已知D可用于实验室制O2,其焰色试验为紫色。A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则M在水溶液中的电离方程式为_______ 。
(3)已知Br2的性质和Cl2有一定的相似性,写出Br2在一定条件下与NaOH溶液反应的离子方程式_______ 。
(4)臭氧氧化技术被广泛用于饮用水的处理,当水中含有Br-时会产生易致癌的BrO 。但水中BrO
。但水中BrO 能被活性炭有效去除,其去除机理分为两步:
能被活性炭有效去除,其去除机理分为两步:
第一步是活性炭吸附BrO
第二步是BrO 被活性炭还原为Br-,
被活性炭还原为Br-,
其反应方程式(未配平)如下:
①_______。
②*C+BrO-→Br- +*CO2
反应的总方程式为:2BrO + 3*C=2Br-+3*CO2 。
+ 3*C=2Br-+3*CO2 。
已知:其中*C代表活性炭表面,*CO2代表活性炭表面氧化物;每步中的*C被氧化为*CO2,则反应①的方程式为_______ ;则反应①与反应②中参加反应的*C个数之比为_______ 。

(1)已知D可用于实验室制O2,其焰色试验为紫色。A、B、C、D四种物质中,属于电解质的是
(2)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则M在水溶液中的电离方程式为
(3)已知Br2的性质和Cl2有一定的相似性,写出Br2在一定条件下与NaOH溶液反应的离子方程式
(4)臭氧氧化技术被广泛用于饮用水的处理,当水中含有Br-时会产生易致癌的BrO
 。但水中BrO
。但水中BrO 能被活性炭有效去除,其去除机理分为两步:
能被活性炭有效去除,其去除机理分为两步:第一步是活性炭吸附BrO

第二步是BrO
 被活性炭还原为Br-,
被活性炭还原为Br-,其反应方程式(未配平)如下:
①_______。
②*C+BrO-→Br- +*CO2
反应的总方程式为:2BrO
 + 3*C=2Br-+3*CO2 。
+ 3*C=2Br-+3*CO2 。已知:其中*C代表活性炭表面,*CO2代表活性炭表面氧化物;每步中的*C被氧化为*CO2,则反应①的方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下12种物质为中学化学中常见的物质:
①Cu ②KCl 固体 ③NaHSO4 固体 ④SO3 ⑤浓H2SO4 ⑥C2H5OH(酒精) ⑦CaO 固体
⑧BaSO4固体 ⑨NaOH 固体 ⑩Al2O3固体 ⑪CuSO4·5H2O晶体 ⑫CO
请按下列要求回答(填写物质的标号):
(1)属于非电解质的是_______________
(2)在水溶液中能电离出H+的是_________________
(3)属于酸性氧化物的是_______________________
(4)既不是电解质又不是非电解质的是____________________
①Cu ②KCl 固体 ③NaHSO4 固体 ④SO3 ⑤浓H2SO4 ⑥C2H5OH(酒精) ⑦CaO 固体
⑧BaSO4固体 ⑨NaOH 固体 ⑩Al2O3固体 ⑪CuSO4·5H2O晶体 ⑫CO
请按下列要求回答(填写物质的标号):
(1)属于非电解质的是
(2)在水溶液中能电离出H+的是
(3)属于酸性氧化物的是
(4)既不是电解质又不是非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十种物质:①铝 ②SiO2 ③熔融NaCl ④稀硫酸 ⑤KOH固体 ⑥FeSO4溶液 ⑦NH3 ⑧新制备的氢氧化铁胶体分散系 ⑨HCl ⑩Na2O2
(1)上述物质属于非电解质的有___________________ 。(填序号)
(2)上述物质能导电的有____________________ 。(填序号)
(3)往装有⑧的试管中逐滴加入④至过量的现象是:____________________ 。
(4)请写出①与⑤的溶液反应的离子方程式:_____________________________ 。
(5)请写出⑩与CO2反应的化学方程式:______________________________ 。
(1)上述物质属于非电解质的有
(2)上述物质能导电的有
(3)往装有⑧的试管中逐滴加入④至过量的现象是:
(4)请写出①与⑤的溶液反应的离子方程式:
(5)请写出⑩与CO2反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一定条件下,反应A(g)+B(g)  C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
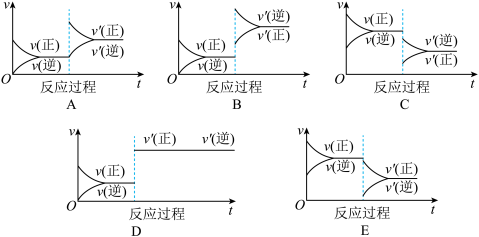
(1)升温,达到新平衡的是________ ,新平衡中C的体积分数________ (填“增大”、“减小”或“不变”,下同)。
(2)降压,达到新平衡的是________ ,A的转化率________ 。
(3)减少C的量,达到新平衡的是_______ 。
(4)增加A的量,达到新平衡的是____ ,此时B的转化率________ ,A的转化率________ 。
(5)使用催化剂,达到平衡的是________ , C的质量分数________ 。
 C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
(1)升温,达到新平衡的是
(2)降压,达到新平衡的是
(3)减少C的量,达到新平衡的是
(4)增加A的量,达到新平衡的是
(5)使用催化剂,达到平衡的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】我国天然气储存量丰富,可用于合成水煤气,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)已知温度、压强和水碳比
CO(g)+3H2(g)已知温度、压强和水碳比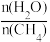 对甲烷平衡含量[
对甲烷平衡含量[ (CH4)]的影响如图:
(CH4)]的影响如图:
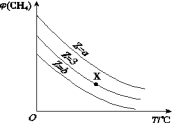
(1)工业上选择高温条件,理由是______________________________ 。
(2)已知:在700℃,1MPa时,1molCH4与1molH2O在2L的密闭容器中反应,6min达到平衡,此时CH4的转化率为80%,则0-6min H2的平均反应速率为v(H2)=_______ 。假设反应开始时容器内气体总压强为p0,则平衡时气体的总压强p =__________ (结果用p0的代数式表示)
(3)在恒压下,平衡时CH4的体积分数与Z(水碳比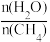 )和T(温度)的关系如图所示,图中三条线Z的大小关系为
)和T(温度)的关系如图所示,图中三条线Z的大小关系为________________ (填a、b与3的大小关系)。温度不变时,图中X点对应的平衡在加压后 (CH4)
(CH4)__________ (填“增大”、“减小”或“不变”)。
(4)为了提高甲烷的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有________________ 。
(5)在700℃时,反应达到平衡后再向其中加入1.0 mol CH4、1.0 mol H2O、1.0 mol CO和1.0 mol H2 ,此时的v正__________ v逆(填“>”“<”或“=”),理由是_____________ 。
 CO(g)+3H2(g)已知温度、压强和水碳比
CO(g)+3H2(g)已知温度、压强和水碳比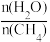 对甲烷平衡含量[
对甲烷平衡含量[ (CH4)]的影响如图:
(CH4)]的影响如图:
(1)工业上选择高温条件,理由是
(2)已知:在700℃,1MPa时,1molCH4与1molH2O在2L的密闭容器中反应,6min达到平衡,此时CH4的转化率为80%,则0-6min H2的平均反应速率为v(H2)=
(3)在恒压下,平衡时CH4的体积分数与Z(水碳比
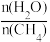 )和T(温度)的关系如图所示,图中三条线Z的大小关系为
)和T(温度)的关系如图所示,图中三条线Z的大小关系为 (CH4)
(CH4)(4)为了提高甲烷的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有
(5)在700℃时,反应达到平衡后再向其中加入1.0 mol CH4、1.0 mol H2O、1.0 mol CO和1.0 mol H2 ,此时的v正
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。
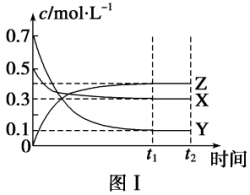
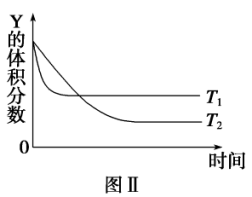
(1)写出容器中发生反应的方程式___________ ;正反应为___________ 反应 填“放热”或“吸热”
填“放热”或“吸热” 。
。
(2)当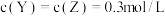 时,该反应
时,该反应___________ 达到平衡状态 填“已”或“未”
填“已”或“未” ;由图Ⅰ,若
;由图Ⅰ,若 为10min,则
为10min,则 时间内,
时间内,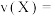
___________ ;
(3)其它条件不变,再充入一定量X,平衡___________ 移动 填“正向”、“逆向”、或“不”
填“正向”、“逆向”、或“不” ,X的转化率
,X的转化率___________  填“增大”、“减小”、或“不变”
填“增大”、“减小”、或“不变” 。
。
 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。

(1)写出容器中发生反应的方程式
 填“放热”或“吸热”
填“放热”或“吸热” 。
。(2)当
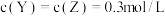 时,该反应
时,该反应 填“已”或“未”
填“已”或“未” ;由图Ⅰ,若
;由图Ⅰ,若 为10min,则
为10min,则 时间内,
时间内,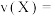
(3)其它条件不变,再充入一定量X,平衡
 填“正向”、“逆向”、或“不”
填“正向”、“逆向”、或“不” ,X的转化率
,X的转化率 填“增大”、“减小”、或“不变”
填“增大”、“减小”、或“不变” 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】运用所学知识,解决下列问题。
(1)现欲测定100℃沸水的pH及酸碱性,溶液呈___________ (填“酸”、“碱”或“中”)性;若用pH计测定,则pH___________ (填“>”、“<”或“=”)7。
(2)25℃时欲使水电离产生的c(H+)=10-13mol·L-1,配制1L溶液,应向其中加入5.0mol·L-1的盐酸溶液___________ L。
(3)25℃时,将①H+、②Fe3+、③Al3+、④Na+、⑤HS-、⑥CH3COO-、⑦CO 、⑧NH
、⑧NH 分别加入H2O中,基本上不影响水的电离平衡的是
分别加入H2O中,基本上不影响水的电离平衡的是___________ (填入相应序号)。
(4)请在下列题目中填入“增大”、“减小”或“不变”。
①0.1mol·L-1CH3COOH溶液加水稀释,CH3COOH的电离度___________ 。
②常温下,用蒸馏水不断稀释醋酸,溶液中 的值
的值___________ 。
(1)现欲测定100℃沸水的pH及酸碱性,溶液呈
(2)25℃时欲使水电离产生的c(H+)=10-13mol·L-1,配制1L溶液,应向其中加入5.0mol·L-1的盐酸溶液
(3)25℃时,将①H+、②Fe3+、③Al3+、④Na+、⑤HS-、⑥CH3COO-、⑦CO
 、⑧NH
、⑧NH 分别加入H2O中,基本上不影响水的电离平衡的是
分别加入H2O中,基本上不影响水的电离平衡的是(4)请在下列题目中填入“增大”、“减小”或“不变”。
①0.1mol·L-1CH3COOH溶液加水稀释,CH3COOH的电离度
②常温下,用蒸馏水不断稀释醋酸,溶液中
 的值
的值
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】常温下,有下列五种溶液:
回答下列问题:
(1)溶液①稀释到原来的10倍后的溶液pH______ ③溶液的pH(填“>”或“=”或“<”,下同),①和④两溶液中水电离出的c(H+):①_______ ④
(2)在相同温度时100mL ②的溶液与10mL ①的溶液相比较,下列数值前者大于后者的是_______ (填字母)。
A .中和时所需NaOH的量 B .电离程度
C .水电离出的c(H+) D. CH3COOH的物质的量
(3)用水稀释⑤时,溶液中随着水量的增加而减小的是______ (填字母)。
A.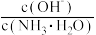 B.
B.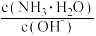
C. c(H+)和c(OH-)的乘积 D.OH-的物质的量
(4)联氨(N2H4)溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式:_______________________________________ 。
(5)已知CH3COOH的电离平衡常数Ka=1.8×10-5 ,另一种二元弱酸H2B的电离平衡常数为K1=4.3×10- 4 ,K2=5.6×10-1 1 试写出向Na2B溶液中加入过量CH3COOH溶液的化学方程式:_________________________________________ 。
| ① | ② | ③ | ④ | ⑤ |
| 0.1 mol·L-1 CH3COOH溶液 | 0.01mol·L-1 CH3COOH溶液 | pH=2 CH3COOH溶液 | 0.1 mol·L-1 NaOH溶液 | 0.1mol·L-1 氨水 |
(1)溶液①稀释到原来的10倍后的溶液pH
(2)在相同温度时100mL ②的溶液与10mL ①的溶液相比较,下列数值前者大于后者的是
A .中和时所需NaOH的量 B .电离程度
C .水电离出的c(H+) D. CH3COOH的物质的量
(3)用水稀释⑤时,溶液中随着水量的增加而减小的是
A.
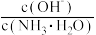 B.
B.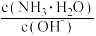
C. c(H+)和c(OH-)的乘积 D.OH-的物质的量
(4)联氨(N2H4)溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式:
(5)已知CH3COOH的电离平衡常数Ka=1.8×10-5 ,另一种二元弱酸H2B的电离平衡常数为K1=4.3×10- 4 ,K2=5.6×10-1 1 试写出向Na2B溶液中加入过量CH3COOH溶液的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如表是几种常见弱酸的电离平衡常数(25℃),回答下列各题:
结合表中给出的电离常数回答下列问题:
(1)上述四种酸中,酸性最弱的是___________。
(2)将pH和体积均相同的 溶液和
溶液和 溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是___________ 的pH变化情况,
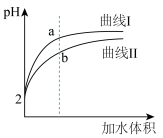
(3)下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是___________ (填序号)。
A.升高温度 B.加水稀释 C.加少量的 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体
(4)依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式___________ 。
(5)室温下,测得10mL 醋酸(
醋酸( )溶液的电离度约为1%。完成下列填空:
)溶液的电离度约为1%。完成下列填空:
①上述醋酸溶液的pH=___________ 。
②加水稀释上述醋酸溶液,相对于原溶液,此时
___________ 。
A.不断减小 B.不断增大 C.无明显变化
(6)已知醋酸的酸性强于碳酸,请问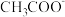 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是___________ 。
(7)某些共价化合物(如 、
、 、
、 等)在液态时会发生微弱的电离,如:
等)在液态时会发生微弱的电离,如: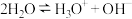 ,则液态
,则液态 的电离方程式为
的电离方程式为___________ 。
(8)现有浓度均为 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是___________ (用序号表示)。
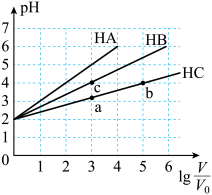
(9)常温下,pH均为2、体积均为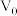 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随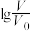 的变化关系如图所示,下列叙述错误的是___________。
的变化关系如图所示,下列叙述错误的是___________。
| 酸 |  |  | HCN | HClO |
| 电离平衡常数 |  |  | 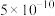 |  |
(1)上述四种酸中,酸性最弱的是___________。
A. | B. | C.HCN | D.HClO |
(2)将pH和体积均相同的
 溶液和
溶液和 溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
(3)下列能使醋酸溶液中
 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是A.升高温度 B.加水稀释 C.加少量的
 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体(4)依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式
(5)室温下,测得10mL
 醋酸(
醋酸( )溶液的电离度约为1%。完成下列填空:
)溶液的电离度约为1%。完成下列填空:①上述醋酸溶液的pH=
②加水稀释上述醋酸溶液,相对于原溶液,此时

A.不断减小 B.不断增大 C.无明显变化
(6)已知醋酸的酸性强于碳酸,请问
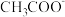 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是(7)某些共价化合物(如
 、
、 、
、 等)在液态时会发生微弱的电离,如:
等)在液态时会发生微弱的电离,如: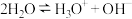 ,则液态
,则液态 的电离方程式为
的电离方程式为(8)现有浓度均为
 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是(9)常温下,pH均为2、体积均为
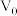 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随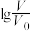 的变化关系如图所示,下列叙述错误的是___________。
的变化关系如图所示,下列叙述错误的是___________。
A.常温下: |
| B.HC的电离程度,a点<b点 |
C.当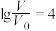 时,三种溶液同时升高温度, 时,三种溶液同时升高温度,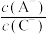 减小 减小 |
| D.a点酸的总浓度小于b点酸的总浓度 |
您最近一年使用:0次
【推荐1】合理利用或转化NO2、SO2、CO、NO等污染性气体是人们共同关注的课题。
Ⅰ.某化学课外小组查阅资料后得知:2NO(g)+O2(g)2NO2(g)的反应历程分两步:
①2NO(g)⇌N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ΔH1<0
②N2O2(g)+O2(g)⇌2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ΔH2<0
请回答下列问题:
(1)反应2NO(g)+O2(g)⇌2NO2(g)的ΔH=________ (用含ΔH1和ΔH2的式子表示)。一定温度下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=________ 。
(2)决定2NO(g)+O2(g)⇌2NO2(g)反应速率的是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________ E2(填“>”“<”或“=”)。

Ⅱ.(3)反应N2O4(g)⇌2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是____________________ ,理由是_________________________________________
(4)在25 ℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1 HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示25 ℃时NH3·H2O的电离常数Kb=____ 。用质量分数为17%,密度为0.93 g·cm-3的氨水,配制200 mL a mol·L-1的氨水溶液,所需原氨水的体积V=________ mL。
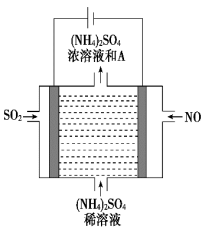
(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为__________ ,阴极的电极反应式是_____________________________________________ 。
Ⅰ.某化学课外小组查阅资料后得知:2NO(g)+O2(g)2NO2(g)的反应历程分两步:
①2NO(g)⇌N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ΔH1<0
②N2O2(g)+O2(g)⇌2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ΔH2<0
请回答下列问题:
(1)反应2NO(g)+O2(g)⇌2NO2(g)的ΔH=
(2)决定2NO(g)+O2(g)⇌2NO2(g)反应速率的是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1

Ⅱ.(3)反应N2O4(g)⇌2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是
(4)在25 ℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1 HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示25 ℃时NH3·H2O的电离常数Kb=

(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有一瓶市售白醋,化学课外兴趣小组欲用酸碱滴定法测定其含酸量(设其中的酸均为乙酸)。请你参与他们的实验并回答有关问题:选择酚酞作指示剂,用标准NaOH溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:
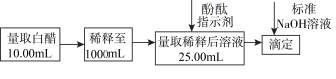
已知:国家标准规定酿造白醋中醋酸含量不得低于0.035g·mL-1。
(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后___________ 。
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示:
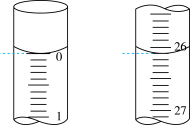
已知实验所用标准NaOH溶液的浓度为0.0600mol/L,根据上述滴定结果计算原酿造食醋中醋酸含量为___________ g/mL(结果保留两位有效数字),由此可知该白醋是否符合国家标准。
③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是___________ (填标号)。
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。

①滴定醋酸的曲线是___________ (填“Ⅰ”或“Ⅱ”)。
②V1和V2的关系:V1___________ V2 (填“>”“=”或“<”)。
(3)已知常温下向0.1mol·L-1的NaHA 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHA的电离方程式为___________ 。
②若在此溶液中能检测到H2A 分子,则此溶液中c(A2-)___________ c(H2A)(填“>”“<”或“=”)。
③若H2A的一级电离为H2A=H+ +HA-,常温下0.1mol·L-1H2A溶液中的c(H+)=0.11mol·L-1,则0.1mol·L-1NaHA溶液中的c(H+)___________ 0.01mol·L-1(填“>”“<”或“=”)。

已知:国家标准规定酿造白醋中醋酸含量不得低于0.035g·mL-1。
(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示:

已知实验所用标准NaOH溶液的浓度为0.0600mol/L,根据上述滴定结果计算原酿造食醋中醋酸含量为
③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。

①滴定醋酸的曲线是
②V1和V2的关系:V1
(3)已知常温下向0.1mol·L-1的NaHA 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHA的电离方程式为
②若在此溶液中能检测到H2A 分子,则此溶液中c(A2-)
③若H2A的一级电离为H2A=H+ +HA-,常温下0.1mol·L-1H2A溶液中的c(H+)=0.11mol·L-1,则0.1mol·L-1NaHA溶液中的c(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。
②c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
④c(CH3COO-)>c(Na+)>c(OH-) >c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是________ ,上述四种离子浓度的大小顺序为_______ (填编号)。
(2)若上述关系中③是正确的,则溶液中的溶质为_________ 。
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)_______ c(CH3COOH)(填“大于”、“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系是c(H+)_____ c(OH-)。
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。
②c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
④c(CH3COO-)>c(Na+)>c(OH-) >c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若上述关系中③是正确的,则溶液中的溶质为
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)
您最近一年使用:0次



