我国天然气储存量丰富,可用于合成水煤气,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)已知温度、压强和水碳比
CO(g)+3H2(g)已知温度、压强和水碳比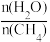 对甲烷平衡含量[
对甲烷平衡含量[ (CH4)]的影响如图:
(CH4)]的影响如图:
(1)工业上选择高温条件,理由是______________________________ 。
(2)已知:在700℃,1MPa时,1molCH4与1molH2O在2L的密闭容器中反应,6min达到平衡,此时CH4的转化率为80%,则0-6min H2的平均反应速率为v(H2)=_______ 。假设反应开始时容器内气体总压强为p0,则平衡时气体的总压强p =__________ (结果用p0的代数式表示)
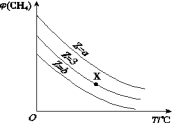
(3)在恒压下,平衡时CH4的体积分数与Z(水碳比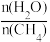 )和T(温度)的关系如图所示,图中三条线Z的大小关系为
)和T(温度)的关系如图所示,图中三条线Z的大小关系为________________ (填a、b与3的大小关系)。温度不变时,图中X点对应的平衡在加压后 (CH4)
(CH4)__________ (填“增大”、“减小”或“不变”)。
(4)为了提高甲烷的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有________________ 。
(5)在700℃时,反应达到平衡后再向其中加入1.0 mol CH4、1.0 mol H2O、1.0 mol CO和1.0 mol H2 ,此时的v正__________ v逆(填“>”“<”或“=”),理由是_____________ 。
 CO(g)+3H2(g)已知温度、压强和水碳比
CO(g)+3H2(g)已知温度、压强和水碳比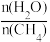 对甲烷平衡含量[
对甲烷平衡含量[ (CH4)]的影响如图:
(CH4)]的影响如图:
(1)工业上选择高温条件,理由是
(2)已知:在700℃,1MPa时,1molCH4与1molH2O在2L的密闭容器中反应,6min达到平衡,此时CH4的转化率为80%,则0-6min H2的平均反应速率为v(H2)=
(3)在恒压下,平衡时CH4的体积分数与Z(水碳比
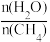 )和T(温度)的关系如图所示,图中三条线Z的大小关系为
)和T(温度)的关系如图所示,图中三条线Z的大小关系为 (CH4)
(CH4)(4)为了提高甲烷的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有
(5)在700℃时,反应达到平衡后再向其中加入1.0 mol CH4、1.0 mol H2O、1.0 mol CO和1.0 mol H2 ,此时的v正
18-19高二下·黑龙江大庆·开学考试 查看更多[1]
(已下线)【百强校】黑龙江省大庆实验中学2018-2019学年高二下学期开学考试化学试题
更新时间:2019/03/05 20:28:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
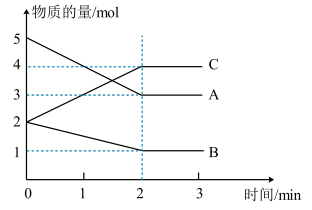
(1)该反应的化学方程式为___ 。
(2)反应开始至2min时,B的平均反应速率为___ 。
(3)能说明该反应已达到平衡状态的是___ (填字母)。
A.v(A)=2v(B)
B.容器内压强保持不变
C.2v逆(A)=v正(B)
D.容器内混合气体的密度保持不变
(4)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是___ (填序号)。
①降低温度 ②加入催化剂(正) ③增大容器容积

(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A.v(A)=2v(B)
B.容器内压强保持不变
C.2v逆(A)=v正(B)
D.容器内混合气体的密度保持不变
(4)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂(正) ③增大容器容积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在2 L恒容密闭容器中,发生反应 2NO(g)+O2(g) 2NO2(g)。
2NO2(g)。
⑴某温度时,按物质的量比2∶1充入NO和O2开始反应,n(NO)随时间变化如表:
0~4s内以O2浓度变化表示的反应速率__________ 1~5s内以NO浓度变化表示的反应速率(选填“小于”、“大于”、“等于”)。
⑵该反应的平衡常数表达式为K=______ 。能说明该反应已达到平衡状态的是_____ 。
A.气体颜色保持不变 B.气体平均相对分子质量保持不变
C.υ逆(NO)=2υ正(O2) D.气体密度保持不变
⑶已知:K300℃>K400℃。下列措施能使该反应的反应速率增大且平衡向正反应方向移动的是________ 。
A.升高温度 B.充入Ar使压强增大 C.充入O2使压强增大 D.选择高效催化剂
⑷将amolNO和bmolO2发生反应,要使反应物和生成物物质的量之比为1∶2,则a/b的取值范围是_________ 。
 2NO2(g)。
2NO2(g)。⑴某温度时,按物质的量比2∶1充入NO和O2开始反应,n(NO)随时间变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
⑵该反应的平衡常数表达式为K=
A.气体颜色保持不变 B.气体平均相对分子质量保持不变
C.υ逆(NO)=2υ正(O2) D.气体密度保持不变
⑶已知:K300℃>K400℃。下列措施能使该反应的反应速率增大且平衡向正反应方向移动的是
A.升高温度 B.充入Ar使压强增大 C.充入O2使压强增大 D.选择高效催化剂
⑷将amolNO和bmolO2发生反应,要使反应物和生成物物质的量之比为1∶2,则a/b的取值范围是
您最近一年使用:0次
【推荐3】氮的氧化物会对空气造成污染。
(1) 会造成光化学烟雾,一般利用碱液吸收
会造成光化学烟雾,一般利用碱液吸收 防止污染环境,
防止污染环境, 发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收
发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收 时发生反应的化学方程式为
时发生反应的化学方程式为_______ 。
(2)在 气体中存在
气体中存在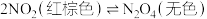 的关系。一定温度下,体积为2L的恒容密闭容器中
的关系。一定温度下,体积为2L的恒容密闭容器中 和
和 的物质的量随时间变化的关系如图所示。回答下列问题:
的物质的量随时间变化的关系如图所示。回答下列问题:
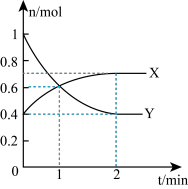
①曲线X表示_______ (填化学式)的物质的量随时间的变化。
②第1min时v(Y)_______ 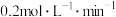 (“>”“<”“=”或“无法确定”)。
(“>”“<”“=”或“无法确定”)。
③反应达到平衡时, 的转化率为
的转化率为_______ 。
④假设上述反应的正反应速率为 、逆反应速率为
、逆反应速率为 ,当温度升高时,
,当温度升高时, 和
和 的变化情况为
的变化情况为_____ 。
⑤下列叙述能表示该反应达到平衡状态的是_______ (填字母)。
a.容器中气体的颜色不再改变
b.容器中 、
、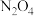 气体的物质的量相等
气体的物质的量相等
c.容器中气体的密度不再改变
d.相同时间内,反应消耗2mol 的同时消耗1mol
的同时消耗1mol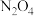
(1)
 会造成光化学烟雾,一般利用碱液吸收
会造成光化学烟雾,一般利用碱液吸收 防止污染环境,
防止污染环境, 发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收
发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收 时发生反应的化学方程式为
时发生反应的化学方程式为(2)在
 气体中存在
气体中存在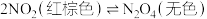 的关系。一定温度下,体积为2L的恒容密闭容器中
的关系。一定温度下,体积为2L的恒容密闭容器中 和
和 的物质的量随时间变化的关系如图所示。回答下列问题:
的物质的量随时间变化的关系如图所示。回答下列问题: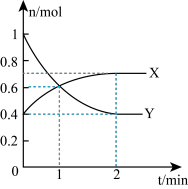
①曲线X表示
②第1min时v(Y)
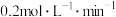 (“>”“<”“=”或“无法确定”)。
(“>”“<”“=”或“无法确定”)。③反应达到平衡时,
 的转化率为
的转化率为④假设上述反应的正反应速率为
 、逆反应速率为
、逆反应速率为 ,当温度升高时,
,当温度升高时, 和
和 的变化情况为
的变化情况为⑤下列叙述能表示该反应达到平衡状态的是
a.容器中气体的颜色不再改变
b.容器中
 、
、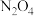 气体的物质的量相等
气体的物质的量相等c.容器中气体的密度不再改变
d.相同时间内,反应消耗2mol
 的同时消耗1mol
的同时消耗1mol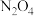
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】mA(g)+nB(g)  pC(g)+qD(g),当反应达到平衡后,若压强改变,其vt图象如下:
pC(g)+qD(g),当反应达到平衡后,若压强改变,其vt图象如下:
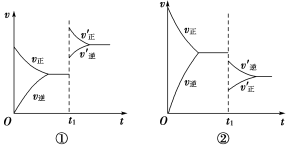
(1)图①表示的压强变化是________ ,平衡移动方向是向________ 方向。
(2)图②表示的压强变化是________ ,平衡移动方向是向________ 方向。
(3)m+n________ p+q(填“>”、“=”或“<”)。
 pC(g)+qD(g),当反应达到平衡后,若压强改变,其vt图象如下:
pC(g)+qD(g),当反应达到平衡后,若压强改变,其vt图象如下:
(1)图①表示的压强变化是
(2)图②表示的压强变化是
(3)m+n
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与时间的关系可由图表示:

在下列因素中
①盐酸的浓度 ②镁带的表面积 ③溶液的浓度 ④氢气的压强 ⑤Cl−的浓度
(1)影响反应速率的因素___ ;
(2)解释图中AB段形成的原因___ ;
(3)解释图中t1时刻后速率变小的原因___

在下列因素中
①盐酸的浓度 ②镁带的表面积 ③溶液的浓度 ④氢气的压强 ⑤Cl−的浓度
(1)影响反应速率的因素
(2)解释图中AB段形成的原因
(3)解释图中t1时刻后速率变小的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】不同温度、压强下,在合成氨平衡体系中N2(g)+3H2(g) 2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
(1)N原子最外层电子排布式为___ ,氮气能在大气中稳定存在的原因是___ 。
(2)已知该反应在2L密闭容器中进行,5min内氨的质量增加了1.7g,则此段时间内H2的平均反应速率为___ mol/(L·min)。
(3)该反应的平衡常数表达式___ ,升高温度,K值___ (选填“增大”、“减小”或“不变”)。T℃(K=3.6)的某一时刻下,c(N2)=1mol/L,c(H2)=3mol/L,c(NH3)=9mol/L,在这种情况下该反应是否处于平衡状态___ (选填“是”、“否”),此时反应速率是v正___ v逆(选填“>”、“<”或“=”)。
(4)合成氨是生产条件一般为压强在20MPa~50MPa,温度为500℃左右,选用该条件的主要原因是___ 。
(5)从表中数据可知,在该条件下氨的平衡含量并不高,为提高原料利用率,工业生产中采取的措施是___ 。
(6)工业上用氨水吸收SO2尾气,最终得到化肥(NH4)2SO4。(NH4)2SO4溶液中离子浓度由大到小的顺序是___ 。
 2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):| 温度/氨的平衡含量(%)/压强(MPa) | 20 | 30 | 60 | 100 |
| 200 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 19.1 | 26.4 | 42.2 | 57.5 |
(1)N原子最外层电子排布式为
(2)已知该反应在2L密闭容器中进行,5min内氨的质量增加了1.7g,则此段时间内H2的平均反应速率为
(3)该反应的平衡常数表达式
(4)合成氨是生产条件一般为压强在20MPa~50MPa,温度为500℃左右,选用该条件的主要原因是
(5)从表中数据可知,在该条件下氨的平衡含量并不高,为提高原料利用率,工业生产中采取的措施是
(6)工业上用氨水吸收SO2尾气,最终得到化肥(NH4)2SO4。(NH4)2SO4溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)⇌2SO3(g) △H<0;
(1)写出该反应的化学平衡常数表达式K=__________
(2)降低温度,该反应K值__________ ,二氧化硫转化率___________ ,化学反应速率___________ (以上均填增大、减小或不变)。
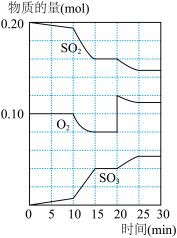
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是___________________________ 。
(4)据图判断,反应进行至20min时,曲线发生变化的原因是_______________________ (用文字表达)。
(5)10min到15min的曲线变化的原因可能是____________ (填写编号)。
A、加了催化剂 B、缩小容器体积
C、降低温度 D、增加SO3的物质的量。
(6)若该反应的密闭容器为2L,则反应15min时,v(SO2)=___________
(7)为使该反应的反应速率增大,且平衡向正反应方向移动的是( )
A、及时分离出SO3气体 B、适当升高温度
C、增大O2的浓度 D、选择高效的催化剂
(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值

(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是
(4)据图判断,反应进行至20min时,曲线发生变化的原因是
(5)10min到15min的曲线变化的原因可能是
A、加了催化剂 B、缩小容器体积
C、降低温度 D、增加SO3的物质的量。
(6)若该反应的密闭容器为2L,则反应15min时,v(SO2)=
(7)为使该反应的反应速率增大,且平衡向正反应方向移动的是
A、及时分离出SO3气体 B、适当升高温度
C、增大O2的浓度 D、选择高效的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】合成氨对人类的生存和发展有着重要意义,至今有三位科学家因在该领域的研究获诺贝尔奖。
合成氨反应为: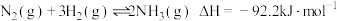 。请回答下列问题:
。请回答下列问题:
(1)该反应的化学平衡常数表达式
_______ 。
(2)某温度下,将 和
和 按一定比例充入
按一定比例充入 恒容容器中,平衡后测得数据如下表:
恒容容器中,平衡后测得数据如下表:
①此条件下 的平衡转化率=
的平衡转化率=_______ 。(保留一位小数)
②若平衡后,再向平衡体系中加入 和
和 各
各 ,此时反应向方向
,此时反应向方向_______ (填“正反应”或“逆反应”)进行,结合计算说明理由:_______ 。
(3)任写一条理论上能提高氨的平衡产率的措施_______ 。
合成氨反应为:
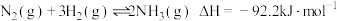 。请回答下列问题:
。请回答下列问题:(1)该反应的化学平衡常数表达式

(2)某温度下,将
 和
和 按一定比例充入
按一定比例充入 恒容容器中,平衡后测得数据如下表:
恒容容器中,平衡后测得数据如下表: |  |  | |
平衡时各物质的物质的量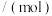 | 1.00 | 3.00 | 1.00 |
 的平衡转化率=
的平衡转化率=②若平衡后,再向平衡体系中加入
 和
和 各
各 ,此时反应向方向
,此时反应向方向(3)任写一条理论上能提高氨的平衡产率的措施
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氢气在工业合成中应用广泛,可用反应CO(g)+2H2(g)⇌CH3OH(g) ΔH<0 来制备甲醇,在容积不变的密闭容器中,当c(CO)=1.0mol/L、c(H2)=1.4 mol/L开始反应,结果如图所示,回答下列问题:
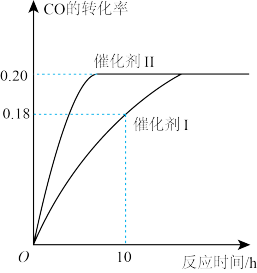
(1)使用催化剂Ⅰ时,在10小时内的平均速率v (H2) =___________ 。
(2)根据图中数据,计算此反应的平衡常数K1 =___________ 。(写出表达式,并代入数据,算出结果)
(3)反应 CO(g)+H2(g)⇌
CO(g)+H2(g)⇌ CH3OH(g)的平衡常数为K2,则K2与K1的关系是
CH3OH(g)的平衡常数为K2,则K2与K1的关系是___________ 。
(4)下列叙述正确的是___________ (填序号) 。
A.充入氩气增大压强有利于提高CO的转化率 B.升高温度有利于提高CO的转化率
C.当容器内气体的密度不再改变时,反应达到平衡D.催化剂Ⅱ的催化效率比催化剂Ⅰ高

(1)使用催化剂Ⅰ时,在10小时内的平均速率v (H2) =
(2)根据图中数据,计算此反应的平衡常数K1 =
(3)反应
 CO(g)+H2(g)⇌
CO(g)+H2(g)⇌ CH3OH(g)的平衡常数为K2,则K2与K1的关系是
CH3OH(g)的平衡常数为K2,则K2与K1的关系是(4)下列叙述正确的是
A.充入氩气增大压强有利于提高CO的转化率 B.升高温度有利于提高CO的转化率
C.当容器内气体的密度不再改变时,反应达到平衡D.催化剂Ⅱ的催化效率比催化剂Ⅰ高
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
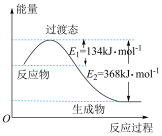
(1)如图所示是 与CO反应生成
与CO反应生成 和NO过程中能量变化示意图,请写出
和NO过程中能量变化示意图,请写出 与CO反应的热化学方程式:
与CO反应的热化学方程式:_______ 。
(2)在2L的密闭绝热容器内,发生反应: ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,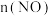 随时间的变化如表:
随时间的变化如表:
①反应开始至第2s时,NO的平均反应速率为_______ 。
②在第5s时, 的转化率为
的转化率为_______ 。
③下列能说明反应已达平衡的是_______ (填字母)。
a.单位时间内,每生成一定物质的量浓度的NO,同时有相同物质的量浓度的 生成
生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气体的密度不再改变
(1)如图所示是
 与CO反应生成
与CO反应生成 和NO过程中能量变化示意图,请写出
和NO过程中能量变化示意图,请写出 与CO反应的热化学方程式:
与CO反应的热化学方程式:
(2)在2L的密闭绝热容器内,发生反应:
 ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,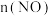 随时间的变化如表:
随时间的变化如表:| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.012 | 0.008 | 0.005 | 0.004 | 0.004 |
②在第5s时,
 的转化率为
的转化率为③下列能说明反应已达平衡的是
a.单位时间内,每生成一定物质的量浓度的NO,同时有相同物质的量浓度的
 生成
生成b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气体的密度不再改变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g)  pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)= v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有
mol,有 molD生成。回答下列问题:
molD生成。回答下列问题:
(1)反应2min内,v(A)=______________ ;v(B)=______________ ;
(2)下列叙述能说明该反应已达平衡状态的是:______ ;
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(3)反应平衡时,D为2amol,则B的转化率为________ ;
(4)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率_____ (是“增大”“减小”或“不变”),
 pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)= v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有
mol,有 molD生成。回答下列问题:
molD生成。回答下列问题:(1)反应2min内,v(A)=
(2)下列叙述能说明该反应已达平衡状态的是:
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(3)反应平衡时,D为2amol,则B的转化率为
(4)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率
您最近一年使用:0次





