纯碱在生产、生活中有广泛应用。例如可用足量的纯碱溶液吸收含氯气的尾气,生成三种盐(反应1);工业上从海水中提取溴的流程中也用到了纯碱溶液,其主要原理如下:反应2: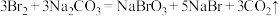 。下列说法正确的是
。下列说法正确的是
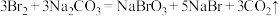 。下列说法正确的是
。下列说法正确的是| A.反应2中氧化产物与还原产物的质量之比为1∶5 |
| B.标准状况下,22.4L溴单质中含有2mol溴原子 |
| C.反应1中生成的三种盐是NaClO,NaClO3和NaHCO3 |
| D.反应2中的Br2与反应1中的Cl2表现出了相似的化学性质 |
更新时间:2022/10/02 17:20:05
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】设NA为阿伏加 德罗常数的值。下列说法正确的是
| A.2.24 L(标准状况)Br2含有的溴分子数为0.1NA |
| B.2.8 g由NaHCO3和MgCO3组成的混合物中含有的氧原子数为0.1NA |
| C.0.1 mol FeCl3·6H2O加入沸水中生成胶体的粒子数为0.1NA |
| D.在加热的条件下,6.4 g Cu与足量的浓硫酸充分反应生成SO2的分子数为0.1NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏加德罗常数的值,下列判断正确的是
| A.标准状况下,22.4LCl2通入足量NaOH溶液中,完全反应时转移的电子数为2NA |
| B.标准状况下,22.4LH2O中含有的分子数目为NA |
| C.1L0.1mol•L-1 NH4NO3溶液中的氮原子数为0.2NA |
| D.20gD2O含有的电子数为10NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业制备高铁酸钾(K2FeO4)的离子方程式为:2Fe(OH)3+3ClO-+4OH- 2FeO
2FeO +3Cl-+5H2O。关于该反应的说法正确的是
+3Cl-+5H2O。关于该反应的说法正确的是
 2FeO
2FeO +3Cl-+5H2O。关于该反应的说法正确的是
+3Cl-+5H2O。关于该反应的说法正确的是A.FeO 中铁显+3价 中铁显+3价 | B.ClO-发生还原反应 |
| C.Fe(OH)3是氧化剂 | D.1mol ClO-参与反应得到2mol电子 |
您最近一年使用:0次
【推荐2】在常温下,发生下列几种反应:
①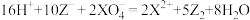
②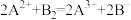
③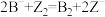
根据上述反应,下列结论判断错误的是
①
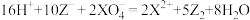
②
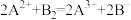
③
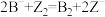
根据上述反应,下列结论判断错误的是
A.溶液中可发生反应: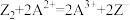 |
| B.Z元素在①、③反应中都被氧化 |
C.氧化性强弱的顺序为: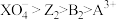 |
D.反应①中, 是 是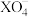 的氧化产物 的氧化产物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】酸性条件下,利用T·F菌可实现天然气脱硫,其原理如下图所示。下列说法中,正确的是
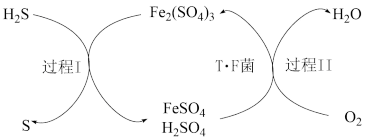

| A.在图示转化关系中,化合价发生变化的元素只有硫和氧 |
B. 可以在转化过程中循环使用 可以在转化过程中循环使用 |
C.在图示转化关系中,氧化性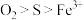 |
D.每消耗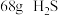 ,标准状况下将有 ,标准状况下将有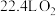 得到电子 得到电子 |
您最近一年使用:0次
【推荐2】反应3BrF3+5H2O=9HF+Br2+HBrO3+O2↑,下列说法中正确的是
| A.BrF3仅作氧化剂,H2O仅作还原剂 |
| B.还原剂与氧化剂的物质的量之比为3:2 |
| C.若生成3.2g O2,则反应中转移电子的物质的量为0.4mol |
| D.若有15mol H2O参加反应,被水还原的BrF3的物质的量为4mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下,下列说法错误的是

A.还原工序逸出的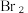 可用NaOH溶液吸收,吸收液可直接返回还原工序 可用NaOH溶液吸收,吸收液可直接返回还原工序 |
| B.除杂工序中产生的滤渣可用二硫化碳进行组分分离 |
C.中和工序中的化学反应为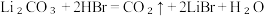 |
D.参与反应的 的物质的量之比为1∶1∶2 的物质的量之比为1∶1∶2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】如图表示铁与不同浓度硝酸反应时,硝酸还原产物中各物质的物质的量百分数与硝酸溶液浓度的关系,下列说法不正确的是
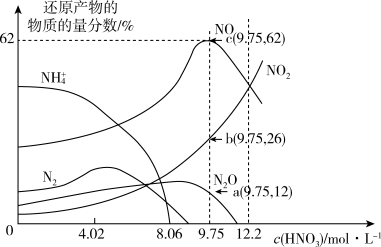

| A.一般来说,不同浓度硝酸与铁反应的还原产物不是单一的 |
B.当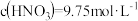 、反应生成2.24L气体(标况下)时,参加反应的硝酸的物质的量为0.112mol 、反应生成2.24L气体(标况下)时,参加反应的硝酸的物质的量为0.112mol |
C. 与 与 反应分别生成等物质的量的 反应分别生成等物质的量的 和 和 时,转移电子的数目之比为1∶2 时,转移电子的数目之比为1∶2 |
D.当硝酸浓度为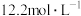 时,反应的化学方程式为 时,反应的化学方程式为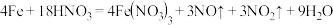 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】由铁及其化合物可制得铁红(Fe2O3)、氯化铁、绿矾(FeSO4•7H2O)、高铁酸钾(K2FeO4)、铁黄(FeOOH)等物质。高铁酸钾是一种既能杀菌、消毒,又能絮凝净水的水处理剂,能与水反应生成氢氧化铁和氧气。铁黄可用作生产磁性材料、颜料的原料。工业制备K2FeO4的离子方程式为Fe(OH)3+ClO−+OH−→FeO +Cl−+H2O(未配平)。下列有关说法
+Cl−+H2O(未配平)。下列有关说法不正确 的是
 +Cl−+H2O(未配平)。下列有关说法
+Cl−+H2O(未配平)。下列有关说法| A.K2FeO4中Fe显+6价 |
B.FeO 的氧化性大于ClO− 的氧化性大于ClO− |
| C.上述反应中氧化剂和还原剂的物质的量之比为3∶2 |
| D.每1molK2FeO4与水反应,产生0.5molO2 |
您最近一年使用:0次

 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是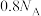
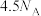

 能够与硫酸酸化的
能够与硫酸酸化的 溶液反应,反应方程式如下:
溶液反应,反应方程式如下: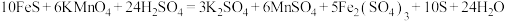 ;关于该反应的下列说法不正确的是
;关于该反应的下列说法不正确的是

