含碳元素的物质是化学世界中最庞大的家族,请填写下列空格。
(1)CH4中的化学键从形成过程来看,属于_______ (填“σ”或“π”)键,从其极性来看属于_______ 键。
(2)CO2和CH3OH分子中C原子的杂化形式分别为_______ 和_______ 。
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为 ,每个COCl2分子内含有的σ键、π键数目为_______。
,每个COCl2分子内含有的σ键、π键数目为_______。
(4)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
甲:
_______ ;乙:
_______ 。
(1)CH4中的化学键从形成过程来看,属于
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为
 ,每个COCl2分子内含有的σ键、π键数目为_______。
,每个COCl2分子内含有的σ键、π键数目为_______。| A.4个σ键 | B.2个σ键、2个π键 | C.2个σ键、1个π键 | D.3个σ键、1个π键 |
甲:


更新时间:2022/12/05 21:06:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知CN-与N2结构相似,CH3CN分子中σ键与π键数目之比为________________ ,碳原子杂化方式______________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下列物质中,以极性键结合的______ ,以非极性键结合的______
(1)F2 (2)O2 (3)NH3 (4)CH4 (5)SO2
(1)F2 (2)O2 (3)NH3 (4)CH4 (5)SO2
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图表示不同类型共价键形成时电子云重叠情况:
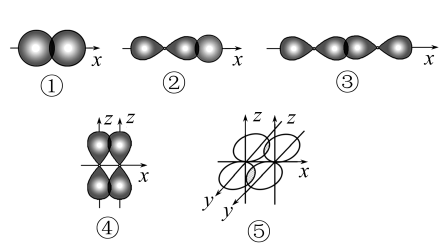
(1)其中形成的化学键属于镜面对称的有______ 。
(2)下列物质中,通过方式①化学键形成的是______ (填选项,下同);通过方式②化学键形成的是______ ;只通过方式③化学键形成的是_______ ;同时含有③、④、⑤三种方式化学键的物质是______ 。
A.Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如图:
甲: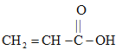 乙:CH2=CH2丙:CH2=CHCN
乙:CH2=CH2丙:CH2=CHCN
①甲分子中有______ 个σ键,______ 个π键。
②乙分子中______ (填“有”或“没有”)极性键,是______ 。(填“极性分子“”或“非极性分子”)
③丙分子中σ键与π键的数目之比为______ 。

(1)其中形成的化学键属于镜面对称的有
(2)下列物质中,通过方式①化学键形成的是
A.Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如图:
甲:
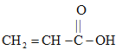 乙:CH2=CH2丙:CH2=CHCN
乙:CH2=CH2丙:CH2=CHCN①甲分子中有
②乙分子中
③丙分子中σ键与π键的数目之比为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请回答下列问题:
(1)Li+半径小于H-,请解释原因________________ 。
(2)有机物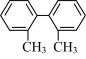 中,同一平面的碳原子数至少为
中,同一平面的碳原子数至少为_____________ 个。
(3)白磷的分子结构为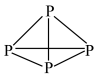 ,分子中磷原子与共价键数目之比为
,分子中磷原子与共价键数目之比为_____________________ 。
(1)Li+半径小于H-,请解释原因
(2)有机物
 中,同一平面的碳原子数至少为
中,同一平面的碳原子数至少为(3)白磷的分子结构为
 ,分子中磷原子与共价键数目之比为
,分子中磷原子与共价键数目之比为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
(1)钒在元素周期表中的位置为第_______ 周期第_______ 族。
(2)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是_______ 对,分子的立体构型为_______ ;SO3气态为单分子,该分子中S原子的杂化轨道类型为_______ ;
(3)杀虫剂Na3AsO4中阴离子的空间构型为_______ ,As原子采取_______ 杂化。
(1)钒在元素周期表中的位置为第
(2)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是
(3)杀虫剂Na3AsO4中阴离子的空间构型为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】臭氧 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ ; 的空间结构为
的空间结构为_______ 。
(2) 分子中
分子中 键与
键与 键的数目之比
键的数目之比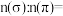
_______ 。
 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间结构为
的空间结构为(2)
 分子中
分子中 键与
键与 键的数目之比
键的数目之比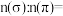
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在氧化硅表面生长高质量六方氮化硼薄膜。回答下面问题:
(1)写出硼的元素符号______ ,其在元素周期表的位置为______ 。
(2)基态O原子的核外电子空间运动状态有______ 种,第二周期主族元素中,第一电离能比O元素大的有______ 种,电负性比O元素大的有______ 。
(3)写出基态Si原子的电子排布式______ ,其单电子数有______ 个。已知H的电负性大于Si,则在硅烷( )中H元素的化合价是
)中H元素的化合价是______ ,中心原子Si的杂化类型是______ 。硅烷分子的空间构型是______ 。
(4)将铬(Cr)原子填充在 ,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
,空隙中,形成常用的催化剂。元素Cr在周期表中的位置______ ,属于______ 区,其基态原子的价层电子排布式为______ 。
(1)写出硼的元素符号
(2)基态O原子的核外电子空间运动状态有
(3)写出基态Si原子的电子排布式
 )中H元素的化合价是
)中H元素的化合价是(4)将铬(Cr)原子填充在
 ,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
您最近半年使用:0次
【推荐1】有下列五种物质:
① ②
② ③CH3OH④CH3COOH⑤
③CH3OH④CH3COOH⑤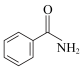
回答问题(1)~(4):
(1)①中碳原子杂化方式分别是_____ 。②中官能团名称是_____ 。
(2)写出②转化成丙烯的化学方程式_____ 。
(3)写出③与④反应的化学方程式_____ 。
(4)⑤在氢氧化钠溶液中反应的化学方程式是_____ 。
(5)下列三组物质能用酸性高锰酸钾溶液鉴别的一组物质是_____ (填字母序号)。
a.乙烯和乙炔 b.乙烯和乙烷 c.苯和环己烷
(6)普伐他汀是一种调节血脂的药物,其结构如图所示。下列关于普伐他汀的性质描述正确的是_____ (填字母序号)。
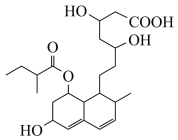
a.该物质能与Na、NaHCO3发生反应
b.能与FeCl3溶液发生显色反应
c.能发生加成、取代、消去反应
d.1mol该物质最多可与1molNaOH反应
①
 ②
② ③CH3OH④CH3COOH⑤
③CH3OH④CH3COOH⑤
回答问题(1)~(4):
(1)①中碳原子杂化方式分别是
(2)写出②转化成丙烯的化学方程式
(3)写出③与④反应的化学方程式
(4)⑤在氢氧化钠溶液中反应的化学方程式是
(5)下列三组物质能用酸性高锰酸钾溶液鉴别的一组物质是
a.乙烯和乙炔 b.乙烯和乙烷 c.苯和环己烷
(6)普伐他汀是一种调节血脂的药物,其结构如图所示。下列关于普伐他汀的性质描述正确的是

a.该物质能与Na、NaHCO3发生反应
b.能与FeCl3溶液发生显色反应
c.能发生加成、取代、消去反应
d.1mol该物质最多可与1molNaOH反应
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】臭氧 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ ; 的空间结构为
的空间结构为_______ 。
(2) 分子中
分子中 键与
键与 键的数目之比
键的数目之比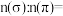
_______ 。
 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间结构为
的空间结构为(2)
 分子中
分子中 键与
键与 键的数目之比
键的数目之比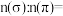
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空:
I.指出下列分子或离子的中心原子的杂化轨道类型及分子的空间结构
(1)SiF4:_______ 杂化,空间结构_______ ;
(2) :
:_______ 杂化,空间结构_______ ;
(3) :
:_______ 杂化,空间结构_______ ;
(4)CS2:_______ 杂化,空间结构_______ ;
II.
(5)O、S、Se为同主族元素, 和
和 的相对分子质量相等,常温下,
的相对分子质量相等,常温下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是_______ ;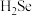 分子的中心原子杂化类型为
分子的中心原子杂化类型为_______ 杂化;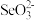 的空间构型为
的空间构型为_______ 。
I.指出下列分子或离子的中心原子的杂化轨道类型及分子的空间结构
(1)SiF4:
(2)
 :
:(3)
 :
:(4)CS2:
II.
(5)O、S、Se为同主族元素,
 和
和 的相对分子质量相等,常温下,
的相对分子质量相等,常温下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是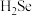 分子的中心原子杂化类型为
分子的中心原子杂化类型为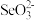 的空间构型为
的空间构型为
您最近半年使用:0次

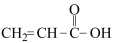 乙:COCl2(
乙:COCl2(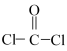 )
)
 键,
键, 键,
键,

