二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
实验室利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。
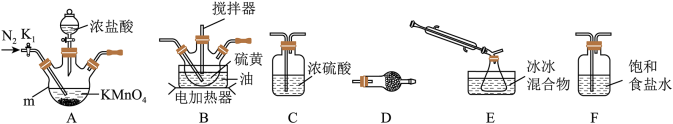
①仪器m的名称为_____ ,装置F中试剂的作用是_____ 。
②装置连接顺序:A→_____ →D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是_____ 。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和_____ 。
(2)S2Cl2遇水强烈反应产生烟雾,其产物中有一种气体X能使品红溶液褪色,加热后又恢复原状,且反应过程中只有一种元素化合价发生变化,写出该反应的化学方程式_____ 。
(3)某同学为了测定S2Cl2与水反应后生成的气体X在混合气体中的体积分数,设计了如图实验方案:

①W溶液可以是_____ (填标号)。
a.H2O2溶液 b.酸性KMnO4溶液 c.氯水
②该混合气体中气体X的体积分数为_____ (用含V、m的式子表示)。
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解; ②S2Cl2+Cl2  2SCl2; 2SCl2;③遇高热或与明火接触,有引起燃烧的危险; ④受热或遇水分解放热,放出腐蚀性烟气; | ||||
实验室利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。

①仪器m的名称为
②装置连接顺序:A→
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
④为了提高S2Cl2的纯度,实验的关键是控制好温度和
(2)S2Cl2遇水强烈反应产生烟雾,其产物中有一种气体X能使品红溶液褪色,加热后又恢复原状,且反应过程中只有一种元素化合价发生变化,写出该反应的化学方程式
(3)某同学为了测定S2Cl2与水反应后生成的气体X在混合气体中的体积分数,设计了如图实验方案:

①W溶液可以是
a.H2O2溶液 b.酸性KMnO4溶液 c.氯水
②该混合气体中气体X的体积分数为
更新时间:2022-12-20 16:40:08
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】血液中的钙离子平衡在临床医学中具有重要的意义。某研究小组为测定血液样品中Ca2+的含量,进行的实验如下:
①量取5.0mL血液样品,处理后配制成100mL溶液;
②量取10.0mL溶液,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4(弱酸)和CaSO4稀溶液;
④加入0.001 mol·L-1的酸性KMnO4溶液,使H2C2O4完全氧化,同时产生使澄清石灰水变浑浊的无色无味气体,同时生成Mn2+,消耗酸性KMnO4溶液的体积为2.00 mL。
(1)步骤①中用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、___________ 。
(2)步骤④中发生反应的离子方程式为___________ 。
(3)血样中Ca2+的含量为___________ mg·L-1(写出计算过程,否则不得分)
①量取5.0mL血液样品,处理后配制成100mL溶液;
②量取10.0mL溶液,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4(弱酸)和CaSO4稀溶液;
④加入0.001 mol·L-1的酸性KMnO4溶液,使H2C2O4完全氧化,同时产生使澄清石灰水变浑浊的无色无味气体,同时生成Mn2+,消耗酸性KMnO4溶液的体积为2.00 mL。
(1)步骤①中用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、
(2)步骤④中发生反应的离子方程式为
(3)血样中Ca2+的含量为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】某兴趣小组对化合物X开展探究实验。

其中:X由5种短周期主族元素组成;B在标况下的密度为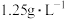 ;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
请回答:
(1)组成X的元素除了Na、O外还有_______ (填元素符号),X的化学式是_______ 。
(2)X与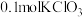 发生的反应的化学方程式是
发生的反应的化学方程式是_______ 。
(3)少量C与足量 反应也产生G,该反应的离子方程式是
反应也产生G,该反应的离子方程式是_______ 。
(4) ,F、H的阴离子相同,反应后所得溶液呈酸性,原因是
,F、H的阴离子相同,反应后所得溶液呈酸性,原因是_______ 。
(5)已知C与A加热可制备得到一种气体,请设计实验探究该气体的组成:_______ (已知该气体只有两种元素组成)。

其中:X由5种短周期主族元素组成;B在标况下的密度为
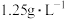 ;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)请回答:
(1)组成X的元素除了Na、O外还有
(2)X与
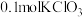 发生的反应的化学方程式是
发生的反应的化学方程式是(3)少量C与足量
 反应也产生G,该反应的离子方程式是
反应也产生G,该反应的离子方程式是(4)
 ,F、H的阴离子相同,反应后所得溶液呈酸性,原因是
,F、H的阴离子相同,反应后所得溶液呈酸性,原因是(5)已知C与A加热可制备得到一种气体,请设计实验探究该气体的组成:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】I.中学化学常见物质A、B、C、D、X、Y,存在如下图转化关系(部分物质和条件略去)。
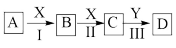
①若A为NaOH溶液,X为CO2,D是沉淀,则Y可为___________ 。(填序号)。
A.SO3B.Ba(OH)2C.H2SO4D.CaO
②若A为碱性气体,X为O2,A与D反应生成一种化肥,则反应Ⅲ的化学方程式为___________ 。
II.氨氮废水的处理流程如图所示:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加NaOH溶液时所发生的反应:___________ 。
②过程Ⅱ:在微生物的作用、碱性条件下NH 被氧化成NO
被氧化成NO 的离子方程式为:
的离子方程式为:___________ 。
III.金属可用于还原废水中的Cr(Ⅵ)。
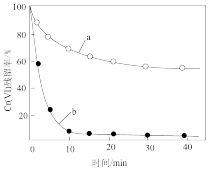
(1)其他条件相同时,用相同物质的量的Zn粉、Zn-Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是___________ (用文字说明)。
(2)用氧化铁包裹的纳米铁粉(用Fe/Fe2O3表示)能有效还原水溶液中的Cr(Ⅵ)。Fe/Fe2O3还原近中性废水中Cr(Ⅵ)的可能反应机理如图所示。Fe/Fe2O3中Fe还原CrO 的过程为:
的过程为:
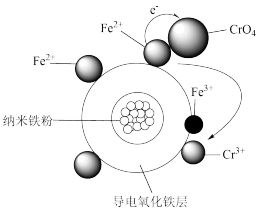
①单质铁发生吸氧腐蚀,铁的电极反应式为___________
②CrO 被还原的离子方程式
被还原的离子方程式___________
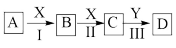
①若A为NaOH溶液,X为CO2,D是沉淀,则Y可为
A.SO3B.Ba(OH)2C.H2SO4D.CaO
②若A为碱性气体,X为O2,A与D反应生成一种化肥,则反应Ⅲ的化学方程式为
II.氨氮废水的处理流程如图所示:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加NaOH溶液时所发生的反应:
②过程Ⅱ:在微生物的作用、碱性条件下NH
 被氧化成NO
被氧化成NO 的离子方程式为:
的离子方程式为:III.金属可用于还原废水中的Cr(Ⅵ)。
(1)其他条件相同时,用相同物质的量的Zn粉、Zn-Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是

(2)用氧化铁包裹的纳米铁粉(用Fe/Fe2O3表示)能有效还原水溶液中的Cr(Ⅵ)。Fe/Fe2O3还原近中性废水中Cr(Ⅵ)的可能反应机理如图所示。Fe/Fe2O3中Fe还原CrO
 的过程为:
的过程为:
①单质铁发生吸氧腐蚀,铁的电极反应式为
②CrO
 被还原的离子方程式
被还原的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.硫元素在人类生命活动以及生产生活中均发挥了重要作用,常见的硫磺皂、二硫化硒洗发水、葡萄酒中都有硫元素的身影。人类对硫元素的探索也在历史上留下了浓墨重彩的一笔,例如黑火药的发明、“绿矾油”的提炼……
(1)硫磺皂的主要成分是脂肪酸钠、硫单质,硫磺皂是最便宜的除螨杀菌药皂。请猜测硫磺皂的颜色___________ ,写出硫离子的电子式___________ 。
(2)下列各反应中,能证明氯气的氧化性比硫的氧化性强的反应是________
①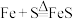

②
③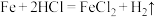
 跟浓
跟浓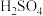 常温下发生钝化
常温下发生钝化
(3)在酿酒时人工添加 有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入
有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入 ,请用化学方程式表示该反应机理
,请用化学方程式表示该反应机理___________ 。
(4)发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总 小于
小于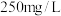 ,若在室温下,每升溶液中最多通入
,若在室温下,每升溶液中最多通入___________  。(室温下
。(室温下 )
)
(5)向 溶液中通入
溶液中通入 至饱和,此过程看不到现象,再向溶液中加入一种物质,溶液变浑浊,加入的这种物质不可能是_________
至饱和,此过程看不到现象,再向溶液中加入一种物质,溶液变浑浊,加入的这种物质不可能是_________
(6)在古代中国,稀硫酸被称为“绿矾油”。关于浓硫酸和稀硫酸的说法,错误的是_______
(7)常温下,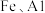 在浓硫酸中钝化,浓硫酸表现了______
在浓硫酸中钝化,浓硫酸表现了______
Ⅱ.某校化学兴趣小组同学取锌粒与浓 充分反应制取
充分反应制取 气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。
气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。
为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。
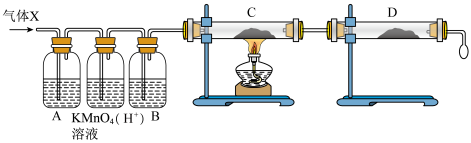
(8)杂质气体可能是___________ ,酸性 溶液的作用
溶液的作用___________ ;B中添加的试剂是___________ 。
(9)装置C中所装药品为___________ ,D中所装药品为___________ ,可证实气体X中混有较多量某杂质气体的实验现象是___________ 。
(1)硫磺皂的主要成分是脂肪酸钠、硫单质,硫磺皂是最便宜的除螨杀菌药皂。请猜测硫磺皂的颜色
(2)下列各反应中,能证明氯气的氧化性比硫的氧化性强的反应是________
①
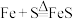

②

③
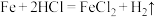
 跟浓
跟浓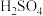 常温下发生钝化
常温下发生钝化| A.只有① | B.只有② | C.①② | D.①②③ |
(3)在酿酒时人工添加
 有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入
有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入 ,请用化学方程式表示该反应机理
,请用化学方程式表示该反应机理(4)发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总
 小于
小于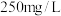 ,若在室温下,每升溶液中最多通入
,若在室温下,每升溶液中最多通入 。(室温下
。(室温下 )
)(5)向
 溶液中通入
溶液中通入 至饱和,此过程看不到现象,再向溶液中加入一种物质,溶液变浑浊,加入的这种物质不可能是_________
至饱和,此过程看不到现象,再向溶液中加入一种物质,溶液变浑浊,加入的这种物质不可能是_________A. | B. | C. | D. |
(6)在古代中国,稀硫酸被称为“绿矾油”。关于浓硫酸和稀硫酸的说法,错误的是_______
A.都有 分子 分子 | B.都有氧化性 |
| C.都能和铁、铝反应 | D.密度都比水大 |
(7)常温下,
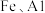 在浓硫酸中钝化,浓硫酸表现了______
在浓硫酸中钝化,浓硫酸表现了______| A.难挥发性 | B.吸水性 | C.脱水性 | D.强氧化性 |
Ⅱ.某校化学兴趣小组同学取锌粒与浓
 充分反应制取
充分反应制取 气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。
气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。

(8)杂质气体可能是
 溶液的作用
溶液的作用(9)装置C中所装药品为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】为测定某地空气中SO2和可吸入颗粒的含量,某同学设计了如下图所示的实验装置:

注:气体流速管是用来测量单位时间内通过气体体积的装置
(1)上述实验测定原理为_________________________________ (用化学方程式表示)。
(2)应用上述装置测定空气中SO2和可吸入颗粒的含量,除需测定气体流速(单位:mL·s-1)外,还需要测定碘溶液蓝色褪去所需的时间和___________________________ 。
(3)已知:碘单质微溶于水,KI可以增大碘在水中溶解度。为精确配制100 mL 5.0×10-4mol·L-1的碘溶液,先要配制1000 mL 1.0×10-2mol·L-1碘溶液,再取5.00 mL溶液稀释成为5.0×10-4mol·L-1碘溶液。
①第一步:用托盘天平称取___ g 碘单质加入烧杯中,同时加入少量碘化钾固体,加适量水搅拌使之完全溶解。
②第二步:________________ ,洗涤、定容、摇匀。
③第三步:用第二步所得溶液配制5.0×10-4mol·L-1碘溶液,此步操作中,除烧杯、玻璃棒、胶头滴管外还需要的玻璃仪器有________________________ 。
(4)空气中SO2含量的测定:
①已知空气中二氧化硫的最大允许排放浓度不得超过0.02mg·L-1,在指定的地点取样,以200mL·s-1气体流速通过气体流速管通入到上图实验装置中,观察记录碘溶液褪色所需时间为500s,则该地空气中的SO2含量是________ mg·L-1,____________ (填“符合”、“不符合”)排放标准。
②如果甲同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,其原因可能是________________________________ (假设溶液配制、称量或量取及各种读数均无错误。写出一种可能原因即可)

注:气体流速管是用来测量单位时间内通过气体体积的装置
(1)上述实验测定原理为
(2)应用上述装置测定空气中SO2和可吸入颗粒的含量,除需测定气体流速(单位:mL·s-1)外,还需要测定碘溶液蓝色褪去所需的时间和
(3)已知:碘单质微溶于水,KI可以增大碘在水中溶解度。为精确配制100 mL 5.0×10-4mol·L-1的碘溶液,先要配制1000 mL 1.0×10-2mol·L-1碘溶液,再取5.00 mL溶液稀释成为5.0×10-4mol·L-1碘溶液。
①第一步:用托盘天平称取
②第二步:
③第三步:用第二步所得溶液配制5.0×10-4mol·L-1碘溶液,此步操作中,除烧杯、玻璃棒、胶头滴管外还需要的玻璃仪器有
(4)空气中SO2含量的测定:
①已知空气中二氧化硫的最大允许排放浓度不得超过0.02mg·L-1,在指定的地点取样,以200mL·s-1气体流速通过气体流速管通入到上图实验装置中,观察记录碘溶液褪色所需时间为500s,则该地空气中的SO2含量是
②如果甲同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,其原因可能是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】在铜冶炼过程中,产生的铜阳极泥富含金、银、硒、碲等。苏打熔炼法是一种从铜阳极泥中回收硒与碲的方法,且贵金属回收率高,工艺流程如图所示:

已知:①铜阳极泥中的铜主要以铜单质和硫化铜形态存在。
② 是白色固体,易溶于水且与水反应,
是白色固体,易溶于水且与水反应,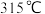 升华。
升华。
③ 是两性氧化物,微溶于水,易溶于强酸和强碱。
是两性氧化物,微溶于水,易溶于强酸和强碱。
(1)阳极泥在煅烧前进行粉碎的目的是_____ ,“煅烧”时阳极泥需在双层炉内氧化焙烧 ,其目的是
,其目的是_____ 。
(2)烟气中主要成分是 ,还原沉硒过程中发生反应的化学方程式为
,还原沉硒过程中发生反应的化学方程式为_____ 。
(3)向“水浸”后的溶液中加硫酸调 ,当
,当 为
为 时可沉出
时可沉出 ,此步骤要缓慢加入硫酸并不断搅拌的目的是
,此步骤要缓慢加入硫酸并不断搅拌的目的是_____ 。
(4) 经
经 溶液碱溶、电解得碲,碱溶时发生反应的离子方程式为
溶液碱溶、电解得碲,碱溶时发生反应的离子方程式为_____ 。
(5)情性电极电解制备碲的阴极电极反应式为_____ 。
(6)若电解法回收铜和碲均使用惰性电极,则可回收再利用的物质是_____ (写名称)。

已知:①铜阳极泥中的铜主要以铜单质和硫化铜形态存在。
②
 是白色固体,易溶于水且与水反应,
是白色固体,易溶于水且与水反应,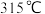 升华。
升华。③
 是两性氧化物,微溶于水,易溶于强酸和强碱。
是两性氧化物,微溶于水,易溶于强酸和强碱。(1)阳极泥在煅烧前进行粉碎的目的是
 ,其目的是
,其目的是(2)烟气中主要成分是
 ,还原沉硒过程中发生反应的化学方程式为
,还原沉硒过程中发生反应的化学方程式为(3)向“水浸”后的溶液中加硫酸调
 ,当
,当 为
为 时可沉出
时可沉出 ,此步骤要缓慢加入硫酸并不断搅拌的目的是
,此步骤要缓慢加入硫酸并不断搅拌的目的是(4)
 经
经 溶液碱溶、电解得碲,碱溶时发生反应的离子方程式为
溶液碱溶、电解得碲,碱溶时发生反应的离子方程式为(5)情性电极电解制备碲的阴极电极反应式为
(6)若电解法回收铜和碲均使用惰性电极,则可回收再利用的物质是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硒(Se)和碲(Te)均为硫(S)的同族元素,原子序数分别为34、52,它们的单质和化合物在电子、冶金、材料等领域有广阔的发展前景。科研小组以精炼铜的阳极泥为原料(含有 、
、 、
、 和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:

回答下列问题:
(1)Cu原子的价电子排布式为_______ ; 属于
属于_______ (填“酸性”“碱性”或“两性”)氧化物。
(2) 的稳定性比
的稳定性比 的
的_______ (填“强”或“弱”); ,
, ,
, 的沸点由高到低为
的沸点由高到低为_______ 。
(3)“水溶”反应的离子方程式为_______ 。
(4)“碱溶”的目的为_______ 。
(5)“分离”过程需控制适当温度,不宜过高或过低的理由为_______ 。
(6)若滤液2的 ,其中
,其中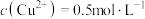 、
、 、
、 ,则滤渣Ⅱ的成分为
,则滤渣Ⅱ的成分为_______ 。[已知 、
、 ]
]
(7)用滤液2制备 的操作为
的操作为_______ 。
 、
、 、
、 和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
回答下列问题:
(1)Cu原子的价电子排布式为
 属于
属于(2)
 的稳定性比
的稳定性比 的
的 ,
, ,
, 的沸点由高到低为
的沸点由高到低为(3)“水溶”反应的离子方程式为
(4)“碱溶”的目的为
(5)“分离”过程需控制适当温度,不宜过高或过低的理由为
(6)若滤液2的
 ,其中
,其中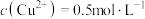 、
、 、
、 ,则滤渣Ⅱ的成分为
,则滤渣Ⅱ的成分为 、
、 ]
](7)用滤液2制备
 的操作为
的操作为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】实验室用如图装置(夹持装置略)制备高效水处理剂高铁酸钾(K2FeO4)并探究其性质。
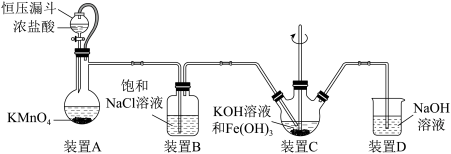
已知K2FeO4具有下列性质:①可溶于水,微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定,在Fe(OH)3或Fe3+催化下发生分解;③在弱碱性至酸性条件下,能与水反应生成O2和Fe(OH)3(或Fe3+)。
(1)装置A用于制取氯气,其中使用恒压漏斗的原因是____ 。
(2)为防止装置C中K2FeO4分解,可以采取的措施是____ 和____ 。
(3)装置C中生成K2FeO4反应的离子方程式为____ 。
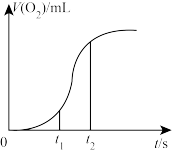
(4)用一定量的K2FeO4处理饮用水,测得产生O2的体积随时间的变化曲线如图所示。t1 s~t2 s内,O2的体积迅速增大的主要原因是____ 。
(5)验证酸性条件下氧化性FeO42->Cl2的实验方案为:取少量K2FeO4固体于试管中,____ 。(实验中须使用的的试剂和用品有:浓盐酸,NaOH溶液、淀粉KI试纸、棉花)
(6)根据K2FeO4的制备实验得出:氧化性Cl2>FeO42-,而第(5)小题实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是____ 。

已知K2FeO4具有下列性质:①可溶于水,微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定,在Fe(OH)3或Fe3+催化下发生分解;③在弱碱性至酸性条件下,能与水反应生成O2和Fe(OH)3(或Fe3+)。
(1)装置A用于制取氯气,其中使用恒压漏斗的原因是
(2)为防止装置C中K2FeO4分解,可以采取的措施是
(3)装置C中生成K2FeO4反应的离子方程式为
(4)用一定量的K2FeO4处理饮用水,测得产生O2的体积随时间的变化曲线如图所示。t1 s~t2 s内,O2的体积迅速增大的主要原因是

(5)验证酸性条件下氧化性FeO42->Cl2的实验方案为:取少量K2FeO4固体于试管中,
(6)根据K2FeO4的制备实验得出:氧化性Cl2>FeO42-,而第(5)小题实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】一氧化二氯(Cl2O)是国际公认的高效安全灭菌消毒剂,其部分性质如下:现用如图所示装置制备少量Cl2O。
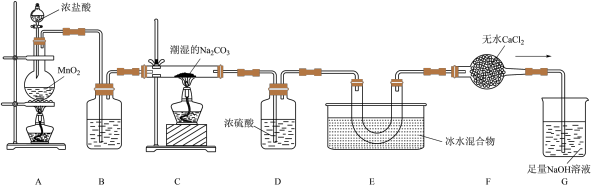
已知:常温下,Cl2O是棕黄色、有刺激性气味的气体,易溶于水;熔点:-120.6℃;沸点2.0℃。
(1)盛有浓盐酸的仪器的名称是_____ 。
(2)装置A中发生反应的离子方程式为______ 。
(3)装置B中的试剂是_____ (填名称)。
(4)装置C中固体产物为NaCl和NaHCO3,写出该反应的化学方程式_____ 。
(5)装置E中Cl2O的收率与装置C的温度和纯碱的含水量的关系如表所示,下列猜想明显不合理的是_____ 。

已知:常温下,Cl2O是棕黄色、有刺激性气味的气体,易溶于水;熔点:-120.6℃;沸点2.0℃。
(1)盛有浓盐酸的仪器的名称是
(2)装置A中发生反应的离子方程式为
(3)装置B中的试剂是
(4)装置C中固体产物为NaCl和NaHCO3,写出该反应的化学方程式
(5)装置E中Cl2O的收率与装置C的温度和纯碱的含水量的关系如表所示,下列猜想明显不合理的是
| 温度/℃ | 纯碱含水量/% | Cl2O收率/% |
| 0~10 | 5.44 | 67.85 |
| 0~10 | 7.88 | 89.26 |
| 10~20 | 8.00 | 64.24 |
| 30~40 | 10.25 | 52.63 |
| 30-40 | 12.50 | 30.38 |
| A.温度越高,Cl2O的收率越低 |
| B.纯碱含水量越高,Cl2O的收率越高 |
| C.随着纯碱含水量增大,Cl2O的收率先增大后减小 |
| D.温度较低时,纯碱含水量越高,Cl2O的收率越高,温度较高时,纯碱含水量越高,Cl2O的收率越低 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】含氯消毒剂给自来水消毒后有余氯Na2S2O3可用于自来水中余氯的测定。测定自来水中余氯含量的方案如下:在250 mL碘量瓶中(或具塞锥形瓶中)放置0.5 g碘化钾,加10 mL稀硫酸,准确量取流动水样100 mL(打开自来水龙头,待水流数十秒后再取水样) 置于碘量瓶,迅速塞上塞摇动,见水样呈淡黄色,加1 mL淀粉溶液变蓝,则说明水样中有余氯。再以cmol·L-1标准Na2S2O3溶液滴定,至溶液蓝色消失呈无色透明溶液,记下消耗硫代硫酸钠溶液的体积。
(已知:滴定时反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6)
(1)若该自来水是以漂白粉消毒,能说明水样中有余氯的反应离子方程式为_______________________________________________________ 。
(2)按上述方案实验,消耗标准Na2S2O3溶液VmL,该次实验测得自来水样品中余氯量(以游离Cl2计算)为________ mg·L-1。在上述实验过程中,若“塞上塞摇动”动作不够迅速,则测得结果________ (填“偏高”、“偏低”或“不变”)。
(已知:滴定时反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6)
(1)若该自来水是以漂白粉消毒,能说明水样中有余氯的反应离子方程式为
(2)按上述方案实验,消耗标准Na2S2O3溶液VmL,该次实验测得自来水样品中余氯量(以游离Cl2计算)为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:
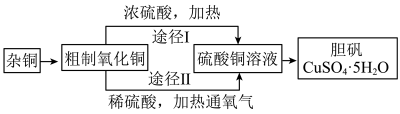
(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于___ 上(用以下所给仪器的编号填入,下同),取用坩埚应使用____ ,灼烧后的坩埚应放在___ 上,不能直接放在桌面上;实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹;
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾,灼烧后含有少量铜的可能原因是____ ;
a.灼烧过程中部分氧化铜被还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)通过途径 II 实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、____ 、冷却结晶、___ 、自然干燥;
(4)由粗制氧化铜通过两种途径制取胆矾,与途径I相比,途径II有明显的两个优点是:____ 、____ ;
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行___ 次;
(6)若测定结果x值偏高, 可能的原因是___ 。
a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却 d.胆矾晶体部分风化

(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾,灼烧后含有少量铜的可能原因是
a.灼烧过程中部分氧化铜被还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)通过途径 II 实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、
(4)由粗制氧化铜通过两种途径制取胆矾,与途径I相比,途径II有明显的两个优点是:
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行
(6)若测定结果x值偏高, 可能的原因是
a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却 d.胆矾晶体部分风化
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D、E、F六种物质有如图变化关系,E是淡黄色粉末,判断:
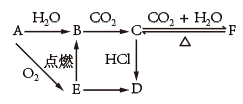
(1)写出A、B、C、D、E、F的化学式:
B._______ ;C._______ ;D._______ ;E._______ ;
(2)写出有关反应的化学方程式(是离子反应的直接写离子方程式)
E→B:_______ ,C→F: _______ ,F→C: _______ 。
(3)下列实验方案中,不能准确测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是_______
A. 取a克混合物充分加热,减重b克
B. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C. 取a克混合物与足量稀硫酸充分反应,逸出气体直接用碱石灰吸收,增重b克
D. 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。

(1)写出A、B、C、D、E、F的化学式:
B.
(2)写出有关反应的化学方程式(是离子反应的直接写离子方程式)
E→B:
(3)下列实验方案中,不能准确测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A. 取a克混合物充分加热,减重b克
B. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C. 取a克混合物与足量稀硫酸充分反应,逸出气体直接用碱石灰吸收,增重b克
D. 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。
您最近一年使用:0次



