2022年9月9日,国家航天局、国家原子能机构联合在北京发布“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族,颗粒约2~30微米,伴生矿物有钛铁矿等。回答下列问题:
(1)基态钛原子价电子排布式为_______ 。
(2)Fe的配合物有多种。 、
、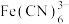 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是_______ (写元素符号,下同);第一电离能由大到小的顺序为_______ 。
(3)磷酸为磷的最高价含氧酸,其空间结构如图:
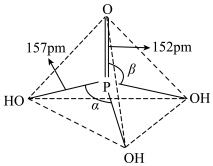
①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
② 的立体构型为
的立体构型为_______ ,中心原子的杂化类型是_______ 。
(4)反型钙钛矿电池无须使用具有光催化活性的 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
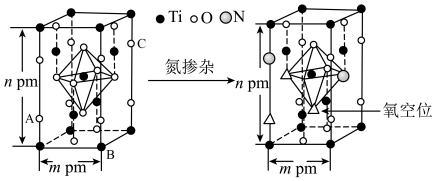
 晶体中
晶体中
_______ ;已知原子A、B的分数坐标分别为 和
和 ,则原子C的坐标为
,则原子C的坐标为_______ ,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为_______ g·cm 。
。
(1)基态钛原子价电子排布式为
(2)Fe的配合物有多种。
 、
、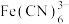 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是(3)磷酸为磷的最高价含氧酸,其空间结构如图:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②
 的立体构型为
的立体构型为(4)反型钙钛矿电池无须使用具有光催化活性的
 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
 晶体中
晶体中
 和
和 ,则原子C的坐标为
,则原子C的坐标为 ,
, 的密度为
的密度为 。
。
22-23高三上·吉林·阶段练习 查看更多[3]
更新时间:2023-01-02 19:29:37
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】ⅢA族与ⅤA族元素及其化合物具有众多优良特性,可用于制作航天器等耐高温设备。回答下列问题。
(1)Al原子中电子占据的最高能层符号为_______ ,第三周期元素中第一电离能介于Al和P有_______ 种
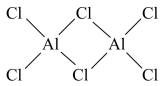
(2)AlCl3在气态时可以发生二聚,其分子式为Al2Cl6,其二聚体结构如图,请在图中以“→”表示该结构中存在的配位键。其中Cl-Al-Cl键角的大小情况是AlCl3_______ Al2Cl6(填“<”、“>”或“=”下同)原因为_______ 。
(3)咪唑结构为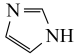 ,N原子的杂化类型为
,N原子的杂化类型为_______ ,分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为_______ 。
(4)噻唑结构与咪唑很相似,结构为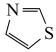 ,噻唑的熔沸点
,噻唑的熔沸点_______ 咪唑,原因是_______ 。
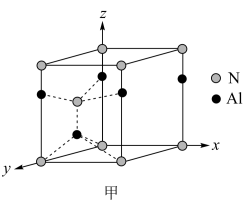
(5)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,其晶胞结构如图甲所示,Al原子位于氮原子形成的_______ 空隙(填“正四面体”或“正八面体”)。已知晶胞的密度为ρ g·cm-3,两种原子半径分别为rN nm和rAl nm,阿伏加德罗常数值为NA,则该晶胞中原子的体积占晶胞体积的百分率为_______ 。(用含ρ、rN 、rAl和NA的代数式表示)
(1)Al原子中电子占据的最高能层符号为
(2)AlCl3在气态时可以发生二聚,其分子式为Al2Cl6,其二聚体结构如图,请在图中以“→”表示该结构中存在的配位键。其中Cl-Al-Cl键角的大小情况是AlCl3

(3)咪唑结构为
 ,N原子的杂化类型为
,N原子的杂化类型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为(4)噻唑结构与咪唑很相似,结构为
 ,噻唑的熔沸点
,噻唑的熔沸点(5)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,其晶胞结构如图甲所示,Al原子位于氮原子形成的

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为______ 。
(2)元素B、C、D第一电离能由大到小的顺序为______ (填元素符号)。
(3)BC 的空间结构为
的空间结构为______ 。
(4)与同族其他元素X形成的XA3相比,BA3易液化的原因是______ 。
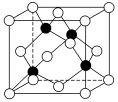
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为apm,则晶体的密度为_____ g·cm-3(用NA表示阿伏加德罗常数的值)。
(1)E的元素名称为
(2)元素B、C、D第一电离能由大到小的顺序为
(3)BC
 的空间结构为
的空间结构为(4)与同族其他元素X形成的XA3相比,BA3易液化的原因是
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为apm,则晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】由第ⅢA和第ⅤA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料,请根据材料回答以下问题:
(1)基态As原子的电子排布式为[Ar]___________ 。N、P、As的第一电离能从大到小的顺序是:___________ 。
(2)除了已知的氮气,科学家还先后研究出了 、
、 、
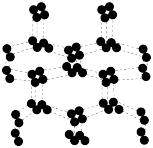
、 、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则
、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则 的沸点
的沸点___________ (填“>”、“<”或“=”)高聚氮的沸点,原因是___________ 。
(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为___________ ,电子重排后的氧原子能量有所升高,原因是不符合___________ (填“泡利原理”或“洪特规则”)。
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是___________ 。
(5) 晶体的晶胞参数为
晶体的晶胞参数为 ,
, ,α=β=90°,
,α=β=90°, =120°,结构如下图:
=120°,结构如下图:
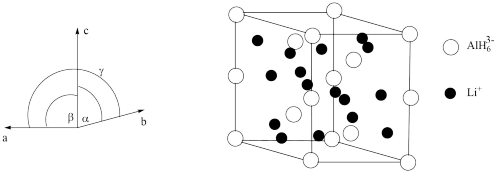
①已知 的分数坐标为(0,0,0)、(0,0,
的分数坐标为(0,0,0)、(0,0, ),(
),( ,
, ,
, ),(
),( ,
, ,
, ),(
),( ,
, ,
, )和 (
)和 ( ,
, ,
, ),晶胞中
),晶胞中 的个数为
的个数为___________ 。
②下图是上述 晶胞的某个截面,共含有10个
晶胞的某个截面,共含有10个 ,其中6个已经画出(图中的○)请在图中用○将剩余的
,其中6个已经画出(图中的○)请在图中用○将剩余的 画出。
画出。___________

③此晶体的密度为___________ g/cm3 (列出计算式即可)。
(1)基态As原子的电子排布式为[Ar]
(2)除了已知的氮气,科学家还先后研究出了
 、
、 、
、 、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则
、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则 的沸点
的沸点
(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是
| 化学键 |  |  |  |
| 键能 (kJ/mol) | 389 | 561 | 293 |
(5)
 晶体的晶胞参数为
晶体的晶胞参数为 ,
, ,α=β=90°,
,α=β=90°, =120°,结构如下图:
=120°,结构如下图:
①已知
 的分数坐标为(0,0,0)、(0,0,
的分数坐标为(0,0,0)、(0,0, ),(
),( ,
, ,
, ),(
),( ,
, ,
, ),(
),( ,
, ,
, )和 (
)和 ( ,
, ,
, ),晶胞中
),晶胞中 的个数为
的个数为②下图是上述
 晶胞的某个截面,共含有10个
晶胞的某个截面,共含有10个 ,其中6个已经画出(图中的○)请在图中用○将剩余的
,其中6个已经画出(图中的○)请在图中用○将剩余的 画出。
画出。
③此晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】氮(N)、磷(P)、砷(As)等VA族元素化合物在研究和生产中有重要用途。如我国科研人员研究发现 As2O3(或写成As4O6,俗称砒霜)对白血病有明显的治疗作用回答下列问题:
(1)As原子的核外电子排布式为____ ;P的第一电离能比S大的原因为____
(2)写出一种与 互为等电子体的粒子
互为等电子体的粒子_ (用化学式表示);(SCN)2分子中 键和
键和 键个数比为
键个数比为___
(3)砒霜剧毒,可用石灰消毒生成 和少量
和少量 ,其中
,其中 中As的杂化方式为
中As的杂化方式为__ , 的空间构型为
的空间构型为___
(4)工业制备铁氧体可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。
比较上表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因____ 。苯胺分子可看做氨分子中一个氢原子被苯基取代,苯胺分子中的离域 键表示为
键表示为____ 。PH3是一种无色剧毒、有类似大蒜臭味的气体,它与NH3互为等电子体,二者分子中的键角关系为
_____ 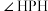 (填“>”或“<”)。
(填“>”或“<”)。
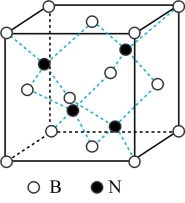
(5)BN的熔点为 ,密度为
,密度为 ,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有
,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有_______ 个;若原子半径分别为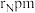 和
和 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则BN晶胞中原子的体积占晶胞体积的百分率为
,则BN晶胞中原子的体积占晶胞体积的百分率为_______ 。
(1)As原子的核外电子排布式为
(2)写出一种与
 互为等电子体的粒子
互为等电子体的粒子 键和
键和 键个数比为
键个数比为(3)砒霜剧毒,可用石灰消毒生成
 和少量
和少量 ,其中
,其中 中As的杂化方式为
中As的杂化方式为 的空间构型为
的空间构型为(4)工业制备铁氧体可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。
| N2H4 | NH3 | |
| 熔点/℃ | 2 | -77.8 |
| 沸点/℃ | 113.5 | -33.5 |
比较上表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因
 键表示为
键表示为
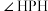 (填“>”或“<”)。
(填“>”或“<”)。 (5)BN的熔点为
 ,密度为
,密度为 ,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有
,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有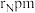 和
和 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则BN晶胞中原子的体积占晶胞体积的百分率为
,则BN晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】我国稀土工艺技术水平世界领先。从离子型稀土矿中(含RE、K、Al、Mg、Si、F等多种铝硅酸盐化合物,RE代表稀土元素)通过阳离子交换法提取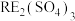 工艺流程如图。
工艺流程如图。
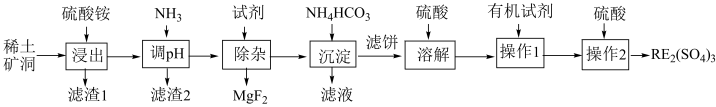
已知:①稀土矿中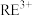 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子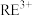
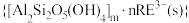 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将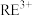 与
与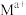 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。
②常温下部分难溶物的溶度积如表:
③pH对稀土和铝浸出率的影响如图:

回答下列问题:
(1)“滤渣1”中存在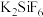 ,其阴离子的空间构型为
,其阴离子的空间构型为___________ 。“浸出”时最佳 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因___________ 。
(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式___________ (注明物质状态)。
(3)“沉淀”稀土离子的离子方程式为___________ 。
(4)回收利用“滤液”的操作单元是___________ 。
(5)“操作2”的名称为___________ ,实验室进行该步操作需要用到的玻璃仪器有___________ 。
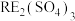 工艺流程如图。
工艺流程如图。
已知:①稀土矿中
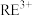 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子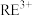
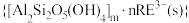 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将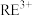 与
与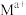 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。②常温下部分难溶物的溶度积如表:
| 物质 |  |  | 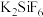 |
 | 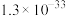 |  |  |

回答下列问题:
(1)“滤渣1”中存在
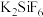 ,其阴离子的空间构型为
,其阴离子的空间构型为 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式
(3)“沉淀”稀土离子的离子方程式为
(4)回收利用“滤液”的操作单元是
(5)“操作2”的名称为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe 等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。___________ 。
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。___________ 。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为___________ 。
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为___________ g·cm-3。
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是___________ 。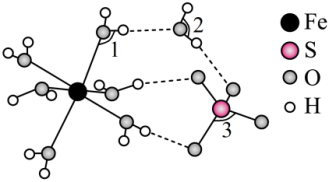
(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有___________ (填标号)。___________ 个,该距离为___________ pm(用含ρ和NA的代数式表示)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.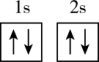 B.
B.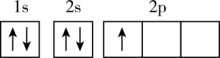 C.
C.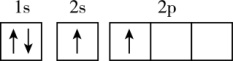 D.
D.
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。

②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是

(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有
a.  b.
b.  c.
c. d.
d.  e.
e.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】硒(Se)是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含Se分子(Ⅳ)合成路线如下:
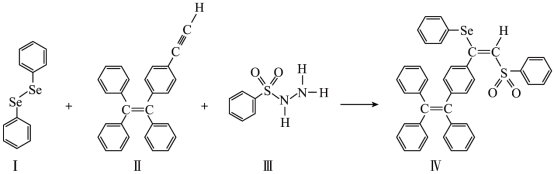
(1)Se与S同族,基态硒原子价电子排布式为__________ 。
(2) 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:__________ 。
(3)关于Ⅰ~Ⅳ四种物质中,下列说法正确的有__________ 。
a.Ⅰ中仅有 键,其中的Se—Se键为非极性键
键,其中的Se—Se键为非极性键
b.Ⅱ易溶于水,其分子式为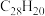
c.Ⅲ、Ⅳ中C均为 杂化,S均为
杂化,S均为 杂化
杂化
d.Ⅰ~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有__________ 。
(5)推测硒的两种含氧酸的酸性强弱为
______  (填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为__________ 。
(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
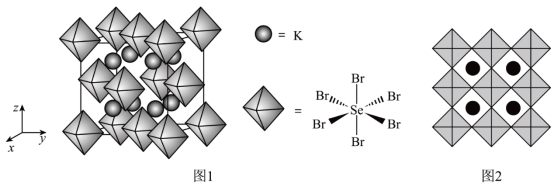
①X的化学式为__________ 。
②设X的最简式的式量为Mr,晶体密度为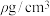 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为__________ nm(列出计算式, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,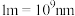 )。
)。

(1)Se与S同族,基态硒原子价电子排布式为
(2)
 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:(3)关于Ⅰ~Ⅳ四种物质中,下列说法正确的有
a.Ⅰ中仅有
 键,其中的Se—Se键为非极性键
键,其中的Se—Se键为非极性键b.Ⅱ易溶于水,其分子式为
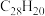
c.Ⅲ、Ⅳ中C均为
 杂化,S均为
杂化,S均为 杂化
杂化d.Ⅰ~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)推测硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为Mr,晶体密度为
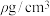 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,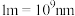 )。
)。
您最近一年使用:0次
【推荐2】A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为______________________________________ 。
(2)AB2分子中,A的杂化类型为___________ ;在元素周期表中A、B及与两者紧邻的元素的第一电离能由大到小的顺序为(用元素符号表示)_________ ;1个AB2分子中,含有______ 个π 键和______ 个σ键。
(3)AB2形成的晶体的熔点_________ (填“高于”“低于”或“无法判断”)CD形成的晶体的熔点,原因是____________________________ .
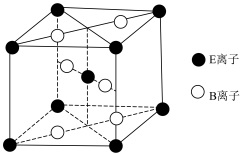
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为______ (用元素符号表示)。 ED4是制取航天航空工业材料的重要原料。取上述橙红色晶体,放在电炉中,通入D2和A的单质后高温加热,可制得ED4,同时产生一种造成温室效应的气体,写出反应的化学方程式:______________ .
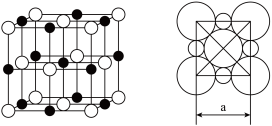
(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如下图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:若a=5.6×10-8cm,则该晶体的密度为____________ g·cm-3。(精确到小数点后1位)。
(1)E的基态原子价层电子排布式为
(2)AB2分子中,A的杂化类型为
(3)AB2形成的晶体的熔点
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为

(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如下图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:若a=5.6×10-8cm,则该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】磷及其化合物在工农业生产中都有重要作用。
(1)磷原子核外电子排布式为_______ 。
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为_______ , 的空间构型为
的空间构型为_______ ,该化合物中所含元素电负性最大的是_______ 。
(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);( ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……
P:( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……
①请在图中画出磷化硼晶胞的俯视图_______ 。
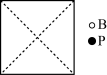
②与每个磷原子紧邻的硼原子有_______ 个,与每个硼原子紧邻的硼原子有_______ 个。
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为_______ ,与 互为等电子体的阴离子有
互为等电子体的阴离子有_______ (写出一种离子符号)。已知晶胞参数a=0.69nm,c=0.60nm,阿伏加德罗常数的值为NA,则该磷钇矿的密度为_______ g·cm-3(列出计算式)。

(1)磷原子核外电子排布式为
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为
 的空间构型为
的空间构型为(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(
 ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……P:(
 ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……①请在图中画出磷化硼晶胞的俯视图

②与每个磷原子紧邻的硼原子有
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为
 互为等电子体的阴离子有
互为等电子体的阴离子有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】半导体纳米晶在生物医学领域有很大需求。我国科研团队用 作保护气,油酸为溶剂,以氧化镉(
作保护气,油酸为溶剂,以氧化镉( )和硒、硫为前驱体得到纳米晶
)和硒、硫为前驱体得到纳米晶 。回答下列问题:
。回答下列问题:
(1) 与
与 同族,均位于元素周期表中
同族,均位于元素周期表中___________ 区;基态N原子电子排布式为___________ 。
(2) 的简单氢化物沸点由高到低的顺序为
的简单氢化物沸点由高到低的顺序为___________ ,原因为___________ 。
(3) 比
比 更易分解,由此可知键能:
更易分解,由此可知键能:
___________ (填“>”“=”或“<”) 。
。
(4)已知油酸的结构简式为 。油酸中各元素电负性由大到小的顺序为
。油酸中各元素电负性由大到小的顺序为___________ ,其中碳原子的杂化方式为___________ 。
(5) 的立方晶胞结构相似(如图)。
的立方晶胞结构相似(如图)。

① 晶胞中,
晶胞中, 原子位于由
原子位于由 原子构成的
原子构成的___________ (填“正四面体”“正六面体”或“正八而体”)空隙中,其空间占有率为___________ 。
② 的晶胞参数为
的晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶胞的密度为
,该晶胞的密度为___________  (写出表达式)。
(写出表达式)。
 作保护气,油酸为溶剂,以氧化镉(
作保护气,油酸为溶剂,以氧化镉( )和硒、硫为前驱体得到纳米晶
)和硒、硫为前驱体得到纳米晶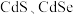 。回答下列问题:
。回答下列问题:(1)
 与
与 同族,均位于元素周期表中
同族,均位于元素周期表中(2)
 的简单氢化物沸点由高到低的顺序为
的简单氢化物沸点由高到低的顺序为(3)
 比
比 更易分解,由此可知键能:
更易分解,由此可知键能:
 。
。(4)已知油酸的结构简式为
 。油酸中各元素电负性由大到小的顺序为
。油酸中各元素电负性由大到小的顺序为(5)
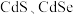 的立方晶胞结构相似(如图)。
的立方晶胞结构相似(如图)。
①
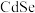 晶胞中,
晶胞中, 原子位于由
原子位于由 原子构成的
原子构成的②
 的晶胞参数为
的晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶胞的密度为
,该晶胞的密度为 (写出表达式)。
(写出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】由Sn、V、Gd等元素组成钒基笼目金属在超导电性方面有广阔的应用前景。回答下列问题:
(1)Sn与C同主族,基态Sn原子的价电子排布式为___________ ,Sn和Cl2反应会生成SnCl2和SnCl4。SnCl2(s)以线性聚合状态存在,其结构如图。

Cl-Sn-Cl键角:SnCl2(s)___________ SnCl4(填“>”或“<”),原因是___________ 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为___________ ;钒有+2、+3、+4、+5等多种化合价,从原子结构角度分析最稳定的化合价是___________ ;将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列含V物质中,属于顺磁性物质的是___________ (填标号)。
A.VF4 B.V(NH3)3Cl3 C.Na3VO4 D.Na4[V(CN)6]
(3)已知钒基笼目金属的晶体结构如图。该钒基笼目金属的化学式为___________ ,1号、2号Sn原子间的距离为___________ pm。

(1)Sn与C同主族,基态Sn原子的价电子排布式为

Cl-Sn-Cl键角:SnCl2(s)
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为
A.VF4 B.V(NH3)3Cl3 C.Na3VO4 D.Na4[V(CN)6]
(3)已知钒基笼目金属的晶体结构如图。该钒基笼目金属的化学式为

您最近一年使用:0次

 和
和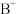 的电子数相差8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差2,A、B和D三种元素组成的一个化合物的晶胞如图所示。
的电子数相差8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差2,A、B和D三种元素组成的一个化合物的晶胞如图所示。


