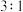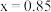向100mL
 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、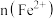 、
、 随通入
随通入 的物质的量
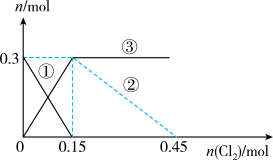
的物质的量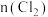 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是

 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、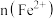 、
、 随通入
随通入 的物质的量
的物质的量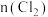 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
A.②代表 ,③代表 ,③代表 |
B.还原性强弱: |
C. 时,溶液中 时,溶液中 |
D.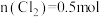 时,总的离子方程式为: 时,总的离子方程式为: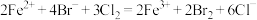 |
更新时间:2023-01-04 20:26:04
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列关于氧化性、还原性的判断正确的是
| A.B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 |
| B.发生氧化还原反应时,A原子失去的电子比B原子多,证明 A的金属性一定比B强 |
| C.因为氯水具有漂白性,所以可以使酸性KMnO4溶液褪色 |
| D.一定量的氯气通入30 mL 10.00 mol/L的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列对应的离子方程式正确的是
A.用 溶液吸收少量 溶液吸收少量 |
B.用铜电极电解饱和食盐水: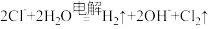 |
C.白色固体 加入氨水中得到无色溶液: 加入氨水中得到无色溶液: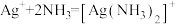 |
D.向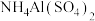 溶液中滴入 溶液中滴入 使 使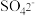 反应完全: 反应完全: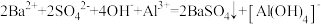 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】工业上用发烟 ,把潮湿的
,把潮湿的 氧化为棕色的烟
氧化为棕色的烟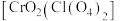 来除去
来除去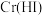 ,
, 中部分氯元素转化为最低价态。下列说法不正确的是( )
中部分氯元素转化为最低价态。下列说法不正确的是( )
 ,把潮湿的
,把潮湿的 氧化为棕色的烟
氧化为棕色的烟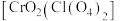 来除去
来除去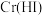 ,
, 中部分氯元素转化为最低价态。下列说法不正确的是( )
中部分氯元素转化为最低价态。下列说法不正确的是( )A. 属于强酸, 属于强酸,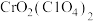 中Cr元素显 中Cr元素显 价 价 |
B.该反应除生成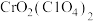 外,还生成了另一种强酸 外,还生成了另一种强酸 |
C.该反应中,参加反应的 与 与 物质的量之比为1∶2 物质的量之比为1∶2 |
D.作氧化剂的 与参加反应的 与参加反应的 物质的量之比为3∶16 物质的量之比为3∶16 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量的镁与100 mL 18.5 mol/L浓硫酸充分反应后,镁完全溶解,同时生成气体A 33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液的c(H+) = 0.1 mol/L,则下列叙述中错误的是
| A.反应中共转移电子3 mol | B.反应中共消耗镁 36 g |
| C.气体A中SO2与H2的体积比为3:1 | D.气体A为SO2和H2的混合物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向2L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。下列有关说法不正确的是
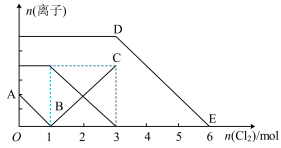

| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)=1.5 mol·L-1 |
| C.当通入Cl2 2 mol时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=1∶2∶3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知①2 +16H++10Cl-=2Mn2++5Cl2↑+8H2O
+16H++10Cl-=2Mn2++5Cl2↑+8H2O
②Cl2+2Fe2+=2Fe3++2Cl-
③2Fe3++2I-=I2+2Fe2+
由此判断,下列说法正确的是
 +16H++10Cl-=2Mn2++5Cl2↑+8H2O
+16H++10Cl-=2Mn2++5Cl2↑+8H2O②Cl2+2Fe2+=2Fe3++2Cl-
③2Fe3++2I-=I2+2Fe2+
由此判断,下列说法正确的是
| A.氧化性:I->Fe2+>Cl->Mn2+ |
| B.把一定量Cl2通入FeI2溶液中时,能发生2Cl2+2Fe2++2I-=2Fe3++I2+4Cl- |
| C.将用盐酸酸化的KMnO4溶液加入FeSO4溶液中,若紫色褪去,则可验证溶液中含有Fe2+ |
| D.若某溶液中含有Fe2+、Cl-、I-,要氧化I-而不氧化Fe2+和Cl-,可以加入FeCl3溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随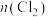 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随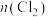 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是
A.a点溶液中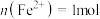 |
B.b点时已通入氯气的总体积为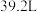 (标况) (标况) |
C.c点的总反应离子方程式为 |
D.d点溶液中阴离子的个数为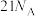 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】将一定量锌与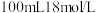 浓硫酸充分反应后,若锌完全溶解同时产生气体
浓硫酸充分反应后,若锌完全溶解同时产生气体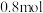 ,将反应后的溶液稀释为400mL,测得溶液
,将反应后的溶液稀释为400mL,测得溶液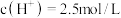 ,则下列叙述中错误的是
,则下列叙述中错误的是
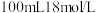 浓硫酸充分反应后,若锌完全溶解同时产生气体
浓硫酸充分反应后,若锌完全溶解同时产生气体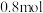 ,将反应后的溶液稀释为400mL,测得溶液
,将反应后的溶液稀释为400mL,测得溶液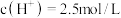 ,则下列叙述中错误的是
,则下列叙述中错误的是| A.反应中共消耗锌48.0g |
| B.反应中生成的气体在标况下体积为17.92L |
C.气体中 和 和 物质的量之比为5:3 物质的量之比为5:3 |
| D.反应共转移电子1.6mol |
您最近一年使用:0次

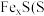 为
为 价
价 ,既含有
,既含有 ,又含有
,又含有 注:矿石中其他成分不与盐酸反应
注:矿石中其他成分不与盐酸反应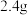 硫单质,
硫单质,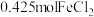 和一定量
和一定量 气体,且溶液中无
气体,且溶液中无

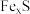 中,
中,