回答下列问题
(1)依据反应: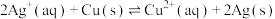 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
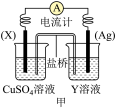
①电极 的材料是
的材料是_______ ;Y溶液可以是_______ ;
②银电极上发生的电极反应式是_______ , 电极上发生的电极反应为
电极上发生的电极反应为_______ 反应(填“氧化”或“还原”);外电路中的电子_______ (填“流出”或“流向”)Ag电极。
(2)次磷酸 是一种精细化工产品,已知
是一种精细化工产品,已知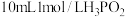 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:
①次磷酸 属于
属于_______ (填“一元酸”“二元酸”或“无法确定”)。
②设计实验方案,证明次磷酸是弱酸:_______ 。
(3)某课外兴趣小组用 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
①该小组同学选用酚酞做指示剂,滴定终点的现象为_______ 。
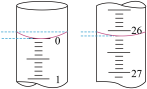
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为_______  。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是_______
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
(1)依据反应:
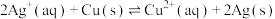 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
①电极
 的材料是
的材料是②银电极上发生的电极反应式是
 电极上发生的电极反应为
电极上发生的电极反应为(2)次磷酸
 是一种精细化工产品,已知
是一种精细化工产品,已知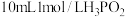 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:①次磷酸
 属于
属于②设计实验方案,证明次磷酸是弱酸:
(3)某课外兴趣小组用
 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。①该小组同学选用酚酞做指示剂,滴定终点的现象为
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为
 。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
更新时间:2023-01-08 15:23:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol·L-1的NaOH溶液滴定上述稀H2SO4溶液25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入几滴酚酞做指示剂
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管,调整液面,记下开始读数
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
滴定操作的正确顺序是(用序号填写)_______________ 。
(2)在D操作中应该调整液面到_________________ ,并使尖嘴处_____________ 。
(3)配制准确浓度的稀H2SO4溶液,必须使用的主要容器是__________________ 。
(4)滴定到终点时锥形瓶内溶液的pH约为________ ;终点时颜色变化是____________ 。
(5)用标准NaOH溶液滴定时,应将标准NaOH溶液注入____ (选填“甲”或“乙”)中。

(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值___________ (选填“偏大”“偏小”或“无影响”)。
(7)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)____ 。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol·L-1的NaOH溶液滴定上述稀H2SO4溶液25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入几滴酚酞做指示剂
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管,调整液面,记下开始读数
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
滴定操作的正确顺序是(用序号填写)
(2)在D操作中应该调整液面到
(3)配制准确浓度的稀H2SO4溶液,必须使用的主要容器是
(4)滴定到终点时锥形瓶内溶液的pH约为
(5)用标准NaOH溶液滴定时,应将标准NaOH溶液注入

(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值
(7)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】油脂的不饱和度可通过油脂与碘的加成反应测定,通常称为油脂的碘值。碘值越大,油脂的不饱和程度越高。碘值是指100g油脂所能吸收的I2的克数。称取xg某油脂,加入含ymol I2的韦氏溶液(韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用cmol/L Na2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液VmL(滴定反应为:2Na2S2O3+I2=Na2S4O6+2NaI)。回答下列问题:
(1)下列有关滴定的说法不正确的是__ (填标号)。
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C.滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是__ 。
(3)该油脂的碘值为__ g(列式表示)。
(1)下列有关滴定的说法不正确的是
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C.滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是
(3)该油脂的碘值为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学生为测定某烧碱样品中NaOH的质量分数,进行如下实验(已知该样品中含有少量不与酸作用的杂质):
A.在250 mL容量瓶中定容,配制成250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品20.5 g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为1.00 mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL
E.锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记录终点耗酸体积V2 mL
回答下列问题:
(1)正确操作步骤的顺序是________ →________ →________ →D→________ (均用字母填写)。(每空一分)
(2)滴定管读数应注意____________________________________ 。
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用_______________________ 。
(4)下列操作中可能使所测NaOH的质量分数偏低的是______ (填字母)。
a.A步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.C步操作中,称量药品时,砝码放在左盘,NaOH放在右盘
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
A.在250 mL容量瓶中定容,配制成250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品20.5 g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为1.00 mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL
E.锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记录终点耗酸体积V2 mL
回答下列问题:
(1)正确操作步骤的顺序是
(2)滴定管读数应注意
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用
(4)下列操作中可能使所测NaOH的质量分数偏低的是
a.A步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.C步操作中,称量药品时,砝码放在左盘,NaOH放在右盘
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】滴定法是解决化学分析问题的常用方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.如图为某浓度的NaOH溶液滴定10.00mL一定浓度的盐酸的示意图。根据图象分析:
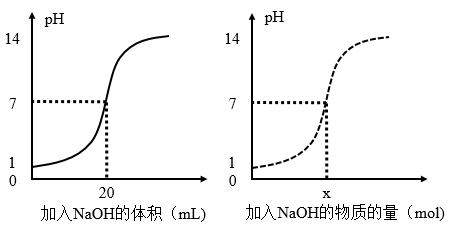
(1)HCl溶液的浓度是__________ ;NaOH溶液的浓度是_______ ;
(2) x =________ 。
ΙΙ.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
(3)人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度,抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,滴定的实验数据如下所示:
①滴定时,盛放高锰酸钾溶液的仪器名称为_________ 确定反应达到终点的现象_____________ 。
②草酸跟酸性KMnO4溶液反应的离子方程式为:2 + 5H2C2O4+ 6H+═ 2Mn2++ 10CO2↑ + 8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为
+ 5H2C2O4+ 6H+═ 2Mn2++ 10CO2↑ + 8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为__________ mg/cm3
I.如图为某浓度的NaOH溶液滴定10.00mL一定浓度的盐酸的示意图。根据图象分析:

(1)HCl溶液的浓度是
(2) x =
ΙΙ.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
(3)人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度,抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,滴定的实验数据如下所示:
| 实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
| 1 | 20.00 | 11.95 |
| 2 | 20.00 | 13.00 |
| 3 | 20.00 | 12.05 |
②草酸跟酸性KMnO4溶液反应的离子方程式为:2
 + 5H2C2O4+ 6H+═ 2Mn2++ 10CO2↑ + 8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为
+ 5H2C2O4+ 6H+═ 2Mn2++ 10CO2↑ + 8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.中和反应反应热的测定。
测定50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是_______ 。
(2)若两种溶液的密度均为 ,反应后生成溶液的比热容
,反应后生成溶液的比热容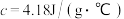 ,反应过程中测得体系温度升高4℃,则该反应放出
,反应过程中测得体系温度升高4℃,则该反应放出_______ kJ热量。
Ⅱ.简易原电池反应。
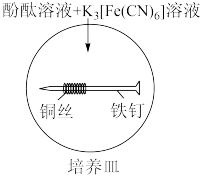
(3)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液和 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的_______ (填化学式)沉淀;铜丝周围的现象是_______ ,发生的电极反应式为_______ 。
Ⅲ.已知某烧碱样品中含有NaCl杂质,为测定样品中NaOH的质量分数,进行如下步骤实验:
①称量1.0g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.10mol/L的盐酸标准溶液滴定三次,每次消耗盐酸的体积记录如下:
请回答:
(4)观察滴定到终点时溶液颜色的变化为_______ 。
(5)烧碱样品的纯度为_______ 。
(6)若出现下列情况,测定结果偏低的是_______ 。
a.滴定前用待测液冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.盛装标准液的滴定管水洗后未用标准液再润洗
Ⅰ.中和反应反应热的测定。
测定50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是
(2)若两种溶液的密度均为
 ,反应后生成溶液的比热容
,反应后生成溶液的比热容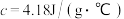 ,反应过程中测得体系温度升高4℃,则该反应放出
,反应过程中测得体系温度升高4℃,则该反应放出Ⅱ.简易原电池反应。

(3)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的Ⅲ.已知某烧碱样品中含有NaCl杂质,为测定样品中NaOH的质量分数,进行如下步骤实验:
①称量1.0g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.10mol/L的盐酸标准溶液滴定三次,每次消耗盐酸的体积记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 21.60 |
| 2 | 25.00 | 6.00 | 27.00 |
| 3 | 25.00 | 1.10 | 22.00 |
(4)观察滴定到终点时溶液颜色的变化为
(5)烧碱样品的纯度为
(6)若出现下列情况,测定结果偏低的是
a.滴定前用待测液冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.盛装标准液的滴定管水洗后未用标准液再润洗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】兴趣小组同学用0.1mol•L-1的标准KOH溶液滴定未知浓度的盐酸,操作如下:
①移取25.00mL待测盐酸注入洁净的锥形瓶中,并加入2~3滴酚酞;
②用标准KOH溶液润洗滴定管2~3次;
③取标准KOH溶液注入滴定管至0刻度线以上2~3cm;
④将盛有标准KOH溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液;
⑤调节液面至0刻度或0刻度以下,记下读数;
⑥将锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度。
(1)正确的操作顺序是______ (填序号)。
(2)操作②中使用的滴定管为图中的______ (填“甲”或“乙”)。
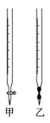
(3)若用25mL滴定管进行实验,当滴定管中的液面在“10”处时,管内液体的体积______ (填字母)。
(4)步骤⑥达到滴定终点的标志是_______ 。
(5)实验数据记录如表:
计算待测盐酸的物质的量浓度为______ mol/L。
(6)下列操作对所测盐酸的浓度有何影响?(填“偏大”、“偏小”或“无影响”)
A.进行步骤①之前,先用待测液润洗锥形瓶______ ;
B.所用KOH固体中含有少量NaOH杂质______ ;
C.滴定前装有待测溶液的滴定管尖嘴部分有气泡,滴定结束后气泡消失______ 。
①移取25.00mL待测盐酸注入洁净的锥形瓶中,并加入2~3滴酚酞;
②用标准KOH溶液润洗滴定管2~3次;
③取标准KOH溶液注入滴定管至0刻度线以上2~3cm;
④将盛有标准KOH溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液;
⑤调节液面至0刻度或0刻度以下,记下读数;
⑥将锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度。
(1)正确的操作顺序是
(2)操作②中使用的滴定管为图中的

(3)若用25mL滴定管进行实验,当滴定管中的液面在“10”处时,管内液体的体积
| A.等于10mL | B.等于15mL | C.小于10mL | D.大于15mL |
(5)实验数据记录如表:
| 实验编号 | 待测盐酸体积(mL) | 消耗标准KOH溶液的体积(mL) | |
| 滴定开始读数 | 滴定结束读数 | ||
| i | 25.00 | 0.00 | 19.95 |
| ii | 25.00 | 1.10 | 18.30 |
| iii | 25.00 | 0.20 | 20.25 |
(6)下列操作对所测盐酸的浓度有何影响?(填“偏大”、“偏小”或“无影响”)
A.进行步骤①之前,先用待测液润洗锥形瓶
B.所用KOH固体中含有少量NaOH杂质
C.滴定前装有待测溶液的滴定管尖嘴部分有气泡,滴定结束后气泡消失
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】溶液的酸碱性是影响物质性质的重要因素。
(1)常温下,现有等体积、 的
的 和
和 两种溶液,分别稀释100倍后,
两种溶液,分别稀释100倍后, 的大小关系为前者
的大小关系为前者_____ 后者(填“>”、“<”或“=”,下同)。若向两种溶液中分别加入足量锌,相同状况下产生气体体积大小关系为前者_____ 后者。若分别与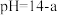 的氢氧化钠溶液等体积混合,反应后溶液的
的氢氧化钠溶液等体积混合,反应后溶液的 的大小关系为前者
的大小关系为前者_____ 后者。
(2)常温下某些弱酸和氨水的电离常数如下:
①下列反应可以发生的是___________ (填序号)。
A.
B.
C.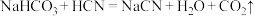
D.
②25℃时,将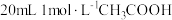 溶液和
溶液和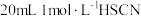 溶液分别与
溶液分别与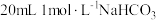 溶液混合,画出产生的
溶液混合,画出产生的 气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式
气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式______ 。

③常温下用氨水吸收 可得到
可得到 溶液,
溶液, 溶液显
溶液显_____ (填“酸性”“中性”或“碱性”),请计算反应 的平衡常数K=
的平衡常数K=____ (保留两位有效数字)。
(1)常温下,现有等体积、
 的
的 和
和 两种溶液,分别稀释100倍后,
两种溶液,分别稀释100倍后, 的大小关系为前者
的大小关系为前者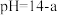 的氢氧化钠溶液等体积混合,反应后溶液的
的氢氧化钠溶液等体积混合,反应后溶液的 的大小关系为前者
的大小关系为前者(2)常温下某些弱酸和氨水的电离常数如下:
| 化学式 |  |  |  |  |  |  |
| 电离常数 |  | 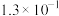 |  |  | 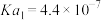 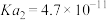 |  |
①下列反应可以发生的是
A.

B.

C.
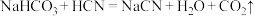
D.

②25℃时,将
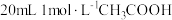 溶液和
溶液和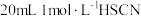 溶液分别与
溶液分别与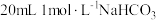 溶液混合,画出产生的
溶液混合,画出产生的 气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式
气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式
③常温下用氨水吸收
 可得到
可得到 溶液,
溶液, 溶液显
溶液显 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】盐酸和醋酸是生活中常用的酸。某实验小组进行了以下实验:
实验一、对比盐酸和醋酸的稀释
用pH计测定25℃时不同浓度醋酸的pH,结果如下:
(1)醋酸的电离方程式_______ 。
(2)25℃时,随着醋酸浓度的增大,醋酸电离程度_______ (填“增大”“减小”或“不变”)
(3)常温下, 溶液加水稀释的过程中,下列表达式的数值一定变小的是____。
溶液加水稀释的过程中,下列表达式的数值一定变小的是____。
(4)图是两种酸稀释过程pH随溶液体积变化的曲线,曲线II代表的酸是_______ ,a、b、c三点导电能力由大到小的顺序是_______ 。

实验二、对比盐酸和醋酸与NaOH反应
常温下,用0.1000mol·L-1NaOH溶液分别滴定20mL0.1000mol·L-1的盐酸和醋酸,滴定过程中溶液的pH的变化曲线如图2所示。
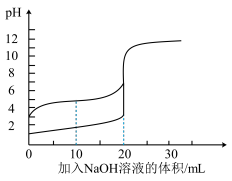
(5)a点溶液中,离子浓度由大到小的顺序为_______ 。
(6)当滴定至溶液pH=7时,醋酸消耗的NaOH溶液的体积_______ 盐酸消耗的NaOH溶液的体积。(填“>”“<”或“=”)
实验一、对比盐酸和醋酸的稀释
用pH计测定25℃时不同浓度醋酸的pH,结果如下:
| 浓度(mol/L) | 0.0010 | 0.0100 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 2.88 | 2.83 |
(1)醋酸的电离方程式
(2)25℃时,随着醋酸浓度的增大,醋酸电离程度
(3)常温下,
 溶液加水稀释的过程中,下列表达式的数值一定变小的是____。
溶液加水稀释的过程中,下列表达式的数值一定变小的是____。| A.c(H+) | B. | C.c(H+)∙c(OH—) | D. |

实验二、对比盐酸和醋酸与NaOH反应
常温下,用0.1000mol·L-1NaOH溶液分别滴定20mL0.1000mol·L-1的盐酸和醋酸,滴定过程中溶液的pH的变化曲线如图2所示。

(5)a点溶液中,离子浓度由大到小的顺序为
(6)当滴定至溶液pH=7时,醋酸消耗的NaOH溶液的体积
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)体积相同、 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)_________ 。
(2)将浓度为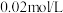 的
的 与
与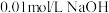 溶液等体积混合,测得混合洛液中
溶液等体积混合,测得混合洛液中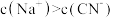 ,下列关系正确的是
,下列关系正确的是_________ 。
a. b.
b.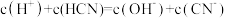 c.
c.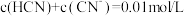
(3)25℃时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为_________ ;
(4)25℃时,醋酸的电离常数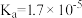 ,则该温度下
,则该温度下 的
的
_________ (保留一位小数)。
(5)25℃时, 的醋酸和
的醋酸和 的氢氧化钠等体积混合后溶液呈
的氢氧化钠等体积混合后溶液呈_________ (填“酸性”“中性”或“碱性”)
(6)25℃时,醋酸的电离常数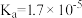 ,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的
,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的 ,则
,则 的电离常数
的电离常数
_________ 。
| 醋酸 | 氢硫酸 | 氢氰酸 |
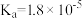 | 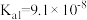 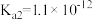 | 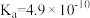 |
(1)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)(2)将浓度为
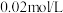 的
的 与
与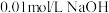 溶液等体积混合,测得混合洛液中
溶液等体积混合,测得混合洛液中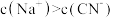 ,下列关系正确的是
,下列关系正确的是a.
 b.
b.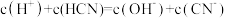 c.
c.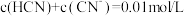
(3)25℃时,向
 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为(4)25℃时,醋酸的电离常数
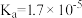 ,则该温度下
,则该温度下 的
的
(5)25℃时,
 的醋酸和
的醋酸和 的氢氧化钠等体积混合后溶液呈
的氢氧化钠等体积混合后溶液呈(6)25℃时,醋酸的电离常数
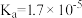 ,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的
,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的 ,则
,则 的电离常数
的电离常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物(NO2)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①△H1___ 0,△H3____ 0。(填“>”或“<”)
②N2(g)+O2(g)=2NO(g)△H=____ kJ·mol-1。
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为_______ 。
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:
①电极a名称是______ 。
②电解质溶液中OH-离子向_____ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为_____ 。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是_____ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | △H1 | △H2 | △H3 |
| 热量值kJ/mol | 945 | 498 | 630 |
①△H1
②N2(g)+O2(g)=2NO(g)△H=
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】十九大报告提出要对环境问题进行全面、系统的可持续治理。
回答下列问题:
(1)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。

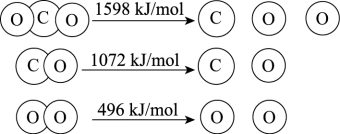
①上述过程中,能量的变化形式是由________ 转化为________ 。
②根据数据计算,分解1molCO2需________ (填“吸收”或“放出”)________ kJ的能量。
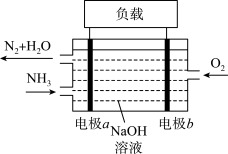
(2)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。
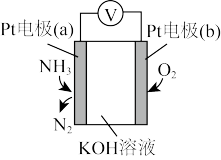
①Pt电极(a)为________ 极(填“正”或“负”);Pt电极(b)上的电极反应式为:________ 。
②该过程总反应的化学反应方程式为________ ,反应一段时间后,KOH溶液的浓度将________ (填“增大”“减小”或“不变”)。
回答下列问题:
(1)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。


①上述过程中,能量的变化形式是由
②根据数据计算,分解1molCO2需
(2)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。

①Pt电极(a)为
②该过程总反应的化学反应方程式为
您最近一年使用:0次
【推荐3】完成下列小题
(1)未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是_____
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
(2)氮是重要的化工原料,已知NH3在纯氧中燃烧的能量变化如图。
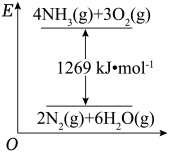
已知:H2O(l)=H2O(g) △H=+44kJ∙mol-1,则NH3(g)的摩尔燃烧焓的热化学方程式为_____ 。
(3)NH3的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极a为_____ (填“正极”或“负极”);电极b上的电极反应为_____ 。当共消耗1.568L(标准状况)气体时,通过负载的电子的物质的量为_____ mol。
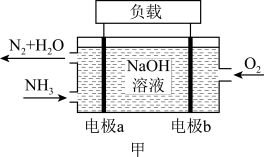
(4)一种肼N2H4燃料电池的工作原理如图乙所示。
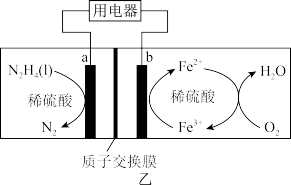
①a极的电极反应式为_____ ;电池中Fe2+→Fe3+的离子方程式为_____ 。
②若利用该电池给铅酸蓄电池充电,当消耗3.2gN2H4时,PbO2电极质量_____ (填“增加”或“减少”)_____ g。
(1)未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是_____
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ | C.③⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |

已知:H2O(l)=H2O(g) △H=+44kJ∙mol-1,则NH3(g)的摩尔燃烧焓的热化学方程式为
(3)NH3的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极a为

(4)一种肼N2H4燃料电池的工作原理如图乙所示。

①a极的电极反应式为
②若利用该电池给铅酸蓄电池充电,当消耗3.2gN2H4时,PbO2电极质量
您最近一年使用:0次



