回答下列问题:
(1)Xe是第五周期的稀有气体元素,与 形成的
形成的 室温下易升华。
室温下易升华。 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
(2)已知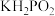 是次磷酸的正盐,
是次磷酸的正盐, 的结构式为
的结构式为_______ ,其中P采取_______ 杂化方式。
(3)氨硼烷在催化剂作用下水解释放氢气: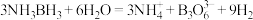 。
。 的结构为
的结构为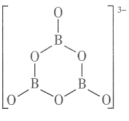 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(4)乙二胺 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是_______ 、_______ 。
(1)Xe是第五周期的稀有气体元素,与
 形成的
形成的 室温下易升华。
室温下易升华。 中心原子的价层电子对数为
中心原子的价层电子对数为 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是A.
 B.
B. C.
C. D.
D.
(2)已知
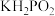 是次磷酸的正盐,
是次磷酸的正盐, 的结构式为
的结构式为(3)氨硼烷在催化剂作用下水解释放氢气:
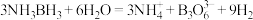 。
。 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(4)乙二胺
 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是
2023高三·全国·专题练习 查看更多[1]
(已下线)题型89 杂化轨道类型及分子空间构型的判断
更新时间:2023-03-09 20:49:34
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氢气是重要而洁净的能源,要利用氢气作能源,必须安
全有效地储存氢气。
(1)某种铜镍合金材料有较大的储氢容量,其晶体结构如图所示。这种合金中La与Ni的原子个数比为 ;其中基态Ni原子的核外电子排布式为 。
(2)氢元素可与其他四种短周期元素a、b、c、d、e、f、g等七种微粒,它们都有10个电子,其填结构特点如下表:
①与c互为等电子体的一种阴离子是 (填化学式);
②微粒中中心原子的杂化方式为 杂化。
③比较相同条件下a与f在水中的溶解度:a f(填“>”、“=”或“<”)
④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
全有效地储存氢气。
(1)某种铜镍合金材料有较大的储氢容量,其晶体结构如图所示。这种合金中La与Ni的原子个数比为 ;其中基态Ni原子的核外电子排布式为 。
(2)氢元素可与其他四种短周期元素a、b、c、d、e、f、g等七种微粒,它们都有10个电子,其填结构特点如下表:
| 微粒 | a | b | c | d | e | f | g |
| 原子核数 | 双核 | 双核 | 三核 | 四核 | 四核 | 五核 | 五核 |
| 所带单位电荷 | 0 | -1 | 0 | 0 | +1 | +1 |
①与c互为等电子体的一种阴离子是 (填化学式);
②微粒中中心原子的杂化方式为 杂化。
③比较相同条件下a与f在水中的溶解度:a f(填“>”、“=”或“<”)
④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
您最近一年使用:0次
【推荐2】中科院大连化物所的科学家在乙酰酮修饰锰氧化物L酸催化胺选择氧化方面的研究取得新进展。回答下列问题:
(1)Mn元素的价层电子排布式为___________ ,Mn元素的一种配合物K3[Mn(CN)6]具有反磁性,该配合物中σ键和π键的个数比为___________ 。
(2)乙腈(CH3CN)分子中碳原子的杂化类型有___________ ,与N同周期的主族元素中,第一电离能大于N的有___________ 种,写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式___________ ,NO 离子的立体构型是
离子的立体构型是___________
(3)苯胺(C6H5NH2)与甲苯的相对分子质量相近,但苯胺的熔、沸点分别高于甲苯的熔、沸点,原因是___________
(4)锰的某种氧化物的晶胞结构如图所示:
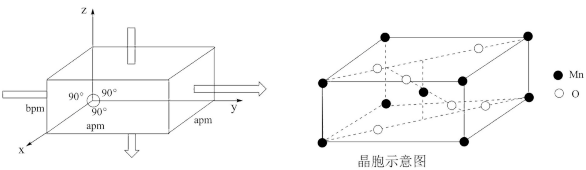
该锰元素的氧化物化学式为___________ ,该晶体的密度为___________  (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(1)Mn元素的价层电子排布式为
(2)乙腈(CH3CN)分子中碳原子的杂化类型有
 互为等电子体的分子的化学式
互为等电子体的分子的化学式 离子的立体构型是
离子的立体构型是(3)苯胺(C6H5NH2)与甲苯的相对分子质量相近,但苯胺的熔、沸点分别高于甲苯的熔、沸点,原因是
(4)锰的某种氧化物的晶胞结构如图所示:

该锰元素的氧化物化学式为
 (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】我国部分城市灰霾天比较多,引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知目前造成我国灰霾天气的原因主要是交通污染。
(1)Zn2+在基态时核外电子排布式为___________ 。
(2) 的立体构型是
的立体构型是___________ 。
(3)水分子的立体结构是___________ ,水分子能与很多金属离子形成配合物,其原因是在氧原子上有___________ 。
(4)Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为___________ ;与CO分子互为等电子体的分子为___________ (填化学式)。
(1)Zn2+在基态时核外电子排布式为
(2)
 的立体构型是
的立体构型是(3)水分子的立体结构是
(4)Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】在A、B、C三种元素中,A元素原子的价电子排布为2s22p5,B元素K、L能层上的电子数与M、N层上的电子数相同。C元素的原子序数等于A、B两元素原子序数之和,C的单质在生产生活中具有许多用途,它可在硫酸铜溶液中用电解法进行精炼。请回答以下问题:
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成___ 键(填“共价”或“离子”);
(2)C元素的价电子排布式为__________ ;
(3)在A元素氢化物的水溶液中,存在有__________ 种不同类型的氢键;
(4)SO42—中S原子的杂化轨道类型是_________ ,SO42—的立体构型是_________ ;
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为____________ ;该晶体中,原子之间的作用力是_____________ ;
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点和面心上的元素为________ (填具体的元素符号)。
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成
(2)C元素的价电子排布式为
(3)在A元素氢化物的水溶液中,存在有
(4)SO42—中S原子的杂化轨道类型是
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点和面心上的元素为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇( )空气氧化法是生产工业甲醛(
)空气氧化法是生产工业甲醛( )的常用方法。发生的反应为
)的常用方法。发生的反应为

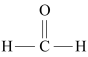 +2H2O
+2H2O
(1) 所含官能团名称为
所含官能团名称为_______ ; 所含官能团名称为
所含官能团名称为_______ 。
(2) 的中心原子上的孤电子对数为
的中心原子上的孤电子对数为_______ 。
(3) 分子内
分子内 键与
键与 键个数之比为
键个数之比为_______ , 的空间结构为
的空间结构为_______ 。
(4) 和
和 分子中碳原子的杂化轨道类型分别为
分子中碳原子的杂化轨道类型分别为_______ 和_______ 。
 )空气氧化法是生产工业甲醛(
)空气氧化法是生产工业甲醛( )的常用方法。发生的反应为
)的常用方法。发生的反应为
 +2H2O
+2H2O(1)
 所含官能团名称为
所含官能团名称为 所含官能团名称为
所含官能团名称为(2)
 的中心原子上的孤电子对数为
的中心原子上的孤电子对数为(3)
 分子内
分子内 键与
键与 键个数之比为
键个数之比为 的空间结构为
的空间结构为(4)
 和
和 分子中碳原子的杂化轨道类型分别为
分子中碳原子的杂化轨道类型分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钛(Ti)和锆(Zr)是同一副族的相邻元素,它们的化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为_______ ;与钛位于同一周期且基态原子单电子数与钛相同的元素,第一电离能由大到小的顺序为_______ (用元素符号填空)。
(2)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是_______ 。
(3)下列各组微粒互为等电子体的是_______(填字母标号)。
(4)ZrCl4可以与乙二胺形成配合物[ZrCl4(H2NCH2CH2NH2)]。
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为_______ mol。
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将_______ (填“变大”、“变小”或“不变”),原因是_______ 。
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是_______ 。
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为_______ 。
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离_______ pm(列出表达式,NA为阿伏加德罗常数的值,ZrO2的摩尔质量为M g/mol)。
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为
(2)Ti(BH4)2是一种储氢材料。BH
 的空间构型是
的空间构型是(3)下列各组微粒互为等电子体的是_______(填字母标号)。
| A.H2O与SO2 | B.CO2与N2O | C.CH2O与BF3 | D.C6H6与B3N3H6 |
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离
您最近一年使用:0次



