主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,他们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为_________ ,W3分子的空间构型为_________ ;
(2)X单质与水发生主要反应的化学方程式为____________________________ ;
(3)化合物M的化学式为________ ,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是________ 。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有_________ ,O—C—O的键角约为_________ ;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z=_________ ;
(5)含有元素Z的盐的焰色反应为_________ 色。许多金属盐都可以发生焰色反应,其原因是________________________________________________________ 。
(1)W元素原子的L层电子排布式为
(2)X单质与水发生主要反应的化学方程式为
(3)化合物M的化学式为
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z=
(5)含有元素Z的盐的焰色反应为
更新时间:2016-12-09 00:37:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_____ 周期_____ 族。
(2)B的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式为_____ 。
(3)研究物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种的是_____ (填化学式)。
(4)能说明元素D的非金属性强于元素C的非金属性的实验事实是_____ (填字母)。
a.常温下,两种单质的熔点不同
b.两种元素的气态氢化物的稳定性不同
c.两种元素的最高价氧化物对应的水化物酸性不同
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,可用作制冷剂 |
| B | 单质的焰色反应为黄色 |
| C | –2价阴离子的电子层结构与Ar原子相同 |
| D | 单质是黄绿色气体,可用于自来水消毒 |
(1)A在周期表中位于第
(2)B的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式为
(3)研究物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种的是
(4)能说明元素D的非金属性强于元素C的非金属性的实验事实是
a.常温下,两种单质的熔点不同
b.两种元素的气态氢化物的稳定性不同
c.两种元素的最高价氧化物对应的水化物酸性不同
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有X、Y、Z、W、M、N六种短周期主族元素,其原子序数依次增大。基态X原子有2个未成对的电子,Y与M同主族,基态Y原子的s电子总数与p电子总数相等,Z在短周期中原子半径最大,W 与N可形成共价化合物W2N6。
(1)基态X原子核外电子占据最高能层的符号____ ;基态Y原子的核外电子排布图____ ;元素W在周期表中的位置____ 。
(2)写出由Y、Z两种元素形成的淡黄色固体的电子式_____ 。
(3)在M常见的两种氧化物对应的水化物中,酸性更强的是___ (填化学式),理由_____ 。
(4)在相同条件下,MY2在水中溶解度比XY2在水中溶解度大,从结构角度解释原因:_____ 。
(5)实验室常用N的氢化物的浓溶液制N单质,其离子反应方程式:______ ;向KI溶液中通入适量的N单质后,再滴加一定量的CCl4,振荡静置后,观察到的现象是____
(1)基态X原子核外电子占据最高能层的符号
(2)写出由Y、Z两种元素形成的淡黄色固体的电子式
(3)在M常见的两种氧化物对应的水化物中,酸性更强的是
(4)在相同条件下,MY2在水中溶解度比XY2在水中溶解度大,从结构角度解释原因:
(5)实验室常用N的氢化物的浓溶液制N单质,其离子反应方程式:
您最近一年使用:0次
【推荐3】Ⅰ.下表标出的是元素周期表的一部分元素,回答下列问题:

①表中用字母标出的14种元素中,化学性质最不活泼的是____________ (用元素符号表示,下同),金属性最强的是____________ ,常温下单质为液态的非金属元素是____________ 。
②B、F、C气态氢化物中以________ (填分子式)最不稳定。
Ⅱ. 有短周期的A、B、C、D、E 五种元素,它们在周期表的位置如图所示。已知A原子最外层电子数是次外层电子数的2倍。试回答下列问题:
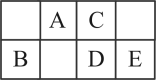
(1) 元素E在周期表中位于第_______ 周期_______ 族。
(2) 元素A的最高价氧化物的电子式为________ ,元素D的原子结构示意图为________ ;
(3) 比较C、D两种元素最高价氧化物对应水化物的酸性强弱:______ > ______ 。(用分子式表示)
(4)元素C的气态氢化物与元素E的最高价氧化物对应水化物化合生成的正盐的化学式为___________ ,该盐的晶体类型为________ 。
(5) ①元素B所在周期的简单离子半径最小的是______ 。(用离子符号表示)
②元素C、D的简单氢化物沸点较高的是______ 。(用分子式表示)
(6)请用电子式表示Na2S的形成过程____________________________________ 。

①表中用字母标出的14种元素中,化学性质最不活泼的是
②B、F、C气态氢化物中以
Ⅱ. 有短周期的A、B、C、D、E 五种元素,它们在周期表的位置如图所示。已知A原子最外层电子数是次外层电子数的2倍。试回答下列问题:

(1) 元素E在周期表中位于第
(2) 元素A的最高价氧化物的电子式为
(3) 比较C、D两种元素最高价氧化物对应水化物的酸性强弱:
(4)元素C的气态氢化物与元素E的最高价氧化物对应水化物化合生成的正盐的化学式为
(5) ①元素B所在周期的简单离子半径最小的是
②元素C、D的简单氢化物沸点较高的是
(6)请用电子式表示Na2S的形成过程
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硼及其化合物的研究在无机化学的发展中占有独特的地位。
(1)硼元素有10B和11B两种天然稳定同位素,在基态11B原子中,价电子中存在______ 对自旋方向相反的电子。第一电离能介于B与N之间的第二周期元素有______ 种。
(2)目前已制得二十多种硼氢化合物,如乙硼烷B2H6、丁硼烷B4H10等在能源方面前景可期。
①NH3能通过配位键与硼元素的某种氢化物作用得到化合物M, M是一种新的储氢材料,加热M 会缓慢释放出H2,并转化为化合物N, M、N分别是乙烷、乙烯的等电子体。M的结构式为______ 须标出配位键),氮原子在M、N分子中的杂化方式分别为_________ 。
②B2H6可作火箭燃料,将B2H6气体通入H2O中的反应为B2H6+6H20=2H3BO3+6H2↑,据此可判断反应中所涉及元素的电负性从小到顺序为_________ 。
③以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,可将竣基直接还原成醇。
CH3C00H CH3CH2OH
CH3CH2OH 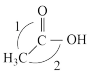
上图中乙酸分子键角1>键角2,其原因为_____________ 。
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,如图1所示。
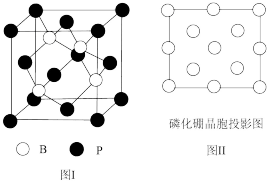
①图II是磷化硼沿Z轴的投影图,请在图II中圆球上涂“ ”和画“×”分别表明B与P的相对位置
”和画“×”分别表明B与P的相对位置_____________ 。
②已知晶胞边长为apm,则磷化硼的密度是______ g/cm3(只要求列算式)。
(1)硼元素有10B和11B两种天然稳定同位素,在基态11B原子中,价电子中存在
(2)目前已制得二十多种硼氢化合物,如乙硼烷B2H6、丁硼烷B4H10等在能源方面前景可期。
①NH3能通过配位键与硼元素的某种氢化物作用得到化合物M, M是一种新的储氢材料,加热M 会缓慢释放出H2,并转化为化合物N, M、N分别是乙烷、乙烯的等电子体。M的结构式为
②B2H6可作火箭燃料,将B2H6气体通入H2O中的反应为B2H6+6H20=2H3BO3+6H2↑,据此可判断反应中所涉及元素的电负性从小到顺序为
③以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,可将竣基直接还原成醇。
CH3C00H
 CH3CH2OH
CH3CH2OH 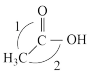
上图中乙酸分子键角1>键角2,其原因为
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,如图1所示。

①图II是磷化硼沿Z轴的投影图,请在图II中圆球上涂“
 ”和画“×”分别表明B与P的相对位置
”和画“×”分别表明B与P的相对位置②已知晶胞边长为apm,则磷化硼的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮可以形成多种离子和分子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)写出N2H62+中共价键的类型除极性键,非极性键外再写出一种__________ 。
(2)下列关于NH2-的说法合理的是____________________ (填字母)。
A.H-N-H夹角109.5° B. H-N-H夹角180° C. H-N-H夹角大约105°
D.中心原子的杂化轨道为四面体形 E. 该离子为V形 F.易与H+结合
(3)写出N3-的等电子体且是中性分子的化学式___________________ (一种)。
(4)N2H4名称是肼,也叫联氨,通常为无色油状发烟液体,有吸湿性,有氨的臭味。可作为火箭的燃料。其沸点比氨气高的主要原因是________________________ 。
利用含N的铜萃取剂M可通过如下反应实现铜离子的富集:
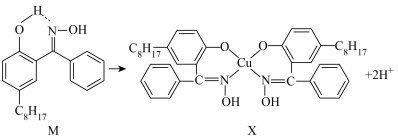
(5)X难溶于水、易溶于有机溶剂,X中配位原子是______ 。
(6)M中氮原子以_______ 杂化轨道与氧原子形成σ键。
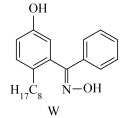
(7)M与W(如图)是同分异构体,则在水中溶解度较大的物质是___ (填字母M或W)。
(8)常用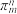 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
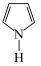
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为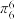 。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为
。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为________ 。
(1)写出N2H62+中共价键的类型除极性键,非极性键外再写出一种
(2)下列关于NH2-的说法合理的是
A.H-N-H夹角109.5° B. H-N-H夹角180° C. H-N-H夹角大约105°
D.中心原子的杂化轨道为四面体形 E. 该离子为V形 F.易与H+结合
(3)写出N3-的等电子体且是中性分子的化学式
(4)N2H4名称是肼,也叫联氨,通常为无色油状发烟液体,有吸湿性,有氨的臭味。可作为火箭的燃料。其沸点比氨气高的主要原因是
利用含N的铜萃取剂M可通过如下反应实现铜离子的富集:

(5)X难溶于水、易溶于有机溶剂,X中配位原子是
(6)M中氮原子以
(7)M与W(如图)是同分异构体,则在水中溶解度较大的物质是

(8)常用
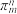 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为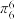 。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为
。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钼酸铋( )和钒酸铋(
)和钒酸铋( )都具有良好的光催化性能。回答下列问题:
)都具有良好的光催化性能。回答下列问题:
(1)已知Mo的价电子排布式为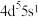 ,则Mo在周期表中的位置为
,则Mo在周期表中的位置为___________ ;基态V原子核外电子排布式为[Ar]___________ 。
(2)制备 的第一步反应为
的第一步反应为 。
。 的空间构型为
的空间构型为___________ ;其中心原子的杂化类型为___________ 。
(3)P与Bi处在同主族,PCl3的熔点为-112℃,沸点为76℃,BiCl3的熔点为232℃,沸点为447℃,其原因是___________ ;BiCl3属于___________ (“极性”或“非极性”)分子。
(4)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各原子的相对位置。钒与形成的晶体晶胞如图所示,其中原子坐标参数A为(0,0,0);B为 。C原子的坐标参数为
。C原子的坐标参数为___________ 。

②晶胞参数:描述晶胞的大小和形状。已知钒与铋形成的晶体晶胞参数为0.587nm。钒与铋之间的最近距离为___________ nm(列出式子,不必计算出结果,下同);该晶体的密度为___________ g·cm-3(阿伏加德罗常数的值为NA)。
 )和钒酸铋(
)和钒酸铋( )都具有良好的光催化性能。回答下列问题:
)都具有良好的光催化性能。回答下列问题:(1)已知Mo的价电子排布式为
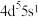 ,则Mo在周期表中的位置为
,则Mo在周期表中的位置为(2)制备
 的第一步反应为
的第一步反应为 。
。 的空间构型为
的空间构型为(3)P与Bi处在同主族,PCl3的熔点为-112℃,沸点为76℃,BiCl3的熔点为232℃,沸点为447℃,其原因是
(4)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各原子的相对位置。钒与形成的晶体晶胞如图所示,其中原子坐标参数A为(0,0,0);B为
 。C原子的坐标参数为
。C原子的坐标参数为
②晶胞参数:描述晶胞的大小和形状。已知钒与铋形成的晶体晶胞参数为0.587nm。钒与铋之间的最近距离为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化铈( )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
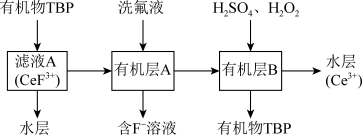
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。
回答下列问题:
(1)滤渣A的主要成分是________ (填化学式);“酸浸”不用盐酸的理由是________ (答一点即可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: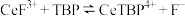 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是________ ,“有机层B”中发生反应的离子方程式为________ 。水层中的一种溶质,理论上可以在工艺流程图中的________ 工序中循环利用,减小“调pH”工序中 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于________ (已知25℃时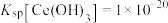 )。
)。
(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为________ 。
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是________ ;晶体中一个Ce周围与其最近的O的个数为________ 。
 )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: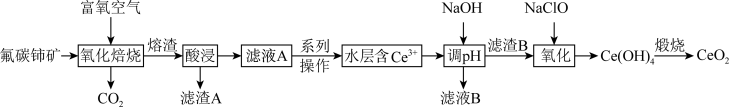
 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。回答下列问题:
(1)滤渣A的主要成分是
(2)“系列操作”包含以下几个过程:已知:
 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: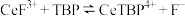 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于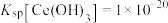 )。
)。(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】ZnGeP2和KTiOPO4都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
(1)基态氧原子核外电子有___________ 种不同的空间运动状态;基态Ti原子的价电子排布式为___________ 。
(2)H2O、KH熔点由高到低的顺序为___________ ,原因是___________ 。
(3)H2O可与H+结合生成H3O+,水中H-O-H的键角比H3O+中的___________ (填“大”或“小”)。H2O2是常用的氧化剂,其分子结构如图1所示。H2O2能与水混溶,却不溶于CCl4的原因是___________ 。
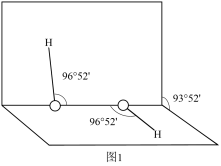
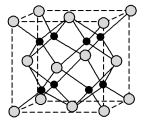
(4)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为___________ ,该晶胞的密度为ρg/cm3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为___________ cm(用含ρ、NA的代数式表示)。
(1)基态氧原子核外电子有
(2)H2O、KH熔点由高到低的顺序为
(3)H2O可与H+结合生成H3O+,水中H-O-H的键角比H3O+中的

(4)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近现代战争中,制造坦克战车最常用的装甲材料是经过轧制和热处理后的合金钢,热处理后整个装甲结构的化学和机械特性和最大限度的保持一致。钢中合金元素的百分比含量为:铬0.5~1.25 镍0.5~1.5 钼0.3~0.6 锰0.8~1.6 碳0.3
(1)铬元素的基态原子的价电子层排布式是_________________ 。
(2)C元素与其同主族下一周期元素组成的晶体中,C原子的杂化方式为_____
(3)Mn和Fe的部分电离能数据如表:
根据表数据,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是_________ 。
(4)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。
某镍配合物结构如右图所示,分子内含有的作用力
有_______________ (填序号)。

A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是__________ 。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是___________
(6)铁能与氮形成一种磁性材料,其晶胞结构如右图所示,则该磁性材料的化学式为_____________

(1)铬元素的基态原子的价电子层排布式是
(2)C元素与其同主族下一周期元素组成的晶体中,C原子的杂化方式为
(3)Mn和Fe的部分电离能数据如表:
| 元 素 | Mn | Fe | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
根据表数据,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是
(4)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。
某镍配合物结构如右图所示,分子内含有的作用力
有

A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是
(6)铁能与氮形成一种磁性材料,其晶胞结构如右图所示,则该磁性材料的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】第IIA族元素在地壳内蕴藏较丰富,其单质和化合物用途广泛。回答下列问题:
(1)基态Ca原子M能层有_______ 个运动状态不同的电子,Mn和Ca属于同一周期,且核外最外层电子构型相同,但金属Mn的熔沸点等都比金属Ca高,原因______ 。
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是_________ ,中心原子的杂化方式为_______ 。
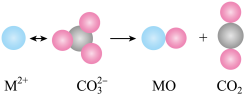
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3__________ (填“高于”或“低于”)SrCO3,原因是_______ 。从成键轨道看,CO2分子内的化学键类型有________ 。
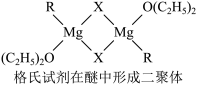
(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键__________ 。
(1)基态Ca原子M能层有
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3

(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)A元素的基态原子价电子排布式:_______ 。
(2)X的化学名称为_______ 。
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:______________ 。
(4)CE、FA的晶格能分别为786 kJ·mol-1、3401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是_______ 。
(5)F与B可形成离子化合物,其晶胞结构如下图所示。F与B形成的离子化合物的化学式为_______ ;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是_______ (只要求列出算式)。

(1)A元素的基态原子价电子排布式:
(2)X的化学名称为
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
(4)CE、FA的晶格能分别为786 kJ·mol-1、3401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是
(5)F与B可形成离子化合物,其晶胞结构如下图所示。F与B形成的离子化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
则,A的化合价_________ B的化合价(填“>”、“<”或“=”)。
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:

则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:______ ,原因是:________ 。
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是_______ 。
(4)某配合物的分子结构如下图所示,

则N原子的杂化方式为_______ ;基态Ni原子的电子排布式________ 。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
则,A的化合价
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(4)某配合物的分子结构如下图所示,

则N原子的杂化方式为
您最近一年使用:0次



