磷及其化合物在电池、催化等领域有重要应用。回答下列问题:
(1)黑磷与石墨类似,也具有层状结构(如图所示)。______ 种。
②下列说法错误的是______ (填字母)。
A.黑磷分子中所用化学键的键能不完全相同 B.黑磷与石墨都属于混合型晶体
C.黑磷中P原子的杂化方式为sp3 D.黑磷分子中存在大π键,易导电
(2)LiPF6、LiAsF6等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。______ (填“物理”或“化学”)变化。
②相同条件下,使用______ (填“LiPF6”或“LiAsF6”)作电极材料时,Li+迁移速率较快,原因是_____ 。
(3)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。______ 。
②若晶胞参数为anm,则晶体的密度为______ g•cm-3(列出计算式)。
(1)黑磷与石墨类似,也具有层状结构(如图所示)。

②下列说法错误的是
A.黑磷分子中所用化学键的键能不完全相同 B.黑磷与石墨都属于混合型晶体
C.黑磷中P原子的杂化方式为sp3 D.黑磷分子中存在大π键,易导电
(2)LiPF6、LiAsF6等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。
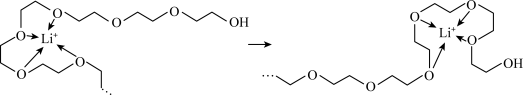
②相同条件下,使用
(3)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。
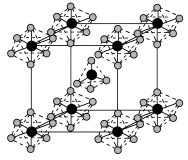
②若晶胞参数为anm,则晶体的密度为
2023·福建龙岩·模拟预测 查看更多[4]
更新时间:2023-03-04 19:56:05
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为_____ 。
(2)NO3-中氮原子轨道的杂化类型是_____ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为_____ 。
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是_____ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有_____ 。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为_____ 。

(1)Mn3+基态核外电子排布式为
(2)NO3-中氮原子轨道的杂化类型是
(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硼及其化合物在现代工业、生活和国防中有重要应用价值。
(1)硼原子的电子排布式是_____ 。
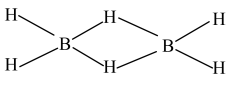
(2)最简单的硼烷是B2H6(乙硼烷),结构见图,其中B原子的杂化方式为_____ 。
(3)BF3和BCl3都有强烈接受孤电子对的倾向,如三氟化硼气体与氨气相遇,立即生成白色固体,写出该白色固体结构式,并标注出其中的配位键_____ 。
(4)近年来,人们肯定硼是人和动物氟中毒的重要解毒剂。硼在体内可与氟形成稳定的配合物____ ,并以和氟相同的途径参加体内代谢,但毒性比氟小,且易随尿排出,故认为硼对氟化物具有解毒作用。
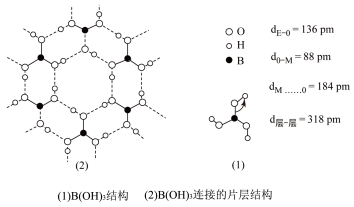
(5)经结构研究证明,硼酸晶体中B(OH)3单元结构如图(1)所示。各单元中的氧原子通过O—H…O氢键连结成层状结构如图(2)所示。层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
①H3BO3是一元弱酸,写出它与水反应的化学方程式_______ ,
②根据结构判断下列说法正确的是_______ 。
a.硼酸晶体属于原子晶体
b.硼酸晶体有鳞片状的外层
c.硼酸晶体是分子晶体
d.硼酸晶体有滑腻感,可作润滑剂
e.在B(OH)3单元中,B原子以sp3杂化轨道和氧原子结合而成
f.H3BO3分子的稳定性与氢键有关
g.含1mol H3BO3的晶体中有3mol氢键
h.分子中硼原子最外层为8e-稳定结构
③硼酸常温下为白色片状晶体,溶于水(273K时溶解度为6.35),在热水中溶解度明显增大(373K时为27.6)。请分析其中原因_______ 。
(1)硼原子的电子排布式是
(2)最简单的硼烷是B2H6(乙硼烷),结构见图,其中B原子的杂化方式为

(3)BF3和BCl3都有强烈接受孤电子对的倾向,如三氟化硼气体与氨气相遇,立即生成白色固体,写出该白色固体结构式,并标注出其中的配位键
(4)近年来,人们肯定硼是人和动物氟中毒的重要解毒剂。硼在体内可与氟形成稳定的配合物
(5)经结构研究证明,硼酸晶体中B(OH)3单元结构如图(1)所示。各单元中的氧原子通过O—H…O氢键连结成层状结构如图(2)所示。层与层之间以微弱的分子间力相结合构成整个硼酸晶体。

①H3BO3是一元弱酸,写出它与水反应的化学方程式
②根据结构判断下列说法正确的是
a.硼酸晶体属于原子晶体
b.硼酸晶体有鳞片状的外层
c.硼酸晶体是分子晶体
d.硼酸晶体有滑腻感,可作润滑剂
e.在B(OH)3单元中,B原子以sp3杂化轨道和氧原子结合而成
f.H3BO3分子的稳定性与氢键有关
g.含1mol H3BO3的晶体中有3mol氢键
h.分子中硼原子最外层为8e-稳定结构
③硼酸常温下为白色片状晶体,溶于水(273K时溶解度为6.35),在热水中溶解度明显增大(373K时为27.6)。请分析其中原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式________________________ 。
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为_______ 个、_______ 个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为______________ 、_______ (各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。
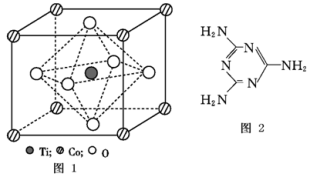
三聚氰胺分子中氮原子轨道杂化类型是______ ,1 mol三聚氰胺分子中σ键的数目为_______ 。
(1)写出基态Mn原子的核外电子排布式
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。

三聚氰胺分子中氮原子轨道杂化类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示,回答下列问题:
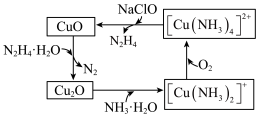
(1)[Cu(NH3)4]2+是一种常见的配离子,其结构式为_____________ ,配位原子为_______________ 。
(2)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是______________________ 。
(3)NaClO发生水解可生成HClO。HClO的空间构型是_______ ,中心原子的杂化类型是_______ 。
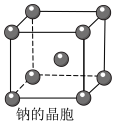
(4)钠晶胞结构如图所示,配位数为____________ 。若钠晶胞的边长为c cm,NA代表阿伏加德罗常数的值,则钠晶体的密度为____________ g·cm-3。

(1)[Cu(NH3)4]2+是一种常见的配离子,其结构式为
(2)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是
(3)NaClO发生水解可生成HClO。HClO的空间构型是
(4)钠晶胞结构如图所示,配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家研究发现 (
(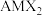 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子M层的电子排布式为_______ ;基态硫原子核外电子中含有_______ 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为_______ (用元素符号表示),O、S为同主族元素, 的键角比
的键角比 大的原因是
大的原因是_______ 。
(3)硫元素能形成多种微粒如 、
、 、
、 、
、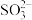 、
、 等,
等, 的中心原子的价层电子对数为
的中心原子的价层电子对数为_______ , 的空间构型为
的空间构型为_______ 。
(4)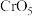 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为_______ (填标号)。
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为_______ ;与Cr最近的氧原子的个数为_______ ; 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为_______  (填含a、
(填含a、 的表达式)。
的表达式)。

 (
(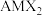 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:(1)基态铬原子M层的电子排布式为
(2)同周期元素Si、P、S的电负性由大到小的顺序为
 的键角比
的键角比 大的原因是
大的原因是(3)硫元素能形成多种微粒如
 、
、 、
、 、
、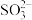 、
、 等,
等, 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的空间构型为
的空间构型为(4)
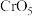 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为 |  | 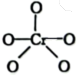 |
| A | B | C |
 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为 (填含a、
(填含a、 的表达式)。
的表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氮元素可以形成多种化合物。肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。已知肼可用作火箭燃料,燃烧时发生的反应为N2O4(g)+2N2H4(g)=3N2(g)+4H2O(g) △H=-1040kJ•mol-1。回答下列问题:
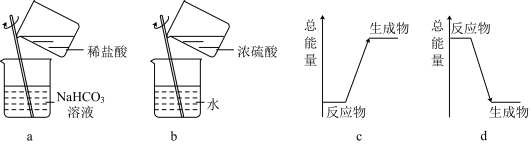
(1)该反应的能量变化与如图所示能量变化不相符的是______ (填标号)。
(2)该反应每放出520kJ热量,同时有_____ molσ键形成,有_____ molN-H键断裂。
(3)N2H4的电子式可表示为______ ,该分子中N原子的杂化方式为______ 。
(4)叠氮化合物在化学工业上有重要的应用。N 被称为叠氮离子,1个N
被称为叠氮离子,1个N 中含有
中含有_____ 个电子;请写出与N 具有等电子数的物质的化学式:
具有等电子数的物质的化学式:_____ (写一种)。
(1)该反应的能量变化与如图所示能量变化不相符的是

(2)该反应每放出520kJ热量,同时有
(3)N2H4的电子式可表示为
(4)叠氮化合物在化学工业上有重要的应用。N
 被称为叠氮离子,1个N
被称为叠氮离子,1个N 中含有
中含有 具有等电子数的物质的化学式:
具有等电子数的物质的化学式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛被视为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”,钛和钛的化合物在航天、化工、建筑、医疗中都有着广泛的用途。回答下列问题:
(1)基态钛原子核外有_______ 种能量不同的电子,其能量最高的电子所在的能层符号为_______ 。
(2)钛与卤素形成的化合物TiX4熔点如下表
TiCl4、TiBr4、TiI4熔点依次升高的原因_______ 。
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①Ti(BH4)3中所含元素电负性由小到大的顺序为_______ 。
②TiCl4 与SiCl4结构相似,TiCl4的中心原子价层电子对数_______ 。
③LiBH4 由Li+和BH 构成,BH
构成,BH 中B原子的杂化类型是
中B原子的杂化类型是_______ 。
④LiBH4存在_______ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
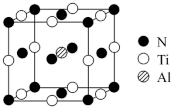
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,已知该晶体的晶胞参数(棱边边长)为a pm,用Al掺杂TiN后,其晶胞结构如下图所示,距离Al最近的Ti有_______ 个,掺杂Al后的晶体密度是TiN晶体的_______ 倍(写出含a的表达式)。
(1)基态钛原子核外有
(2)钛与卤素形成的化合物TiX4熔点如下表
| TiX4 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点℃ | 377 | -24 | 38.3 | 153 |
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①Ti(BH4)3中所含元素电负性由小到大的顺序为
②TiCl4 与SiCl4结构相似,TiCl4的中心原子价层电子对数
③LiBH4 由Li+和BH
 构成,BH
构成,BH 中B原子的杂化类型是
中B原子的杂化类型是④LiBH4存在
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,已知该晶体的晶胞参数(棱边边长)为a pm,用Al掺杂TiN后,其晶胞结构如下图所示,距离Al最近的Ti有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬(Cr)18%、含镍(Ni)8%等。回答下列问题:
(1)碳的价电子层的电子排布式为___________ ;石墨烯(即单层石墨)是一种碳原子构成的单层二维蜂窝状晶格结构的新材料,其中碳原子采取___________ 杂化。
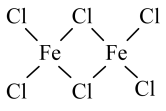
(2)铁的氯化物FeCl3蒸汽状态下以双聚分子形式存在(如图),其中Fe的配位数为___________ ,双聚分子中存在配位键,提供空轨道的是___________ 原子。
(3)O、F、Cl电负性由大到小的顺序为___________ ;OF2分子的空间构型为___________ ;OF2的熔、沸点___________ (填“高于”或“低于”)Cl2O,原因是___________ 。
(4)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为___________ cm(用含NA的表达式表示)。

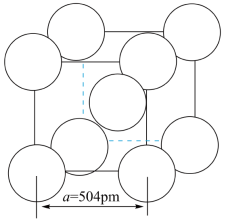
(5) 晶体中
晶体中 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 主要分布在由
主要分布在由 构成的四面体、八面体等空隙中。已知阿伏加德罗常数为
构成的四面体、八面体等空隙中。已知阿伏加德罗常数为 ,则
,则 晶体的摩尔体积
晶体的摩尔体积
___________  (列出算式)。
(列出算式)。
(1)碳的价电子层的电子排布式为
(2)铁的氯化物FeCl3蒸汽状态下以双聚分子形式存在(如图),其中Fe的配位数为

(3)O、F、Cl电负性由大到小的顺序为
(4)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为

(5)
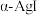 晶体中
晶体中 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 主要分布在由
主要分布在由 构成的四面体、八面体等空隙中。已知阿伏加德罗常数为
构成的四面体、八面体等空隙中。已知阿伏加德罗常数为 ,则
,则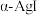 晶体的摩尔体积
晶体的摩尔体积
 (列出算式)。
(列出算式)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
③查阅资料得知:离子晶体的熔点一般较高,在600~2000℃,共价晶体具有较高的熔点,一般在1000℃以上。
回答下列问题:
(1)基态As的价层电子轨道表示式为_______ 。
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为______ 。
(3)向碱浸液中加盐酸调节pH=4,有TeO2析出,分离TeO2,滤液中As元素最主要的存在形式为_______ (常温下,H3AsO4的各级电离常数:Ka1=6.3×10-3、Ka2=1.0×10-7、Ka3=3.2×10-12,填字母)。
(4)“氯盐酸浸”时,通入SO2的目的是_______ 。
(5)“水解”时,生成SbOCl的化学方程式为_______ 。
(6)TeO2可用作电子元件材料,熔点为733℃,其熔点远高于SO2的原因为______ 。TeO2晶胞是长方体结构(如图所示),已知NA为阿伏加德罗常数的值,则该晶体的密度为______ g•cm-3(列出计算表达式)。


已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
③查阅资料得知:离子晶体的熔点一般较高,在600~2000℃,共价晶体具有较高的熔点,一般在1000℃以上。
回答下列问题:
(1)基态As的价层电子轨道表示式为
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为
(3)向碱浸液中加盐酸调节pH=4,有TeO2析出,分离TeO2,滤液中As元素最主要的存在形式为
| A.H3AsO4 | B.H2As | C.HAsO | D.AsO |
(4)“氯盐酸浸”时,通入SO2的目的是
(5)“水解”时,生成SbOCl的化学方程式为
(6)TeO2可用作电子元件材料,熔点为733℃,其熔点远高于SO2的原因为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】SiC又叫金刚砂,是砂轮的主要成分,可看作是金刚石里一半碳原子被硅原子替换的产物。
(1)工业上用焦炭和石英在高温下反应制得SiC:3C+SiO2 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为________ 。
(2)SiC晶体中有两个含五个原子的基本结构单元,分别是__________ 和_________ 。
(3)SiC晶体中最小的原子环是____ 元环,该环独立有___ 个Si原子,_____ 个C原子。
(4)1molSiC晶体中含____ mol Si-C键。
(5)金刚石、SiC晶体、晶体Si 熔点由高到低的顺序_____________ 。
(1)工业上用焦炭和石英在高温下反应制得SiC:3C+SiO2
 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为(2)SiC晶体中有两个含五个原子的基本结构单元,分别是
(3)SiC晶体中最小的原子环是
(4)1molSiC晶体中含
(5)金刚石、SiC晶体、晶体Si 熔点由高到低的顺序

您最近一年使用:0次
【推荐2】【化学—物质结构与性质】
(1)下列叙述正确的是________ 。
a.含有金属阳离子的晶体一定是离子晶体
b.化合物硫氰化铁和氢氧化二氨合银中都存在配位键
c.KCl、HF、CH3CH2OH、SO2都易溶于水,且原因相同
d.MgO的熔点比NaCl的高,主要是因为MgO的晶格能大于NaCl的晶格能
(2)氨基酸是蛋白质的基石,甘氨酸是最简单的氨基酸(结构如图),

在甘氨酸分子中,N原子的杂化形式是_____ ,在甘氨酸分子中C、N、O原子的第一电离能从大到小的顺序是_______ ;氮可以形成多种离子,如N3-、NH2-、NH4+、N2H5+等,其中,NH4+的空间构型是____ 。
(3)已知MO与CsCl的结构相似(如图所示),MO晶体的密度为p g·cm-3,NA为阿伏加德罗常数,相邻的两个M2+的核间距为acm。写出Cs基态原子的价电子排布式______ ,MO的相对分子质量可以表示为_____ 。

(1)下列叙述正确的是
a.含有金属阳离子的晶体一定是离子晶体
b.化合物硫氰化铁和氢氧化二氨合银中都存在配位键
c.KCl、HF、CH3CH2OH、SO2都易溶于水,且原因相同
d.MgO的熔点比NaCl的高,主要是因为MgO的晶格能大于NaCl的晶格能
(2)氨基酸是蛋白质的基石,甘氨酸是最简单的氨基酸(结构如图),

在甘氨酸分子中,N原子的杂化形式是
(3)已知MO与CsCl的结构相似(如图所示),MO晶体的密度为p g·cm-3,NA为阿伏加德罗常数,相邻的两个M2+的核间距为acm。写出Cs基态原子的价电子排布式

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)下列状态的钙中,电离最外层一个电子所需能量最大的是_____(填标号);
(2)写出基态 离子的M层电子排布式
离子的M层电子排布式_____ 。
(3)实验室常用 检验
检验 ,
, 中
中 的配位数为
的配位数为_____ , 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为_____ 杂化。
(4)已知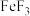 的熔点(1000℃)显著高于
的熔点(1000℃)显著高于 的熔点(306C),原因是
的熔点(306C),原因是_____ 。
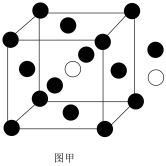
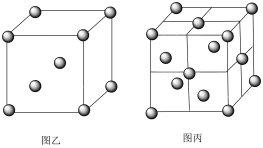
(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图甲所示,写出该反应的化学方程式:_____ 。 _____ ,图乙中铁原子沿着晶胞体对角线相切,图丙中铁原子沿着晶胞面对角线相切。若两种晶体中铁原子半径相同,则两种铁晶体中密度较高的是_____ 。(填“图乙”或“图丙”)
(1)下列状态的钙中,电离最外层一个电子所需能量最大的是_____(填标号);
A. 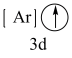 | B. 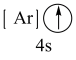 | C. 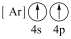 | D. 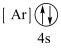 |
(2)写出基态
 离子的M层电子排布式
离子的M层电子排布式(3)实验室常用
 检验
检验 ,
, 中
中 的配位数为
的配位数为 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为(4)已知
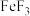 的熔点(1000℃)显著高于
的熔点(1000℃)显著高于 的熔点(306C),原因是
的熔点(306C),原因是(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图甲所示,写出该反应的化学方程式:
您最近一年使用:0次



