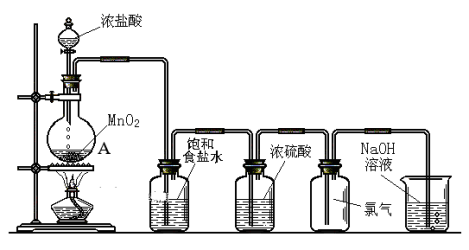
如图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放有脱脂棉。
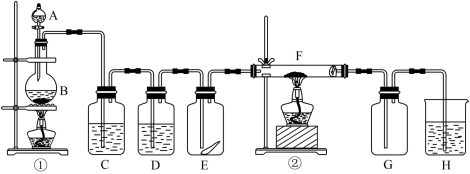
试回答:
(1)A试剂为_____ ,B试剂为_____ ,离子方程式为_____ 。
(2)C试剂为_____ ;D试剂作用为_____ 。
(3)E中干燥红色布条_____ (填“褪色”或“不褪色”)。
(4)F管中现象_____ ,脱脂棉的作用是_____ 。
(5)H中试剂为_____ ,离子方程式为_____ 。

试回答:
(1)A试剂为
(2)C试剂为
(3)E中干燥红色布条
(4)F管中现象
(5)H中试剂为
更新时间:2023-03-29 18:51:48
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一、
(1)写出用该方法制取氯气的化学方程式_______ 。
(2)某同学应用该方法,按照制备、净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)能达到实验目的的是_______ 。
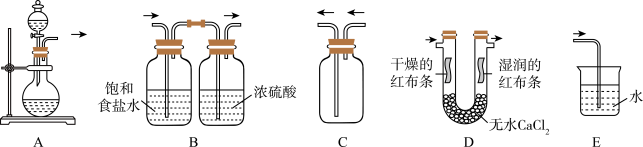
(3)写出上述D装置中Cl2经过湿润红布条时发生反应的离子方程式_______ 。
(4)验证氯水中HClO光照分解的产物。将新制的氯水加入三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图1),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。(酸性溶液中, 越大,pH越小,溶液酸性越强)
越大,pH越小,溶液酸性越强)

若能够证明氯水中HClO在光照下发生了分解反应,则图2中纵坐标可以表示的物理量是_______ (填字母)
a.氢离子的浓度 b.氯离子的浓度 c.氯水的pH d.氧气的体积分数
(5)某化工厂用氯气与氢氧化钙生产漂白粉。该厂出厂产品说明书如图3:
①漂白粉的有效成分是_______ (填化学式)。漂白粉需“密封避光保存于阴凉处”是因为漂白粉有效成分与空气中 、
、 反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为
反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为_______ 。
②使用漂白粉时最好“随用随配”。某次使用时,取漂白粉2.54 g溶解于1000 g水中,所得溶液中次氯酸钙的物质的量浓度为_______ (假设漂白粉中只含有次氯酸钙和氯化钙,不含其它杂质,且所得溶液的体积仍为1 L)
(1)写出用该方法制取氯气的化学方程式
(2)某同学应用该方法,按照制备、净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)能达到实验目的的是

(3)写出上述D装置中Cl2经过湿润红布条时发生反应的离子方程式
(4)验证氯水中HClO光照分解的产物。将新制的氯水加入三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图1),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。(酸性溶液中,
 越大,pH越小,溶液酸性越强)
越大,pH越小,溶液酸性越强)
若能够证明氯水中HClO在光照下发生了分解反应,则图2中纵坐标可以表示的物理量是
a.氢离子的浓度 b.氯离子的浓度 c.氯水的pH d.氧气的体积分数
(5)某化工厂用氯气与氢氧化钙生产漂白粉。该厂出厂产品说明书如图3:
①漂白粉的有效成分是
 、
、 反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为
反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为②使用漂白粉时最好“随用随配”。某次使用时,取漂白粉2.54 g溶解于1000 g水中,所得溶液中次氯酸钙的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室用二氧化锰和浓盐酸反应制取氯气并探究其性质,实验装置如图所示。
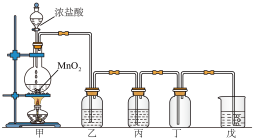
(1)装置甲中发生的离子方程式为________ ;其中二氧化锰为________ 剂。
(2)装置乙中盛放的试剂为________ ;装置丙的作用为________ 。
(3)将干燥的氯气与干燥的有色纸条接触,纸条________ (填“有”或“无”)变化,若与湿润的有色纸条接触,现象为________ 。
(4)装置戊的作用为________ ,戊中反应化学方程式为________ 。

(1)装置甲中发生的离子方程式为
(2)装置乙中盛放的试剂为
(3)将干燥的氯气与干燥的有色纸条接触,纸条
(4)装置戊的作用为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】现有X、Y、Z、W四种元素,其原子序数依次递增。已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④ 两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
⑥由Y、Z、W三种元素组成的化合物M受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)化合物M的化学式为_______ ,1molM中含有的电子的物质的量为_______ 。
(2)用化学方程式表示Z单质的实验室检验方法_______ 。
(3)写出Z的单质溶于X2Y中反应的化学方程式:_______ ,若该反应中有2mol电子发生转移,则参加反应的Z单质在标况下的体积为_______ 。
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④ 两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
⑥由Y、Z、W三种元素组成的化合物M受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)化合物M的化学式为
(2)用化学方程式表示Z单质的实验室检验方法
(3)写出Z的单质溶于X2Y中反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某兴趣小组设计实验制取Cl2并验证Cl2的氧化性。回答下列问题:
(1)用K2MnO4与浓盐酸反应制取Cl2,装置如图甲:
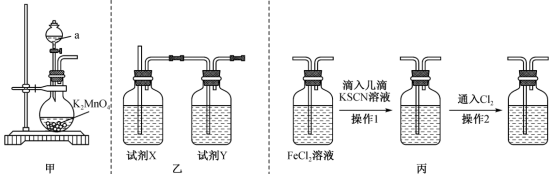
①反应的化学方程式为K2MnO4+8HCl(浓)=MnCl2+2Cl2↑+2KCl+4H2O,该反应中氧化剂为__________ (填化学式),若生成5.6 L Cl2(标准状况),则被氧化的盐酸为__________ mol。
②制取的Cl2中含有的杂质有__________ (填化学式),通过乙装置除去该杂质,则试剂X、试剂Y依次为__________ (填字母)。
A.饱和食盐水、碱石灰 B.饱和食盐水、浓硫酸 C.浓硫酸、饱和食盐水
(2)用图丙所示装置验证Cl2的氧化性。操作1后观察到现象为_________________________ ,操作2后观察到现象为________________________________________ ,产生操作2后现象的原因是__________________________________________ (用必要的语言和离子方程式说明)。
(3)KMnO4、K2MnO4均能与浓盐酸反应制取Cl2,充分反应后Mn元素的化合价均降为+2,消耗等物质的量的KMnO4、K2MnO4产生Cl2的体积(标准状况)更大的是__________ (填“KMnO4”或“K2MnO4”)。
(1)用K2MnO4与浓盐酸反应制取Cl2,装置如图甲:

①反应的化学方程式为K2MnO4+8HCl(浓)=MnCl2+2Cl2↑+2KCl+4H2O,该反应中氧化剂为
②制取的Cl2中含有的杂质有
A.饱和食盐水、碱石灰 B.饱和食盐水、浓硫酸 C.浓硫酸、饱和食盐水
(2)用图丙所示装置验证Cl2的氧化性。操作1后观察到现象为
(3)KMnO4、K2MnO4均能与浓盐酸反应制取Cl2,充分反应后Mn元素的化合价均降为+2,消耗等物质的量的KMnO4、K2MnO4产生Cl2的体积(标准状况)更大的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】无水三氯化铁呈棕红色、易潮解,在100 ℃左右时升华。设计如下实验,用来制取纯净、无水的FeCl3。

主要步骤:(1)加热浓盐酸和MnO2的混合物制取Cl2,请完成化学方程式:____________ 。
(2)________ 物质可净化Cl2,___________ 物质可干燥Cl2。
(3)净化干燥后的Cl2与Fe加热生成FeCl3
(4)过量的Cl2用NaOH溶液吸收,可制备________________ 。
【化学与生活】

主要步骤:(1)加热浓盐酸和MnO2的混合物制取Cl2,请完成化学方程式:
(2)
(3)净化干燥后的Cl2与Fe加热生成FeCl3
(4)过量的Cl2用NaOH溶液吸收,可制备
【化学与生活】
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某化学兴趣小组欲在实验室探究氯气氧化性并模拟工业制取漂白粉,设计如图装置进行实验:

(1)圆底烧瓶中发生反应的离子方程式为
(2)装置的连接顺序为
(3)淀粉KI溶液的现象为
(4)与石灰乳反应制取漂白粉的化学方程式为
(5)NaOH溶液的作用为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室制取并收集氯气的装置如图所示,请回答下列问题:

(1)写出HCl的电子式_______ 。
(2)在装置中:①饱和食盐水的作用是_______ ,②浓硫酸的作用是_______ 。
(3)化学实验中检验是否有 产生常用湿润的淀粉
产生常用湿润的淀粉 试纸。如果有
试纸。如果有 产生,可观察到的现象是
产生,可观察到的现象是_______ 。
(4)写出尾气吸收装置中进行的反应的离子方程式_______ 。

(1)写出HCl的电子式
(2)在装置中:①饱和食盐水的作用是
(3)化学实验中检验是否有
 产生常用湿润的淀粉
产生常用湿润的淀粉 试纸。如果有
试纸。如果有 产生,可观察到的现象是
产生,可观察到的现象是(4)写出尾气吸收装置中进行的反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】如图中A~H均为中学化学中常见的物质,A、B、H是气体,其中A为黄绿色气体,它们之间有如下转化关系。(反应中生成的水已略去)

请回答以下问题:
(1) F是____________________ , (填化学式)。
(2)C物质在日常生活中可作______________________ 剂。
(3)写出反应①的化学方程式:____________________________________________ 。
(4)写出反应⑤的化学方程式:_____________________________________ 。

请回答以下问题:
(1) F是
(2)C物质在日常生活中可作
(3)写出反应①的化学方程式:
(4)写出反应⑤的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某实验小组对中学课本中可生成氢气的反应进行了研究,总结出两个可以生成H2的反应:①Zn+盐酸,②Na+水。为点燃上述两个反应生成的H2,他们设计了图示装置。请回答下列问题:

(1)写出Na与H2O反应的化学方程式:___________ 。
(2)实验小组在点燃用上述装置制得的H2时,①实验获得成功,②却失败了。他们分析认为失败的原因是Na的用量太少,Na与H2O的反应速率太快。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是___________ 。
(3)实验小组查阅钠、煤油、水的密度分别为0.97g·cm-3、0.80g·cm-3、1.00g·cm-3,并据此对实验进行改进。在改进后的实验中H2的生成速率减慢,原因是___________ 。

(1)写出Na与H2O反应的化学方程式:
(2)实验小组在点燃用上述装置制得的H2时,①实验获得成功,②却失败了。他们分析认为失败的原因是Na的用量太少,Na与H2O的反应速率太快。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是
(3)实验小组查阅钠、煤油、水的密度分别为0.97g·cm-3、0.80g·cm-3、1.00g·cm-3,并据此对实验进行改进。在改进后的实验中H2的生成速率减慢,原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如下图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:
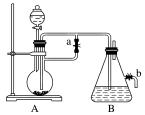
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是_______ 。A中反应的离子方程式是_______ 。
(2)实验开始时先将止水夹a_______ (填“打开”或“关闭”)。
(3)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式为_______ 。

(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是
(2)实验开始时先将止水夹a
(3)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】过氧化钙是一种温和的氧化剂,常温下为白色固体,易溶于酸,难溶于水、乙醇等溶剂。
(1)某实验小组拟选用如图装置(部分固定装置略)制备过氧化钙,按气流方向连接顺序为___________ (填仪器接口的字母编号,装置可重复使用)。
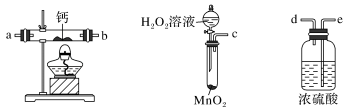
实验步骤如下:
①___________ 后,装入药品;
②打开分液漏斗活塞,通入一段时间气体,加热药品;
③反应结束后,先熄灭酒精灯,待反应管冷却至室温后,停止通入气体;
④拆除装置,取出产物。
实验步骤③的操作目的是___________ 。
(2)利用反应Ca2++H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH ,在碱性环境下制取CaO2·8H2O的装置如下:
,在碱性环境下制取CaO2·8H2O的装置如下:

①仪器C的名称为___________ ;反应结束后,经___________ (填操作名称)、洗涤、低温烘干可获得CaO2·8H2O。
②装置A试管中反应的化学方程式为___________ ;装置B中用冰水浴控制温度,其可能的原因是___________ 。
③化工生产中可用装置A所制气体的浓溶液检验氯气管道是否泄漏,能看到的现象是___________ 。
(1)某实验小组拟选用如图装置(部分固定装置略)制备过氧化钙,按气流方向连接顺序为

实验步骤如下:
①
②打开分液漏斗活塞,通入一段时间气体,加热药品;
③反应结束后,先熄灭酒精灯,待反应管冷却至室温后,停止通入气体;
④拆除装置,取出产物。
实验步骤③的操作目的是
(2)利用反应Ca2++H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH
 ,在碱性环境下制取CaO2·8H2O的装置如下:
,在碱性环境下制取CaO2·8H2O的装置如下:
①仪器C的名称为
②装置A试管中反应的化学方程式为
③化工生产中可用装置A所制气体的浓溶液检验氯气管道是否泄漏,能看到的现象是
您最近一年使用:0次