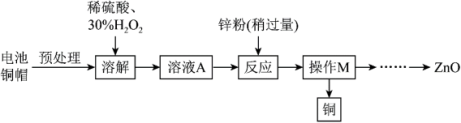
从砷化镓废料(主要成分为GaAs、 ,
, 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
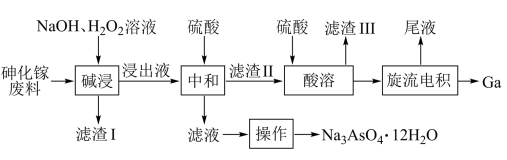
已知:① 是两性氢氧化物,25℃时,
是两性氢氧化物,25℃时, 的溶度积
的溶度积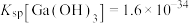 ,电离常数
,电离常数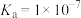 ;②溶液中微粒的浓度不大于
;②溶液中微粒的浓度不大于 时,可认为该微粒沉淀完全。下列说法错误的是
时,可认为该微粒沉淀完全。下列说法错误的是
 ,
, 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
已知:①
 是两性氢氧化物,25℃时,
是两性氢氧化物,25℃时, 的溶度积
的溶度积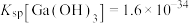 ,电离常数
,电离常数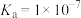 ;②溶液中微粒的浓度不大于
;②溶液中微粒的浓度不大于 时,可认为该微粒沉淀完全。下列说法错误的是
时,可认为该微粒沉淀完全。下列说法错误的是| A.“碱浸”时,温度不能过高也不能过低 |
B.“碱浸”时,GaAs发生反应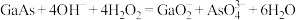 |
| C.为提高镓的回收率,加硫酸中和时,pH的最大值是5 |
| D.“旋流电积”所得“尾液”可循环利用 |
2023·全国·模拟预测 查看更多[4]
(已下线)2023年普通高中学业水平选择性考试化学押题卷(六)(已下线)2023年湖南卷高考真题变式题(选择题6-10)河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题(已下线)选择题11-15
更新时间:2023-04-21 11:23:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法中不正确的是
A.某温度时的混合溶液中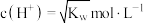 ,说明该溶液呈中性 ,说明该溶液呈中性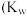 为该温度时水的离子积常数 为该温度时水的离子积常数 |
B.常温下,由水电离出的 的溶液的pH可能为2或12 的溶液的pH可能为2或12 |
C.已知 , ,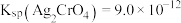 ,向含有 ,向含有 、 、 且浓度均为 且浓度均为 的溶液中逐滴加入 的溶液中逐滴加入 的 的 溶液时, 溶液时, 先产生沉淀 先产生沉淀 |
D.常温下 的 的 和 和 混合溶液中, 混合溶液中,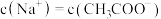 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,取一定量的PbI2固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如图所示。下列有关说法正确的是
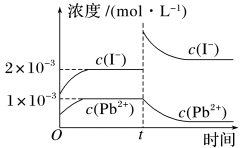

| A.常温下,PbI2的Ksp为2×10-6 |
| B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,平衡向生产沉淀的方向移动,Pb2+的浓度减小 |
| C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI2的Ksp增大 |
D.常温下,Ksp(PbS)=8×10-28,向PbI2的悬浊液中加入Na2S溶液,反应PbI2(s)+S2-(aq) PbS(s)+2I-(aq)的平衡常数为5×1018 PbS(s)+2I-(aq)的平衡常数为5×1018 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】习近平总书记视察赣州时强调,稀土是重要的战略资源,也是不可再生资源。钪(Sc)是一种稀土金属,从钛白酸性废水(主要含有 、
、 ,还含有微量
,还含有微量 )中富集钪,并制备氧化钪(
)中富集钪,并制备氧化钪( )的工艺流程如图所示[已知:
)的工艺流程如图所示[已知: 、
、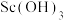 均难溶于水]。下列说法错误的是
均难溶于水]。下列说法错误的是

 、
、 ,还含有微量
,还含有微量 )中富集钪,并制备氧化钪(
)中富集钪,并制备氧化钪( )的工艺流程如图所示[已知:
)的工艺流程如图所示[已知: 、
、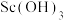 均难溶于水]。下列说法错误的是
均难溶于水]。下列说法错误的是
A.酸洗时加入 的目的是将 的目的是将 氧化为 氧化为 |
| B.实验室进行“操作Ⅰ”需要的玻璃仪器有烧杯、玻璃棒、漏斗 |
C.“滤渣Ⅰ”的成分是 、 、 |
D.草酸钪焙烧时反应的化学方程式: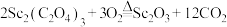 |
您最近一年使用:0次
单选题
|
适中
(0.65)
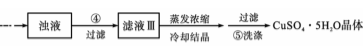
【推荐2】实验室用含有杂质(FeO、Fe2O3)的废CuO 制备胆矾晶体,经历了下列过程(已知Fe3+在pH=3.2时沉淀完全 。下列分析不正确的是
。下列分析不正确的是
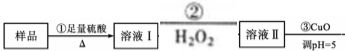
 。下列分析不正确的是
。下列分析不正确的是

| A.配制240mL1mol/L的CuSO4溶液,需称量CuSO4∙5H2O的质量为62.5g |
| B.步骤②目的是将溶液Ⅰ中的Fe2+充分转化为Fe3+,实验操作可用足量的O3代替H2O2 |
| C.步骤③用CuCO3、Cu(OH)2代替CuO 也可调节溶液的pH而不影响实验结果 |
| D.步骤⑤的操作为:向漏斗中加入少量冷的蒸馏水,至浸没晶体,用玻璃棒搅拌均匀,液体流尽后,重复三次 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】锰白(MnCO3,受热易分解)是生产锰盐的初始原料,工业上合成锰白的流程如图所示,下列说法中错误的是


| A.碱浸的目的是为了除去Al2O3和SiO2,二者均能和NaOH溶液反应 |
| B.”还原”步骤中氧化剂和还原剂的物质的量之比为2:1 |
| C.用盐酸和氯化钡溶液可检验锰白是否洗涤干净 |
| D.“低温烘干”可避免温度过高导致MnCO3分解,提高产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于氧气的说法中,不正确的是
| A.氧气能支持燃烧,所以氧气可作燃烧 |
| B.氧气能使带火星的木条复燃 |
| C.红磷在氧气中燃烧。产生浓厚的白烟 |
| D.实验室加热高锰酸钾制取氧气时,试管内靠近导管处放一团蓬松的棉花 |
您最近一年使用:0次

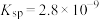 ,现将浓度为
,现将浓度为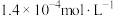 的
的 溶液与
溶液与 溶液等体积混合,若要产生沉淀,则所用
溶液等体积混合,若要产生沉淀,则所用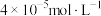
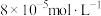
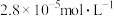
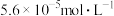
 及杂质
及杂质 、
、
 的转化率
的转化率 再通
再通 ,滤液1中浓度最大的阴离子为
,滤液1中浓度最大的阴离子为