锌的氯化物与氨水反应可形成配合物 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.该配合物的配体为 |
| B.该配合物中含有极性共价键、离子键 |
C.在 中, 中, 提供孤对电子, 提供孤对电子, 提供空轨道 提供空轨道 |
D.氨水的电离方程式为 |
更新时间:2023-04-27 14:13:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】表示下列变化的化学用语正确的是
A.NaHS溶液显碱性:HS-+H2O H3O++S2- H3O++S2- |
B.NaHSO4在水溶液中的电离方程式:NaHSO4=Na++HSO |
C.MgCl2溶液显酸性:Mg2++2H2O Mg(OH)2+2H+ Mg(OH)2+2H+ |
| D.铁在潮湿空气中被腐蚀的负极反应式:Fe-3e-=Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列溶液显酸性,解释其原因的化学用语错误的是
A.碳酸溶液:H2CO3⇌2H++ |
B.硫酸溶液:H2SO4=2H++ |
C.硫酸氢钠溶液:NaHSO4=Na++H++ |
D.NH4Cl溶液: +H2O⇌NH3∙H2O+H+ +H2O⇌NH3∙H2O+H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于氰酸铵(NH4CNO)与尿素(CO(NH2)2)的说法正确的是
| A.互为同分异构体 | B.互为同素异形体 | C.都是共价化合物 | D.都是离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝对值等于电子层数;Q元素原子的最外层电子数是次外层电子数的3倍,则下列叙述中肯定不正确的是。
| A.原子半径:R>Q |
| B.R和Q可形成离子化合物R2Q5 |
| C.R和Q可形成共价化合物RQ |
| D.R和Q可形成共价化合物RO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某元素的最高价氧化物的分子式RO2,其中含R 27.27% 。对此元素的叙述不正确的是( )
| A.该元素为碳 |
| B.该元素的气态氢化物含H 25% |
| C.RO2为极性分子 |
| D.RO2与水反应能生成酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.NaOH固体熔化的过程中,离子键和共价键均被破坏 |
| B.NaHSO4在水溶液中或熔融状态下,都能电离出H+ |
| C.CO2和PCl3分子中,每个原子最外层都具有8电子稳定结构 |
| D.HBr比HCl的热稳定性差,说明HBr的分子间作用力比HCl弱 |
您最近一年使用:0次
【推荐1】设 表示阿伏加德罗常数的值,下列说法中不正确的
表示阿伏加德罗常数的值,下列说法中不正确的
 表示阿伏加德罗常数的值,下列说法中不正确的
表示阿伏加德罗常数的值,下列说法中不正确的A.含16g氧原子的二氧化硅晶体中含有的 键数目为 键数目为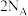 |
B.1mol冰中氢键的个数为 |
C.向 中加入足量 中加入足量 溶液,可以得到 溶液,可以得到 沉淀 沉淀 |
D.12g石墨烯(单层石墨)中含有的六元环数为 个 个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关晶体及配合物结构和性质的判断错误的是
| 选项 | 结构和性质 | 相应判断 |
| A | 贵金属磷化物Rh2P 可用作电解水的高效催化剂,其立方晶胞如图所示 | 该晶体中磷原子的配位数为 8 |
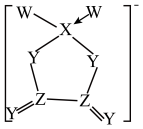
| B | 配离子[Co(NO2)6]3−可用于检验K+的存在 | 该离子中Co3+配位数为 6 |
| C | GaN、GaP、GaAs 都是良好的半导体材料,晶体类型与晶体碳化硅类似 | GaN、GaP、GaAs 的熔点依次升高 |
| D | 氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一 | 分子中存在配位键,提供孤电子对的原子是氮原子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 H2CO3
H2CO3
 )纳米复合物是一种新型光催化剂,可用于光分解水的反应,其原理如图所示。下列说法错误的是
)纳米复合物是一种新型光催化剂,可用于光分解水的反应,其原理如图所示。下列说法错误的是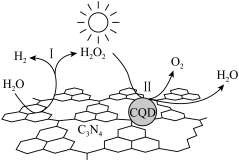
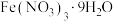 溶于水后再依次加
溶于水后再依次加 溶液和
溶液和 溶液,发现溶液出现下列变化:
溶液,发现溶液出现下列变化: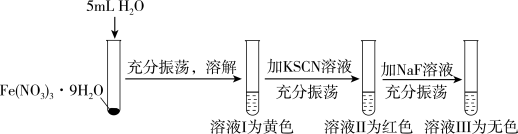
 为浅紫色、
为浅紫色、 为红色、
为红色、 为无色。
为无色。 含12mol
含12mol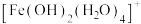 而显黄色
而显黄色 、
、 ,现象不变
,现象不变

