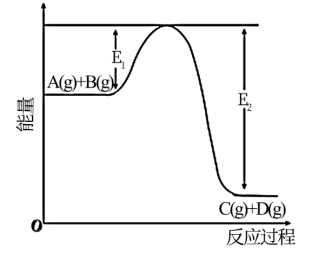
在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
变化示意图如图:
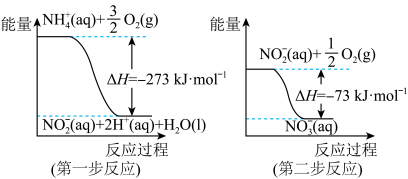
(1)第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
(2)1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3)HCl与氧气在催化剂加热条件下可生成氯气和气态水:4HCl+O2 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:
该反应的热化学方程式是_______ 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:变化示意图如图:

(1)第一步反应是
(2)1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3)HCl与氧气在催化剂加热条件下可生成氯气和气态水:4HCl+O2
 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:| 化学键 | H-Cl | O=O | Cl-Cl | H-O |
| 键能/kJmol | 431 | 498 | 243 | 463 |
该反应的热化学方程式是
更新时间:2023-05-16 11:38:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.(1)某种铵根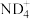 中的中子数是
中的中子数是_____ ,核外电子数是_____ 。
(2)下列装置能够组成原电池的是____ 。
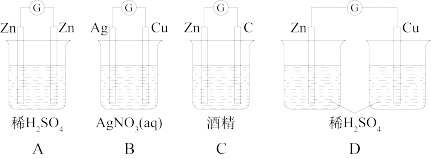
(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要____ (填“放出”或“吸收”)____ kJ的热量。
(4)用电子式表示CS2的形成过程:____ 。
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是____ ;(填序号,下同);
②既存在非极性共价键又存在极性共价键的是_______ 。
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是____ ;仅共价键被破坏的是____ 。
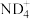 中的中子数是
中的中子数是(2)下列装置能够组成原电池的是

(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要
(4)用电子式表示CS2的形成过程:
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是
②既存在非极性共价键又存在极性共价键的是
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)有①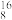 O、
O、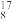 O、
O、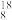 O;②H2、D2、T2,③金刚石、石墨烯、碳纳米管;④
O;②H2、D2、T2,③金刚石、石墨烯、碳纳米管;④ H、
H、 H、
H、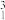 H四组微粒或物质,互为同位素的是
H四组微粒或物质,互为同位素的是_____ (填编号)。
(2)化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
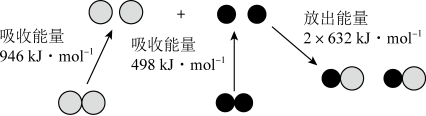
该反应为______ (填“吸热”或“放热”)反应。
(3)已知:反应aA(g)+bB(g) cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
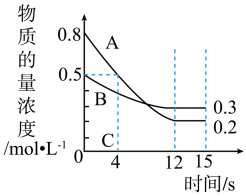
①经测定,前4s内v(C)=0.05mol·L-1·s-1,v(A)=______ 。
②下列叙述能说明该反应达到化学平衡状态的是______ 。
A.混合气体的总物质的量不随时间变化而变化
B.单位时间内每消耗3molA,同时生成2molC
C.v(A):v(B)=3:1
D.混合气体的密度不随时间变化而变化
E.混合气体的平均摩尔质量不随时间变化而变化
(1)有①
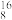 O、
O、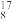 O、
O、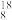 O;②H2、D2、T2,③金刚石、石墨烯、碳纳米管;④
O;②H2、D2、T2,③金刚石、石墨烯、碳纳米管;④ H、
H、 H、
H、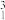 H四组微粒或物质,互为同位素的是
H四组微粒或物质,互为同位素的是(2)化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

该反应为
(3)已知:反应aA(g)+bB(g)
 cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。
①经测定,前4s内v(C)=0.05mol·L-1·s-1,v(A)=
②下列叙述能说明该反应达到化学平衡状态的是
A.混合气体的总物质的量不随时间变化而变化
B.单位时间内每消耗3molA,同时生成2molC
C.v(A):v(B)=3:1
D.混合气体的密度不随时间变化而变化
E.混合气体的平均摩尔质量不随时间变化而变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)今有如下两个热化学方程式:则a_____ b (填“>”、“=”或“<”)
H2(g)+ O2(g)═H2O (g)△H1=a kJ•mol﹣1
O2(g)═H2O (g)△H1=a kJ•mol﹣1
H2(g)+ O2(g)═H2O (1)△H2=b kJ•mol﹣1
O2(g)═H2O (1)△H2=b kJ•mol﹣1
(2)拆开lmol气态物质中某种共价键需要吸收的能量叫键能,部分化学键键能如表。
已知反应N2(g)+3H2(g)=2NH3(g)△H=a kJ•mol﹣1,试根据表中所列键能数据计算a=_____ 。
(3)利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g);△H=﹣90.8kJ•mol ﹣1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=﹣23.5kJ•mol ﹣1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=﹣41.3kJ•mol ﹣1
写出水煤气合成二甲醚并生成CO2的热化学反应方程式_____ 。
(1)今有如下两个热化学方程式:则a
H2(g)+
 O2(g)═H2O (g)△H1=a kJ•mol﹣1
O2(g)═H2O (g)△H1=a kJ•mol﹣1H2(g)+
 O2(g)═H2O (1)△H2=b kJ•mol﹣1
O2(g)═H2O (1)△H2=b kJ•mol﹣1(2)拆开lmol气态物质中某种共价键需要吸收的能量叫键能,部分化学键键能如表。
| 化学键 | H﹣H | N﹣H | N≡N |
| 键能/kJ•mol﹣1 | 436 | 391 | 945 |
已知反应N2(g)+3H2(g)=2NH3(g)△H=a kJ•mol﹣1,试根据表中所列键能数据计算a=
(3)利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g);△H=﹣90.8kJ•mol ﹣1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=﹣23.5kJ•mol ﹣1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=﹣41.3kJ•mol ﹣1
写出水煤气合成二甲醚并生成CO2的热化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65 kJ的热量。
①写出反应的热化学方程式:________________________________ ,其中氧化剂是____________ ,若反应中当有1molN2生成时转移的电子物质的量是__________ 。
②此反应用于火箭推进,除释放大量热和产生气体外,还有一个很大的优点是___________ 。
(2)已知:2CO(g) + O2(g) = 2CO2(g) △H= -566 kJ/mol
Na2O2(s) + CO2(g) = Na2CO3(s) + O2(g) △H= -226 kJ/mol
O2(g) △H= -226 kJ/mol
请写出常温下,过氧化钠与一氧化碳反应生成碳酸钠的热化学方程式:____________________ 。
(3)中学化学实验中的中和热的测定所需的玻璃仪器除了大烧杯、小烧杯、量筒外还有:_____ ,在大小烧杯之间填满碎泡沫(或纸条)其作用是_____ 。
①写出反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和产生气体外,还有一个很大的优点是
(2)已知:2CO(g) + O2(g) = 2CO2(g) △H= -566 kJ/mol
Na2O2(s) + CO2(g) = Na2CO3(s) +
 O2(g) △H= -226 kJ/mol
O2(g) △H= -226 kJ/mol请写出常温下,过氧化钠与一氧化碳反应生成碳酸钠的热化学方程式:
(3)中学化学实验中的中和热的测定所需的玻璃仪器除了大烧杯、小烧杯、量筒外还有:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】将二氧化碳转化为高附加值化学品是目前研究的热点之一,甲醇是重要的化工原料和优良的替代燃料,因此加氢制甲醇被广泛关注。在催化剂作用下主要发生以下反应。
Ⅰ、CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1
CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1
Ⅱ、CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ·mol−1
CO(g)+H2O(g) ΔH2=+41kJ·mol−1
Ⅲ、CO(g)+2H2(g) CH3OH(g) ΔH3
CH3OH(g) ΔH3
反应Ⅲ自发进行的条件是_____ 。
Ⅰ、CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1
CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1Ⅱ、CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ·mol−1
CO(g)+H2O(g) ΔH2=+41kJ·mol−1Ⅲ、CO(g)+2H2(g)
 CH3OH(g) ΔH3
CH3OH(g) ΔH3反应Ⅲ自发进行的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g)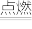 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:
则生成1molH2O(g)可以放出____ kJ热量。
(2)下列反应中,属于放热反应的是____ (填字母,下同),属于吸热反应的是____ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向____ (填“A”或“B”)极。
②装置乙中正极的电极反应式为____ 。
③四种金属活动性由强到弱的顺序是____ 。
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g)
 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 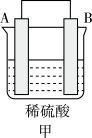 |  | 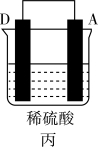 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生 ,做出
,做出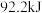 热量。
热量。
①该可逆反应,若起始时向容器内放入 和
和 ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)___________ 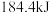 。
。
②在图中画出合成氨反应过程中焓(H)的变化示意图___________ 。
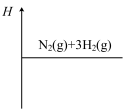
③已知:
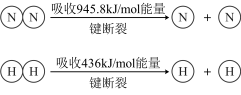
 键断裂吸收的能量约等于
键断裂吸收的能量约等于___________ kJ。
(2)二甲醚 是重要的化工原料,可用
是重要的化工原料,可用 和
和 制得,总反应的热化学方程式如下:
制得,总反应的热化学方程式如下:
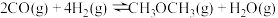
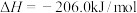
此反应工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行来完成:
i甲醇合成反应:___________ (请补全)
ii甲醇脱水反应: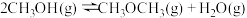 ,
,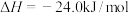
生产二甲醚的过程中存在以下副反应,与甲醇脱水反应形成竞争: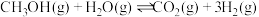 ;
;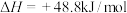
将反应物混合气按进料比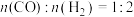 通入反应装置,选择合适的催化剂。
通入反应装置,选择合适的催化剂。
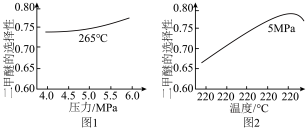
在不同温度和压强下,测得二甲醚的选择性分别如图1、图2所示。
资料:二甲醚的选择性是指转化为二甲醚的 在全部
在全部 反应物中所占的比例。
反应物中所占的比例。
①图1中,温度一定,压强增大,二甲醚选择性增大的原因是___________ 。
②图2中,温度高于265℃后,二甲醚选择性降低的原因有___________ 。
(1)合成氨工业中,合成塔中每产生
 ,做出
,做出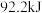 热量。
热量。①该可逆反应,若起始时向容器内放入
 和
和 ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)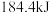 。
。②在图中画出合成氨反应过程中焓(H)的变化示意图

③已知:

 键断裂吸收的能量约等于
键断裂吸收的能量约等于(2)二甲醚
 是重要的化工原料,可用
是重要的化工原料,可用 和
和 制得,总反应的热化学方程式如下:
制得,总反应的热化学方程式如下: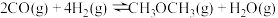
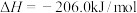
此反应工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行来完成:
i甲醇合成反应:
ii甲醇脱水反应:
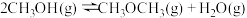 ,
,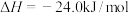
生产二甲醚的过程中存在以下副反应,与甲醇脱水反应形成竞争:
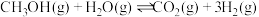 ;
;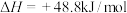
将反应物混合气按进料比
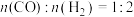 通入反应装置,选择合适的催化剂。
通入反应装置,选择合适的催化剂。在不同温度和压强下,测得二甲醚的选择性分别如图1、图2所示。

资料:二甲醚的选择性是指转化为二甲醚的
 在全部
在全部 反应物中所占的比例。
反应物中所占的比例。①图1中,温度一定,压强增大,二甲醚选择性增大的原因是
②图2中,温度高于265℃后,二甲醚选择性降低的原因有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。
(1)已知:





则反应

______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)化学反应的能量变化( )与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)1 mol化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
)与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)1 mol化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
反应
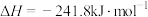 ,则
,则
______ 。
(3)甲醇(g)和水蒸气反应生成氢气的能量变化如图1所示:
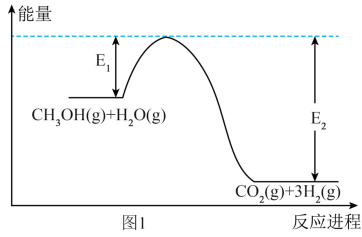
①该反应是______ (填“放热反应”或“吸热反应”);该反应过程中若加入催化剂,催化剂将______ (填“增大”、“减少”或“不影响”)反应热。
②该反应的
______ (用含 、
、 的代数式表示)。
的代数式表示)。
③已知常温下1 g甲醇完全燃烧生成气态CO2和液态水时放热22.68 kJ,请写出甲醇燃烧的热化学方程式:____________________ 。
(4)取 的NaOH溶液50 mL与
的NaOH溶液50 mL与 的稀盐酸50 mL置于如图2所示的简易装置中进行反应,并测定中和反应的反应热。
的稀盐酸50 mL置于如图2所示的简易装置中进行反应,并测定中和反应的反应热。
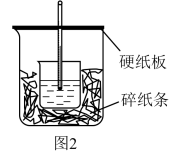
图2所示装置中缺少的仪器名称为______ ,除此外______ (填“仍存在”或“不存在”)错误;当将装置完善后,测得的中和反应的反应热 ,则产生此结果的原因可能是
,则产生此结果的原因可能是______ (填标号)。
a.用温度计测量NaOH溶液起始温度后直接测量盐酸的温度
b.用量筒量取稀盐酸体积时仰视读数
c.分多次把NaOH溶液缓慢倒入盛有稀盐酸的小烧杯中
(1)已知:






则反应


 、
、 、
、 的代数式表示)。
的代数式表示)。(2)化学反应的能量变化(
 )与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)1 mol化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
)与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)1 mol化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:化学键 | H—H | O=O | O—H |
| 436 | x | 463 |

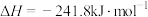 ,则
,则
(3)甲醇(g)和水蒸气反应生成氢气的能量变化如图1所示:

①该反应是
②该反应的

 、
、 的代数式表示)。
的代数式表示)。③已知常温下1 g甲醇完全燃烧生成气态CO2和液态水时放热22.68 kJ,请写出甲醇燃烧的热化学方程式:
(4)取
 的NaOH溶液50 mL与
的NaOH溶液50 mL与 的稀盐酸50 mL置于如图2所示的简易装置中进行反应,并测定中和反应的反应热。
的稀盐酸50 mL置于如图2所示的简易装置中进行反应,并测定中和反应的反应热。
图2所示装置中缺少的仪器名称为
 ,则产生此结果的原因可能是
,则产生此结果的原因可能是a.用温度计测量NaOH溶液起始温度后直接测量盐酸的温度
b.用量筒量取稀盐酸体积时仰视读数
c.分多次把NaOH溶液缓慢倒入盛有稀盐酸的小烧杯中
您最近一年使用:0次