肼( )可作火箭发射的燃料。某实验兴趣小组利用氨与次氯酸钠反应制备
)可作火箭发射的燃料。某实验兴趣小组利用氨与次氯酸钠反应制备 ,并探究
,并探究 的性质,其制备装置如图所示。
的性质,其制备装置如图所示。
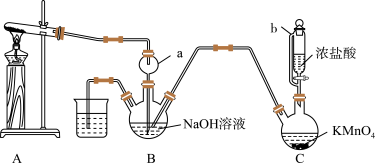
回答下列问题:
(1)仪器b的名称为___________ ,仪器a的作用是___________ 。
(2)装置A试管中发生反应的化学方程式为___________ 。
(3)上述装置B、C间缺少一个装置,可能导致的结果是___________ 。
(4)探究 的性质。将制得的
的性质。将制得的 分离提纯后,进行如下实验。
分离提纯后,进行如下实验。
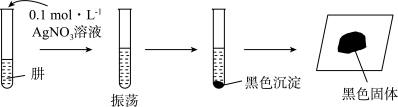
[查阅资料]AgOH不稳定,易分解生成黑色的 ,
, 可溶于氨水。
可溶于氨水。
[提出假设]黑色固体可能是Ag、 中的一种或两种。
中的一种或两种。
[实验验证]设计如下方案,进行实验。
(5)实验制得的肼往往以 的形式存在于溶液中,其原因是
的形式存在于溶液中,其原因是___________ 。
(6)肼又称联氨,是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg联氨可除去水中溶解的 的质量为
的质量为___________ kg。
 )可作火箭发射的燃料。某实验兴趣小组利用氨与次氯酸钠反应制备
)可作火箭发射的燃料。某实验兴趣小组利用氨与次氯酸钠反应制备 ,并探究
,并探究 的性质,其制备装置如图所示。
的性质,其制备装置如图所示。
回答下列问题:
(1)仪器b的名称为
(2)装置A试管中发生反应的化学方程式为
(3)上述装置B、C间缺少一个装置,可能导致的结果是
(4)探究
 的性质。将制得的
的性质。将制得的 分离提纯后,进行如下实验。
分离提纯后,进行如下实验。
[查阅资料]AgOH不稳定,易分解生成黑色的
 ,
, 可溶于氨水。
可溶于氨水。[提出假设]黑色固体可能是Ag、
 中的一种或两种。
中的一种或两种。[实验验证]设计如下方案,进行实验。
| 操作 | 现象 | 结论 |
| ⅰ.取少量黑色固体于试管中,加入足量① | 黑色固体部分溶解 | 黑色固体中有 |
| ⅱ.取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ② | 黑色固体是Ag和 ,则肼具有的性质是碱性和③ ,则肼具有的性质是碱性和③ |
 的形式存在于溶液中,其原因是
的形式存在于溶液中,其原因是(6)肼又称联氨,是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg联氨可除去水中溶解的
 的质量为
的质量为
2023·全国·模拟预测 查看更多[8]
(已下线)全国卷(老教材)理综化学预测卷湖北省名校2023届高三下学期5月适应性考试化学试题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)福建省泉州第五中学2023届高三一模化学试题(已下线)第8讲 物质的量与气体摩尔体积化学02(15+4模式)2024年1月“九省联考”考前化学猜想卷湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学湖南省邵阳市第二中学2023-2024学年高三下学期2月月考化学试题
更新时间:2023-05-08 11:19:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】电子工业中常用FeCl3溶液做“腐蚀液”,腐蚀覆铜板制作印刷电路板。为使“腐蚀液”能得到循环利用并回收铜的流程图如下:
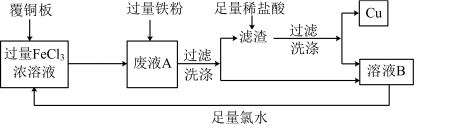
(1)写出FeCl3溶液与铜反应的离子方程式___________ 。
(2)滤渣的成分为___________ (填化学式)。
(3)加足量氯水后反应的离子方程式为___________ 。
(4)将少量溶液B滴入氢氧化钠溶液中,产生的现象是___________ 。
(5)能在酸性环境下将Fe2+氧化为Fe3+的氧化剂有KMnO4、KClO3、H2O2、Cl2等。已知下列四种氧化剂氧化Fe2+后对应的还原产物如下:
①判断等物质的量的四种氧化剂分别与足量的酸性FeSO4溶液反应,得到Fe3+最多的是___________ (填化学式)。
②写出KClO3溶液与酸性FeSO4溶液反应的离子方程式___________ 。
(6)取废液A加入12.6 g铁粉,充分反应后过滤、洗涤、干燥得滤渣 11.0 g,滤渣与足量盐酸反应后过滤、洗涤、干燥得到9.6 g Cu。合并两次的滤液和洗涤液得溶液B 500 mL,则溶液B中含FeCl2的物质的量浓度为___________ mol/L。

(1)写出FeCl3溶液与铜反应的离子方程式
(2)滤渣的成分为
(3)加足量氯水后反应的离子方程式为
(4)将少量溶液B滴入氢氧化钠溶液中,产生的现象是
(5)能在酸性环境下将Fe2+氧化为Fe3+的氧化剂有KMnO4、KClO3、H2O2、Cl2等。已知下列四种氧化剂氧化Fe2+后对应的还原产物如下:
| 氧化剂 | KMnO4 | KClO3 | H2O2 | Cl2 |
| 还原产物 | Mn2+ | Cl- | H2O | Cl- |
②写出KClO3溶液与酸性FeSO4溶液反应的离子方程式
(6)取废液A加入12.6 g铁粉,充分反应后过滤、洗涤、干燥得滤渣 11.0 g,滤渣与足量盐酸反应后过滤、洗涤、干燥得到9.6 g Cu。合并两次的滤液和洗涤液得溶液B 500 mL,则溶液B中含FeCl2的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】(1)按要求写出方程式:
①HNO3 (电离方程式)_____
②Fe2(SO4)3 (电离方程式)_____
③硫酸钠和氯化钡溶液反应(离子方程式)____
④二氧化碳通入足量氢氧化钠溶液(离子方程式)____________
(2)①0.4molCH4分子中所含原子数与__ g HCl分子中所含原子数相等,该HCl气体在标准状况下的体积为________ L;
②等物质的量O2和臭氧(O3),其质量之比为_______ ;若O2和O3质量相等,则其原子数之比为__ 。
(3)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水,其中属于电解质的有_____ ,属于非电解质的有____ (填编号)。
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取: 2Fe (OH) 3 + 4NaOH + 3NaClO = 2Na2FeO4 + 3NaCl + 5H2O
①该反应中氧化剂是_________ (用化学式表示,后同),______ 元素被氧化,还原物为__________ ;
②用单线桥在方程式中标出电子转移的情况:_______________
③当反应中有lmolNaFeO4生成,转移的电子有_________ mol;
④实验室欲配制250mL0.1 mol•L-1NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为__________ ,下列操作配制的溶液浓度偏低的是__________ 。
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线
①HNO3 (电离方程式)
②Fe2(SO4)3 (电离方程式)
③硫酸钠和氯化钡溶液反应(离子方程式)
④二氧化碳通入足量氢氧化钠溶液(离子方程式)
(2)①0.4molCH4分子中所含原子数与
②等物质的量O2和臭氧(O3),其质量之比为
(3)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水,其中属于电解质的有
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取: 2Fe (OH) 3 + 4NaOH + 3NaClO = 2Na2FeO4 + 3NaCl + 5H2O
①该反应中氧化剂是
②用单线桥在方程式中标出电子转移的情况:
③当反应中有lmolNaFeO4生成,转移的电子有
④实验室欲配制250mL0.1 mol•L-1NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】醋酸亚铬水合物{[Cr(CH3COO)2]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒。已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
Zn(s)+2HCl(aq)===ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)===2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)===[Cr(CH3COO)2]2·2H2O(s)
请回答下列问题:
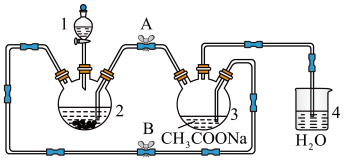
(1)仪器1的名称是________ 。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是________ (选下面字母);目的是__________________________________________________________________ 。
A、盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭止水夹________ (填“A”或“B”,下同),打开止水夹________ 。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是____________________________ 。(用离子方程式表示)
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51 g,取用的醋酸钠溶液为1.5 L 0.1 mol·L-1;实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.48 g,则该实验所得产品的产率为________ (不考虑溶解的醋酸亚铬水合物)。
Zn(s)+2HCl(aq)===ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)===2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)===[Cr(CH3COO)2]2·2H2O(s)
请回答下列问题:

(1)仪器1的名称是
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是
A、盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭止水夹
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51 g,取用的醋酸钠溶液为1.5 L 0.1 mol·L-1;实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.48 g,则该实验所得产品的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组设计用如图所示实验装置(夹持仪器省略),制取干燥的NH3并验证NH3的性质。
(1)实验室用装置甲制备NH3的化学方程式为___________ 。
(2)装置乙的作用是___________ ,若装置丙用于收集NH3,应将导管___________ (填“a”或“b”)延长至集气瓶底部。
(3)装置戊所用仪器的名称为___________ 。
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有___________ 性,写出NH3和Fe2O3反应的化学方程式___________ 。
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是___________ (填标号)。
a.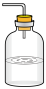 b.
b. c.
c.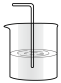 d.
d.

(1)实验室用装置甲制备NH3的化学方程式为
(2)装置乙的作用是
(3)装置戊所用仪器的名称为
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是
a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氮化锶可做荧光粉的原料,可通过金属锶与干燥纯净的氮气在460℃时反应制得。锶与镁、钙同主族,能与水、NH3反应。实验室设计以下装置来制备氮化锶(夹持装置略去)。
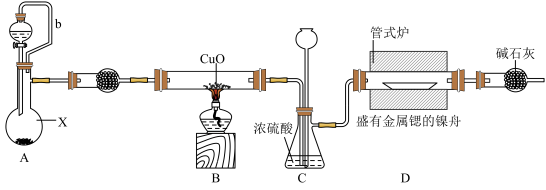
(1)实验简单步骤如下:①连接装置,检验装置的气密性②加装实验药品③点燃B处的酒精灯④加热D处的管式炉⑤打开A处的分液漏斗活塞。正确的实验操作步骤是________ 。
(2)仪器X的名称是__________ ;装置A是制取氨气的简易装置,仪器X中的固体是______________ 。
(3)装置B中的化学方程式是____________________ 。
(4)装置C的作用是平衡装置中的压强和____________________ 。
(5)装置D中的固体物质中含有氮化锶,已知氮化锶极易与水反应生成微溶于水的氢氧化锶,写出反应的化学方程式_________________________ 。
(6)锶的金属性比钠强,但锶与水反应的剧烈程度不如钠,原因足锶的熔点比钠高和____________________________ 。

(1)实验简单步骤如下:①连接装置,检验装置的气密性②加装实验药品③点燃B处的酒精灯④加热D处的管式炉⑤打开A处的分液漏斗活塞。正确的实验操作步骤是
(2)仪器X的名称是
(3)装置B中的化学方程式是
(4)装置C的作用是平衡装置中的压强和
(5)装置D中的固体物质中含有氮化锶,已知氮化锶极易与水反应生成微溶于水的氢氧化锶,写出反应的化学方程式
(6)锶的金属性比钠强,但锶与水反应的剧烈程度不如钠,原因足锶的熔点比钠高和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】已知氨气具有还原性,可以与灼热的氧化铜反应生成两种单质和水,用下图中的装置可以实现该反应。
(1)A中加入的物质是两种固体,A中反应的化学方程式为______ 。
(2)仪器B中加入的物质是_______ (单选,填标号)。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是_______ ,发生反应的化学方程式为________ 。
(4)D中收集到的物质是_______ (选填“液氨”或“氨水”);将酚酞溶液滴到该物质中,出现的现象是_______ ,用电离方程式解释出现该现象的原因________ 。
(5)金属镁在E中收集到的气体中燃烧的化学方程式为_______ 。
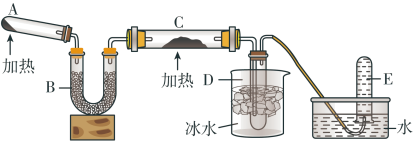
(1)A中加入的物质是两种固体,A中反应的化学方程式为
(2)仪器B中加入的物质是
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是
(4)D中收集到的物质是
(5)金属镁在E中收集到的气体中燃烧的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、[Fe(OCN)6]4-等。
(1)Fe2+基态核外电子排布式为______________ 。
(2)尿素与氯化铁形成{Fe[CO(NH2)2]6}Cl3配合物是一种高效有机催化剂。C、N、O三种元素的电负性由大到小的顺序为___________ ,该配合物中π键和σ键的个数比为______________ 。
(3)研究表明用TiO2作光催化剂可将CN-、CO、N2O、C2H4等氧化为N2、CO2。下列说法正确的是____________ (选填序号)。
a. N2O呈直线形 b. N的第一电离能比C小 c. CO2和N2均属于非极性分子
d. C2H4沸点比N2H4低得多,主要是因为C2H4 相对分子质量小
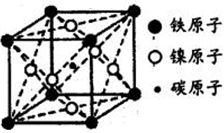
(4)铁可形成多种功能性材料.右图为铁的一种高韧性、高耐磨性合金的晶体结构,其化学式为___________ 。
(5)纳米晶体Mg2FeH6是一种贮氢容量大、价格低廉的储氢材料。M&FeH6可由Mg 和Fe的粉末在H2气氛中反应加热球磨制得,该反应分两步进行.第一步反应为 Mg+H2 MgH2,第二步反应的化学方程式为
MgH2,第二步反应的化学方程式为____________________________ 。
(1)Fe2+基态核外电子排布式为
(2)尿素与氯化铁形成{Fe[CO(NH2)2]6}Cl3配合物是一种高效有机催化剂。C、N、O三种元素的电负性由大到小的顺序为
(3)研究表明用TiO2作光催化剂可将CN-、CO、N2O、C2H4等氧化为N2、CO2。下列说法正确的是
a. N2O呈直线形 b. N的第一电离能比C小 c. CO2和N2均属于非极性分子
d. C2H4沸点比N2H4低得多,主要是因为C2H4 相对分子质量小
(4)铁可形成多种功能性材料.右图为铁的一种高韧性、高耐磨性合金的晶体结构,其化学式为
(5)纳米晶体Mg2FeH6是一种贮氢容量大、价格低廉的储氢材料。M&FeH6可由Mg 和Fe的粉末在H2气氛中反应加热球磨制得,该反应分两步进行.第一步反应为 Mg+H2
 MgH2,第二步反应的化学方程式为
MgH2,第二步反应的化学方程式为
您最近一年使用:0次
【推荐2】四川含有丰富的矿产资源,钒矿、硫铁矿、铜矿等七种矿产储量位居全国前列。回答下列问题:
(1)钒在元素周期表中的位置为_________ ,V3+的价电子排布图为_____________ 。
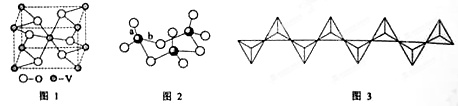
(2)钒的某种氧化物的晶胞结构如图1所示,其晶体的化学式为_____
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中键角______ 120°(填“>”、“<”或“=”); SO3的三聚体环状结构如图2所示,该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为__ (填图2中字母),该分子中含有__ 个σ键。
(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为___ ,例举与VO43-空间构型相同的一种阳离子和一种阴离子___________ (填化学式);也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为___ 。
(5)硫能形成很多种含氧酸,如H2SO3、H2SO4。硫的某种含氧酸分子式为H2S2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式________ (配位键须注明)。
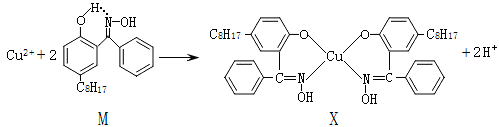
(6)利用铜萃取剂M,通过如下反应实现铜离子的富集:
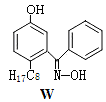
M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是____
(1)钒在元素周期表中的位置为
(2)钒的某种氧化物的晶胞结构如图1所示,其晶体的化学式为
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中键角

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为
(5)硫能形成很多种含氧酸,如H2SO3、H2SO4。硫的某种含氧酸分子式为H2S2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式
(6)利用铜萃取剂M,通过如下反应实现铜离子的富集:


M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】O,O-二甲基-S-(N-甲基氨基甲酰甲基)硫代磷酸酯(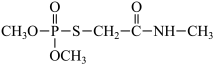 )是一种高效低毒的有机磷杀虫,杀螨剂,其合成路线如图所示:
)是一种高效低毒的有机磷杀虫,杀螨剂,其合成路线如图所示:
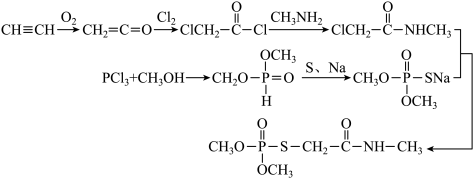
回答下列问题:
(1)CH≡CH分子中C原子与H原子以_____ (填“头碰头”或“肩并肩”)重叠形成C-Hσ键。
(2)熔、沸点比较:CH3NH2_____ (填“>”或“<”)CH3CH3,理由是_____ ;下列事实中,也能用该理由解释的是_____ (填标号)。
A.NH3极易溶于水 B.HF属于弱酸
C.冰的密度比干冰的小 D.H2O比CH4更难分解
(3)乙烯酮(CH2=C=O)生成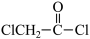 的过程中断裂的是
的过程中断裂的是_____ 键,理由是_____ 。
(4)已知P4(白磷)为正四面体结构,与氧气反应生成P4O10(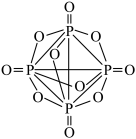 ),P4O10属于
),P4O10属于_____ (填“极性”或“非极性”)分子,该分子中σ键和π键的数目之比为_____ 。
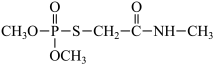 )是一种高效低毒的有机磷杀虫,杀螨剂,其合成路线如图所示:
)是一种高效低毒的有机磷杀虫,杀螨剂,其合成路线如图所示:
回答下列问题:
(1)CH≡CH分子中C原子与H原子以
(2)熔、沸点比较:CH3NH2
A.NH3极易溶于水 B.HF属于弱酸
C.冰的密度比干冰的小 D.H2O比CH4更难分解
(3)乙烯酮(CH2=C=O)生成
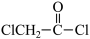 的过程中断裂的是
的过程中断裂的是(4)已知P4(白磷)为正四面体结构,与氧气反应生成P4O10(
 ),P4O10属于
),P4O10属于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
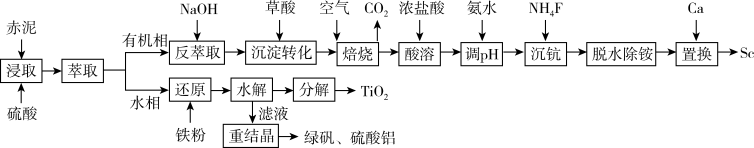
【推荐1】从铝土矿废料“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中提钪与TiO2的一种工艺如下:
已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
(1)钪为21号元素,该元素在元素周期表中的位置是_______ 。
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是_______ 。
(3)“焙烧”过程中,生成Sc2O3的化学方程式为_______ 。
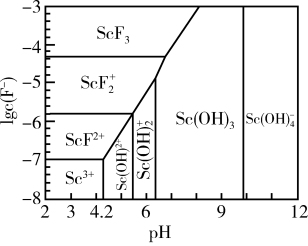
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。已知c(F-)=1×10-5,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为_______ (填化学式)。
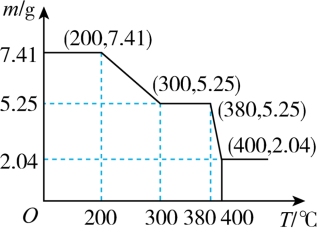
(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=_______ (填数字)。
(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为_______ ;应控制溶液的pH值为_______ 。

已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | TiO2+ |
| 开始沉淀pH | 7.0 | 1.9 | 3.0 | 0.3 |
| 完全沉淀pH | 9.0 | 3.2 | 4.7 | 2.0 |
(1)钪为21号元素,该元素在元素周期表中的位置是
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是
(3)“焙烧”过程中,生成Sc2O3的化学方程式为
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。已知c(F-)=1×10-5,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为

(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=

(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:
a. NH4HCO3 b. NH4Cl c. Ca(OH)2 d. NaOH
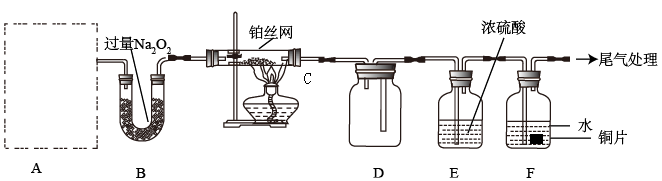
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是______ (填代表备选试剂的字母);此时A中主要的玻璃仪器有______ (填名称)。
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:______ 。
(3)对于C中发生的可逆反应,下列说法正确的______ 。
a. 增大一种反应物的浓度可以提高另一种反应物的转化率
b. 工业上进行该反应时,可采取高压的条件提高反应物转化率
c. 该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
d. 使用铂丝网可以使正反应速率增大,同时也增大逆反应速率
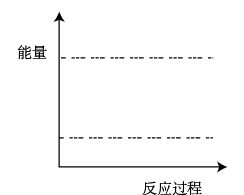
(4)请在如图坐标中画出C装置中反应发生过程中的能量变化示意图(具体能量数值不用标出),并在虚线上分别标出反应物和生成物的化学式______ 。
(5)待实验结束后,将B中固体混合物溶于500 mL 1 mol·L-1的盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是______ mol,甲在标准状况下体积为______ L(忽略气体溶解)。
a. NH4HCO3 b. NH4Cl c. Ca(OH)2 d. NaOH

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的
a. 增大一种反应物的浓度可以提高另一种反应物的转化率
b. 工业上进行该反应时,可采取高压的条件提高反应物转化率
c. 该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
d. 使用铂丝网可以使正反应速率增大,同时也增大逆反应速率
(4)请在如图坐标中画出C装置中反应发生过程中的能量变化示意图(具体能量数值不用标出),并在虚线上分别标出反应物和生成物的化学式

(5)待实验结束后,将B中固体混合物溶于500 mL 1 mol·L-1的盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】新型净水剤PAC的化学式为Al(OH)xCly∙zH2O,它的一般生产工艺流程如下:
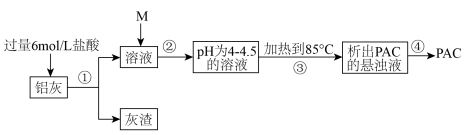
(1)用36.5% (p为1.1 8g/cm3)的盐酸配制500mL6mo/L的盐酸,所用玻璃器有烧杯、量筒(量取一定体积浓盐酸)、玻璃棒、_________________ ,操作②是测定溶液的pH値,控制pH値在一定范围的目的是_______ 。
(2)操作③使用的是_______ 方法,④的具体操作为____________ 。
(3)为测定PAC化学式中的x、y、z的値。
①取样品研碎置于(填仪器名称)________ 中加热灼烧到质量不再减少, 26.5g样品最终变为白色粉末10.2g。实验过程中至少进行的称量次数为_________ 。
②另取相同质量的样品溶于_________ 中,加入足量硝酸银溶液取得沉淀,经洗涤、烘干、称量为28.7g,实验中检查沉淀是否洗净的方法是____________ 。
③列式计算:x+y=3, =
=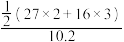
请写出另一条比例式为______________ 。

(1)用36.5% (p为1.1 8g/cm3)的盐酸配制500mL6mo/L的盐酸,所用玻璃器有烧杯、量筒(量取一定体积浓盐酸)、玻璃棒、
(2)操作③使用的是
(3)为测定PAC化学式中的x、y、z的値。
①取样品研碎置于(填仪器名称)
②另取相同质量的样品溶于
③列式计算:x+y=3,
 =
=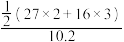
请写出另一条比例式为
您最近一年使用:0次



