下图所示为工业合成氨的流程图。下列有关生产条件的调控作用分析错误的是
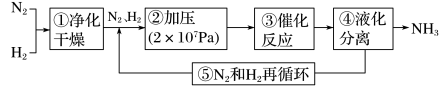

| A.步骤①中“净化”可以防止催化剂中毒 |
| B.步骤②“加压”可以加快反应速率,但压强过高,氨的产率会降低 |
| C.步骤③一般选择控制反应温度为400~500℃,因为在该温度下催化剂的活性最大 |
| D.步骤④⑤有利于提高原料的利用率,能节约生产成本 |
更新时间:2023-04-23 19:38:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在一个压强恒定的密闭容器中,N2 与 H2 反应合成氨的反应达到平衡后,容器中含 1molN2、3molH2、1molNH3,保持温度不变,向该容器中再加 1mol N2、3mol H2、1molNH3,下列说法正确的是
| A.正、逆反应速率同时增大,平衡不移动 |
| B.正、逆反应速率同时增大,NH3 百分含量增大 |
| C.正.逆反应速率不变,平衡不移动 |
| D.正反应速率增大,逆反应速率减小,平衡向逆反应移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列生产或实验事实引出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 向5 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡,完全反应后,滴加 溶液,出现血红色 溶液,出现血红色 | 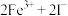  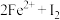 是可逆反应 是可逆反应 |
| B | 向淀粉-KI溶液中滴加氯水溶液变蓝色 | 氯水中含有次氯酸 |
| C | 其他条件相同, 溶液和 溶液和 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| D | 取 固体,溶解后滴加硝酸酸化的硝酸钡溶液,产生白色沉淀 固体,溶解后滴加硝酸酸化的硝酸钡溶液,产生白色沉淀 |  固体已变质 固体已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
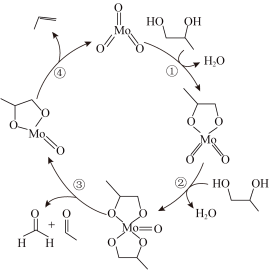
【推荐1】一定条件下双氧水与某浓度的硫酸反应过程如图所示,下列说法正确的是
HO—OH HO—OSO3H(过一硫酸)
HO—OSO3H(过一硫酸) HO3SO—OSO3H(过二硫酸)
HO3SO—OSO3H(过二硫酸)
HO—OH
 HO—OSO3H(过一硫酸)
HO—OSO3H(过一硫酸) HO3SO—OSO3H(过二硫酸)
HO3SO—OSO3H(过二硫酸)| A.生成过硫酸反应过程因硫酸的羟基被取代而呈中性 |
| B.可以用硝酸钡溶液鉴别过一硫酸和过二硫酸 |
| C.过一硫酸与过二硫酸均可做漂白剂,温度越高,漂白性越强 |
| D.等物质的量的过一硫酸与过二硫酸消耗FeSO4的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
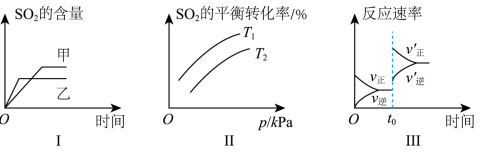
【推荐2】工业生产硫酸的一步重要反应是2SO2(g)+O2(g) 2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
 2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
| A.图Ⅰ表示催化剂对化学平衡的影响,且甲使用了催化剂 |
| B.图Ⅰ表示温度对化学平衡的影响,且甲温度高 |
| C.图Ⅱ表示SO2平衡转化率与温度及压强的关系,可以判断T1<T2 |
| D.图Ⅲ表示t0时刻升高温度或增大压强对反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在一定温度下,将气体X和气体Y各0.16mol充入1.0L恒容密闭容器中,发生反应2X(g)+Y(g) 2Z(g) ∆H<0,一段时间后达到平衡。反应过程中测定的数据如表:
2Z(g) ∆H<0,一段时间后达到平衡。反应过程中测定的数据如表:
下列说法正确的是
 2Z(g) ∆H<0,一段时间后达到平衡。反应过程中测定的数据如表:
2Z(g) ∆H<0,一段时间后达到平衡。反应过程中测定的数据如表:| T/min | 0 | 2 | 4 | 7 | 9 |
| n(Y)mol | 0.16 | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前4分钟的平均反应速率v(X)=1.25×10-2mol·L-1·min-1 |
| B.该温度下该反应的平衡常数的值为90 |
| C.其他条件不变,升高温度,反应达新平衡前v正>v逆 |
| D.其他条件不变,再充入0.16mol Y,平衡时Y的转化率增大 |
您最近一年使用:0次