磁铁矿的主要成分是Fe3O4。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。
(1)Fe2+的核外电子排布式为_______ ,具有_______ 种运动状态不同的电子。
(2)步骤一:取少量磁铁矿石样品,粉碎后加入过量的试剂A溶解,试剂A可选用_______(填字母)。
(3)步骤二:验证:Fe3+。取溶解后的液体少许,加入少量_______ ,若观察到溶液变为血红色,则证明有Fe3+。
(4)步骤三:验证:Fe2+。取溶解后的液体少许,加入少量_______ ,若观察到_______ ,则证明有Fe2+。
(1)Fe2+的核外电子排布式为
(2)步骤一:取少量磁铁矿石样品,粉碎后加入过量的试剂A溶解,试剂A可选用_______(填字母)。
| A.氨水 | B.氢氧化钠溶液 | C.盐酸 | D.硫酸 |
(4)步骤三:验证:Fe2+。取溶解后的液体少许,加入少量
更新时间:2023-04-24 10:06:29
|
相似题推荐
【推荐1】长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验FeSO4溶液的变质程度
①将上述方案补充完整___________ 、___________ 、___________
②若要使部分变质的FeSO4复原,方法是___________ 。(写离子反应方程式)
(2)利用部分变质 的FeSO4溶液制备Fe2O3
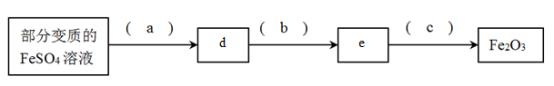
①填写下列各空:a.___________ b.___________ c.___________ d.___________ e.___________
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为___________ 。
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
(1)设计实验检验FeSO4溶液的变质程度
| 实验方案 | 实验现象 | 实验结论 | |
| 步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | ___________ | FeSO4溶液部分变质 |
| 步骤2 | ___________ | ___________ | |
②若要使部分变质的FeSO4复原,方法是
(2)利用
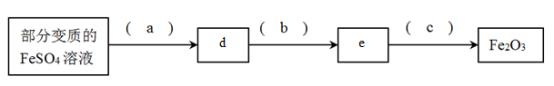
①填写下列各空:a.
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量 Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
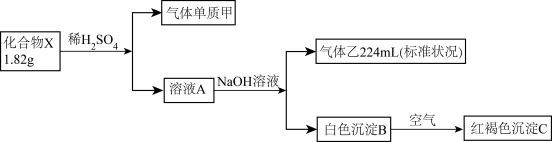
【推荐2】为探究某物质X(仅含两种元素)的组成及和性质,设计并完成如下实验。(气体体积已转化为标准状况下的体积)

请回答下列问题:
(1)X的化学式是___________ 。
(2)无色气体A通入饱和碳酸钠溶液中的离子方程式______________ 。
(3)溶液C中滴加NH4SCN溶液可以检验某种阳离子的存在,请设计实验检验溶液C中另一种金属阳离子的实验方案________________________ 。

请回答下列问题:
(1)X的化学式是
(2)无色气体A通入饱和碳酸钠溶液中的离子方程式
(3)溶液C中滴加NH4SCN溶液可以检验某种阳离子的存在,请设计实验检验溶液C中另一种金属阳离子的实验方案
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某科研小组以铜矿石(含 、
、 和少量
和少量 )为原料,采用微生物堆浸技术制备黄铵铁矾
)为原料,采用微生物堆浸技术制备黄铵铁矾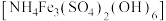 的实验流程如下:
的实验流程如下:
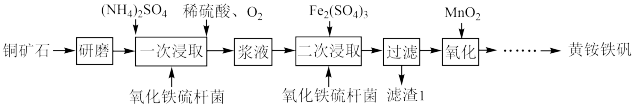
已知:
①氧化铁硫杆菌可将 单质转化为
单质转化为 。
。
② 完全沉淀时
完全沉淀时 为3.7、
为3.7、 、
、 开始沉淀时的
开始沉淀时的 分别为5.4、8.3.。回答下列问题:
分别为5.4、8.3.。回答下列问题:
(1)“研磨”的目的是_____ 。
(2)“一次浸取”时需在低温下进行,温度过高浸出率会下降,写出两种可能的原因:_____ 。
(3)“二次浸取”时加入 和氧化铁硫杆菌的目的是把
和氧化铁硫杆菌的目的是把 全部转化为可溶性的铜盐。检验加入的
全部转化为可溶性的铜盐。检验加入的 中的
中的 是否完全被还原的实验操作是
是否完全被还原的实验操作是_____ ;滤渣1的化学式为_____ 。
(4)“氧化”时发生反应的离子方程式为_____ 。
(5)黄铵铁矾的制备:
①将“氧化”后浆液过滤,边搅拌边向滤液中滴加 溶液,调节溶液
溶液,调节溶液 至
至_____ (填数值范围)。
②过滤、用蒸馏水洗涤滤渣2~3次。向最后一次洗涤液中滴加_____ (填试剂),无沉淀产生。
③向滤渣中加入等体积的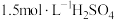 溶液和
溶液和_____  溶液,搅拌使其恰好完全反应。经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得黄铵铁矾。
溶液,搅拌使其恰好完全反应。经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得黄铵铁矾。
 、
、 和少量
和少量 )为原料,采用微生物堆浸技术制备黄铵铁矾
)为原料,采用微生物堆浸技术制备黄铵铁矾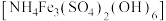 的实验流程如下:
的实验流程如下:
已知:
①氧化铁硫杆菌可将
 单质转化为
单质转化为 。
。②
 完全沉淀时
完全沉淀时 为3.7、
为3.7、 、
、 开始沉淀时的
开始沉淀时的 分别为5.4、8.3.。回答下列问题:
分别为5.4、8.3.。回答下列问题:(1)“研磨”的目的是
(2)“一次浸取”时需在低温下进行,温度过高浸出率会下降,写出两种可能的原因:
(3)“二次浸取”时加入
 和氧化铁硫杆菌的目的是把
和氧化铁硫杆菌的目的是把 全部转化为可溶性的铜盐。检验加入的
全部转化为可溶性的铜盐。检验加入的 中的
中的 是否完全被还原的实验操作是
是否完全被还原的实验操作是(4)“氧化”时发生反应的离子方程式为
(5)黄铵铁矾的制备:
①将“氧化”后浆液过滤,边搅拌边向滤液中滴加
 溶液,调节溶液
溶液,调节溶液 至
至②过滤、用蒸馏水洗涤滤渣2~3次。向最后一次洗涤液中滴加
③向滤渣中加入等体积的
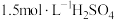 溶液和
溶液和 溶液,搅拌使其恰好完全反应。经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得黄铵铁矾。
溶液,搅拌使其恰好完全反应。经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得黄铵铁矾。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C为中学化学常见的单质,其中只有一种为金属;通常情况下,A为固体,B、C为气体。D、E、F、G、H、X均为化合物,其中X是一种实验室常见的无氧酸且为强酸。E为黑色固体,F含有四种元素,H在常温下为液体,它们之间的转化关系如图所示(其中某些反应的条件已略去)。
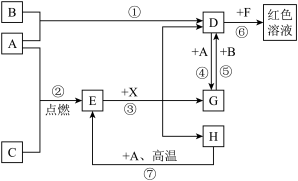
回答下列问题:
(1)B的化学式为____ ,F中的非金属元素的原子半径由大到小的顺序是____ (用元素符号表示)。
(2)在反应①~⑦中,不属于氧化还原反应的是____ (填编号)。
(3)反应⑦的化学方程式为____ ,该反应中每生成2.32g化合物E,转移电子的物质的量为____ mol。
(4)水溶液中,反应⑤的离子方程式为____ 。
(5)D的水溶液与金属铜反应的离子方程式为____ 。

回答下列问题:
(1)B的化学式为
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)反应⑦的化学方程式为
(4)水溶液中,反应⑤的离子方程式为
(5)D的水溶液与金属铜反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:
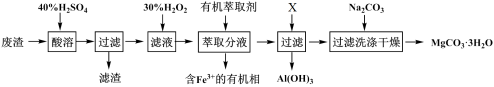
(1)为了加快废渣的酸溶速率,可采取的办法有_________ (任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________ 。
(2)加入30%H2O2的目的是__________________________________ 。
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是__________________________ 。
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是______________________________ 。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________ ,应调节pH的范围为_________________ 。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是____________________________ 。
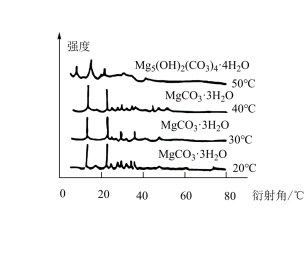
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________ ,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________ 。

(1)为了加快废渣的酸溶速率,可采取的办法有
(2)加入30%H2O2的目的是
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为

您最近一年使用:0次
【推荐1】根据元素在体内含量的不同,可将体内元素分为常量元素和微量元素。其中H、C、O、N、S、P等为常量元素,Fe、Zn等为微量元素。回答下列问题:
(1)基态Fe原子的核外电子排布式为[Ar]_______ ,有_______ 组相同能量的电子。
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是___________ 。
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
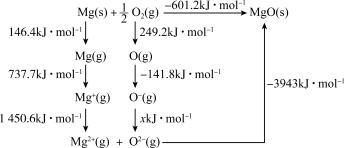
由图可知,Mg原子的第一电离能为___________ kJ·mol-1;O=O键键能为___________ kJ·mol-1;氧原子的第二电子亲和能为___________ kJ·mol-1。
(1)基态Fe原子的核外电子排布式为[Ar]
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
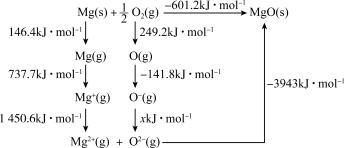
由图可知,Mg原子的第一电离能为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+价层电子排布式_______ 。
(2)元素的第一电离能用I1表示。试分析I1(Li)>I1(Na)的原因是_______ 。I1(Mg)>I1(Al)>I1(Na)的原因是_______ 。
(3)磷酸根离子的空间构型为_______ 其中P杂化轨道类型为_______ 。
(4)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有_______ 个。
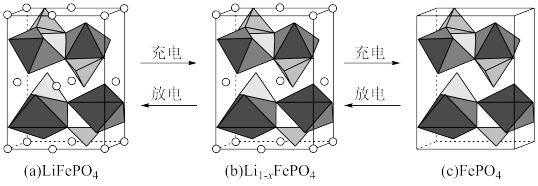
电池充电时,LiFeO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=_______ 。n(Fe2+):n(Fe3+)=_______ 。
(1)基态Fe2+价层电子排布式
(2)元素的第一电离能用I1表示。试分析I1(Li)>I1(Na)的原因是
(3)磷酸根离子的空间构型为
(4)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有

电池充电时,LiFeO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】钙钛矿 型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2) 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示,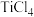 熔点最低,原因是
熔点最低,原因是_______ 。
(3) 的晶胞如图
的晶胞如图 所示,其组成元素的电负性大小顺序是
所示,其组成元素的电负性大小顺序是_______ ;金属离子与氧离子间的作用力为_______ ,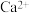 的配位数是
的配位数是_______ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为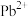 、
、 和有机碱离子
和有机碱离子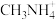 ,其晶胞如图
,其晶胞如图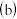 所示。其中
所示。其中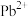 与图
与图 中
中_______ 的空间位置相同,有机碱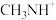 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是_______ ;若晶胞参数为 ,则晶体密度为
,则晶体密度为_______ 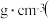 列出计算式
列出计算式 。
。

 型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)
 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示,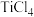 熔点最低,原因是
熔点最低,原因是| 化合物 |  | 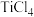 |  |  |
熔点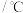 | 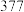 | 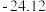 |  | 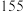 |
 的晶胞如图
的晶胞如图 所示,其组成元素的电负性大小顺序是
所示,其组成元素的电负性大小顺序是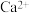 的配位数是
的配位数是(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为
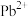 、
、 和有机碱离子
和有机碱离子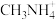 ,其晶胞如图
,其晶胞如图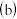 所示。其中
所示。其中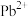 与图
与图 中
中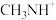 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是 ,则晶体密度为
,则晶体密度为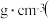 列出计算式
列出计算式 。
。
您最近一年使用:0次