某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:
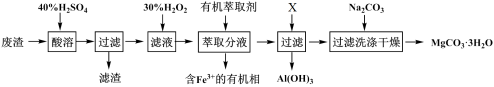
(1)为了加快废渣的酸溶速率,可采取的办法有_________ (任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________ 。
(2)加入30%H2O2的目的是__________________________________ 。
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是__________________________ 。
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是______________________________ 。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________ ,应调节pH的范围为_________________ 。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是____________________________ 。
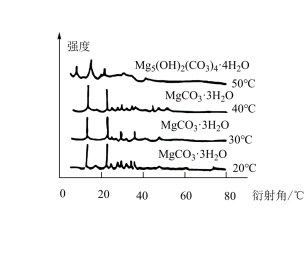
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________ ,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________ 。

(1)为了加快废渣的酸溶速率,可采取的办法有
(2)加入30%H2O2的目的是
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为

更新时间:2018-03-12 20:45:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是_____ ,证明Fe3+存在的现象是__________ 。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:_________________ 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
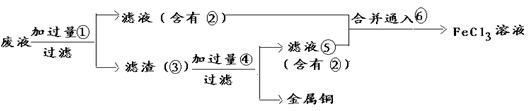
①请写出上述实验中③的化学式:_______
②配制并保存硫酸亚铁溶液时,常在其中加入_______________________
③要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为______ 。
①加入足量氯水 ②加入足量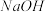 溶液 ③加入少量KSCN溶液
溶液 ③加入少量KSCN溶液
A、①③ B、③② C、③① D、①②③
④写出向②⑤的合并液中通入⑥的离子方程式__________________
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

①请写出上述实验中③的化学式:
②配制并保存硫酸亚铁溶液时,常在其中加入
③要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为
①加入足量氯水 ②加入足量
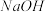 溶液 ③加入少量KSCN溶液
溶液 ③加入少量KSCN溶液A、①③ B、③② C、③① D、①②③
④写出向②⑤的合并液中通入⑥的离子方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸亚铁晶体( )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含________ (填离子符号),检验滤液中还存在 的方法为
的方法为________ (说明试剂、现象)。
(2)步骤②加入过量 的目的是
的目的是________ 。
(3)步骤③中反应的离子方程式________ 。
(4)步骤④中一系列处理的操作步骤包括:过滤、________ 、灼烧、________ 、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为________ g。
 )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含
 的方法为
的方法为(2)步骤②加入过量
 的目的是
的目的是(3)步骤③中反应的离子方程式
(4)步骤④中一系列处理的操作步骤包括:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组拟配制FeI2溶液并探究相关性质。
Ⅰ.配制240mL0.2mol·L-1FeI2溶液
(1)配制FeI2溶液除烧杯、量筒、胶头滴管外,
①还需要的玻璃仪器是_____ 。
②用托盘天平称量,需要称取FeI2_____ g。
③定容时,若仰视容量瓶刻度线会使配制的FeI2溶液浓度_____ 。(填“偏大”或“偏小”)
④久置的FeI2溶液容易变质,检测其是否变质的试剂为_____ 。
Ⅱ.探究Fe2+与I-的还原性强弱
取10mL上述FeI2溶液,向其中滴加少量新制的氯水,振荡后发现溶液呈黄色。
同学们对产生黄色的原因提出假设:
假设1:只有I-被少量Cl2氧化成I2溶解在溶液中,碘水为黄色,还原性:I->Fe2+;
假设2:只有Fe2+被少量Cl2氧化成Fe3+,FeCl3溶液为黄色,还原性:Fe2+>I-。
(2)设计方案,验证假设
①为______ (填“CCl4”或“苯”)。
②上层呈______ 色。
最终实验现象证实:假设1正确。
③若向20mL上述FeI2溶液通入112mL(标准状况)Cl2,反应的离子方程式为______ 。
Ⅰ.配制240mL0.2mol·L-1FeI2溶液
(1)配制FeI2溶液除烧杯、量筒、胶头滴管外,
①还需要的玻璃仪器是
②用托盘天平称量,需要称取FeI2
③定容时,若仰视容量瓶刻度线会使配制的FeI2溶液浓度
④久置的FeI2溶液容易变质,检测其是否变质的试剂为
Ⅱ.探究Fe2+与I-的还原性强弱
取10mL上述FeI2溶液,向其中滴加少量新制的氯水,振荡后发现溶液呈黄色。
同学们对产生黄色的原因提出假设:
假设1:只有I-被少量Cl2氧化成I2溶解在溶液中,碘水为黄色,还原性:I->Fe2+;
假设2:只有Fe2+被少量Cl2氧化成Fe3+,FeCl3溶液为黄色,还原性:Fe2+>I-。
(2)设计方案,验证假设
| 实验方案 | 预期现象 | 结论 |
| 向反应后的溶液中加入适量______,振荡,静置,分层,观察下层液体颜色,在上层溶液中加入KSCN溶液,观察上层颜色 | 下层呈紫红色 | 假设1正确 |
| ______ | 假设2正确 |
②上层呈
最终实验现象证实:假设1正确。
③若向20mL上述FeI2溶液通入112mL(标准状况)Cl2,反应的离子方程式为
您最近半年使用:0次
【推荐1】一维纳米材料因其特殊的纳米结构,呈现出一系列独特的光、电、磁、催化等性能,具有十分广阔的应用前景。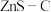 (
( 纳米粒子分散在碳纳米材料上)是新型一维纳米材料,某科研小组用下列流程制备
纳米粒子分散在碳纳米材料上)是新型一维纳米材料,某科研小组用下列流程制备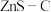 纳米材料。
纳米材料。

已知: 表示
表示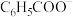
回答下列问题:
(1)“搅拌”后所得溶液显______________ (填“酸性”“中性”或“碱性”)。
(2)配制 溶液时,蒸馏水要煮沸的原因之一是除去溶解氧,另一原因是
溶液时,蒸馏水要煮沸的原因之一是除去溶解氧,另一原因是______________ 。
(3)向混合盐溶液中缓缓滴加 溶液,促进相关离子的水解,出现
溶液,促进相关离子的水解,出现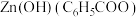 白色沉淀。
白色沉淀。
①写出生成沉淀的离子方程式____________________________ 。
② ,调
,调 ,不产生
,不产生 沉淀,该溶液中
沉淀,该溶液中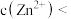
______________  。[已知
。[已知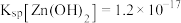 ]
]
(4)“硫化”、“焙烧”过程,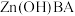 通过原位固相反应制备
通过原位固相反应制备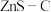 纳米纤维的过程示意图如下:
纳米纤维的过程示意图如下:

①该过程中一直处于原位的离子是______________ ;
②在 氛围中“焙烧”时,
氛围中“焙烧”时,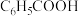 分解的化学方程式为
分解的化学方程式为______________ 。
(5)用 吸附法对不同焙烧温度下制备得到的
吸附法对不同焙烧温度下制备得到的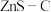 纳米纤维的比表面积(比表面积是指单位质量物料所具有的总面积,单位是
纳米纤维的比表面积(比表面积是指单位质量物料所具有的总面积,单位是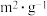 。通常指的是固体材料的比表面积,例如粉末、纤维、颗粒、片状、块状等材料。)进行测定,在不同温度
。通常指的是固体材料的比表面积,例如粉末、纤维、颗粒、片状、块状等材料。)进行测定,在不同温度 下焙烧所得
下焙烧所得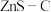 纳米纤维的比表面积如下表:
纳米纤维的比表面积如下表:
①随着温度的升高, 纳米粒子
纳米粒子______________ (填“变大”“不变”或“变小”)。
②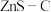 纳米纤维可将
纳米纤维可将 吸附在其表面,形成均匀的单分子层。氮气分子横截面积为
吸附在其表面,形成均匀的单分子层。氮气分子横截面积为 ,则在
,则在 焙烧所得的
焙烧所得的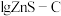 纳米纤维最大吸附的氮分子数为
纳米纤维最大吸附的氮分子数为______________ (保留3位有效数字)。
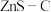 (
( 纳米粒子分散在碳纳米材料上)是新型一维纳米材料,某科研小组用下列流程制备
纳米粒子分散在碳纳米材料上)是新型一维纳米材料,某科研小组用下列流程制备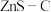 纳米材料。
纳米材料。
已知:
 表示
表示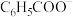
回答下列问题:
(1)“搅拌”后所得溶液显
(2)配制
 溶液时,蒸馏水要煮沸的原因之一是除去溶解氧,另一原因是
溶液时,蒸馏水要煮沸的原因之一是除去溶解氧,另一原因是(3)向混合盐溶液中缓缓滴加
 溶液,促进相关离子的水解,出现
溶液,促进相关离子的水解,出现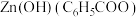 白色沉淀。
白色沉淀。①写出生成沉淀的离子方程式
②
 ,调
,调 ,不产生
,不产生 沉淀,该溶液中
沉淀,该溶液中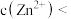
 。[已知
。[已知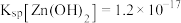 ]
](4)“硫化”、“焙烧”过程,
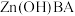 通过原位固相反应制备
通过原位固相反应制备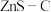 纳米纤维的过程示意图如下:
纳米纤维的过程示意图如下:
①该过程中一直处于原位的离子是
②在
 氛围中“焙烧”时,
氛围中“焙烧”时,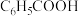 分解的化学方程式为
分解的化学方程式为(5)用
 吸附法对不同焙烧温度下制备得到的
吸附法对不同焙烧温度下制备得到的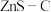 纳米纤维的比表面积(比表面积是指单位质量物料所具有的总面积,单位是
纳米纤维的比表面积(比表面积是指单位质量物料所具有的总面积,单位是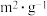 。通常指的是固体材料的比表面积,例如粉末、纤维、颗粒、片状、块状等材料。)进行测定,在不同温度
。通常指的是固体材料的比表面积,例如粉末、纤维、颗粒、片状、块状等材料。)进行测定,在不同温度 下焙烧所得
下焙烧所得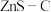 纳米纤维的比表面积如下表:
纳米纤维的比表面积如下表:
| 400 | 500 | 600 | 700 | 800 |
比表面积/ | 130.1 | 123.1 | 70.2 | 49.2 | 47.6 |
 纳米粒子
纳米粒子②
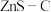 纳米纤维可将
纳米纤维可将 吸附在其表面,形成均匀的单分子层。氮气分子横截面积为
吸附在其表面,形成均匀的单分子层。氮气分子横截面积为 ,则在
,则在 焙烧所得的
焙烧所得的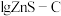 纳米纤维最大吸附的氮分子数为
纳米纤维最大吸附的氮分子数为
您最近半年使用:0次
【推荐2】Ⅰ、我国规定生活用水中镉排放的最大允许浓度为0.005 mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
(1)磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=________ 。
(2)一定温度下,CdCO3的Ksp=4.0 × 10-12,Cd(OH)2的Ksp=3.2 × 10-14,那么它们在水中的溶解量________ 较大。
(3)在某含镉废水中加入Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为_____ mol/L(已知:Ksp(CdS)=7.9 × 10-27,Ar(Cd)=112);此时是否符合水源标准?______ (填“是”或“否”)。
Ⅱ、炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
(4)加入H2O2溶液的作用是________________ 。
(5)流程图中,调节pH时,加入的试剂X可以是________ (填序号)
A、ZnO B、NaOHC、Zn2(OH)2CO3D、ZnSO4
pH应调整到_________ 。
(1)磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=
(2)一定温度下,CdCO3的Ksp=4.0 × 10-12,Cd(OH)2的Ksp=3.2 × 10-14,那么它们在水中的溶解量
(3)在某含镉废水中加入Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为
Ⅱ、炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 | Fe3+ | Zn2+ | Fe2+ |
| 开始沉淀的pH | 1. 1 | 5. 2 | 5. 8 |
| 沉淀完全的pH | 3. 2 | 6. 4 | 8. 8 |
(5)流程图中,调节pH时,加入的试剂X可以是
A、ZnO B、NaOHC、Zn2(OH)2CO3D、ZnSO4
pH应调整到
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】氧化铁可以用于电子工业、通讯整机、电视机、计算机等磁性原料及行输出变压器、开关电源及其高U及高UQ等的铁氧体磁芯,用作分析试剂、催化剂和抛光剂,也用于颜料的配料。下面是制备氧化铁的一种方法(铁屑表面常附着油污),其流程如下:
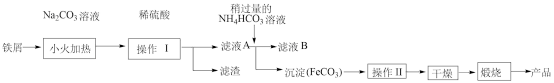
(1)Na2CO3溶液是用来除去铁屑表面附着油污,原因是Na2CO3溶液呈碱性,用离子方程式表示其呈碱性的主要原因___________ ;在Na2CO3溶液中,用各离子浓度表示的电荷守恒关系为___________ 。
(2)实验室进行过滤操作所用到的玻璃仪器有___________ ;操作Ⅱ为洗涤,检验沉淀洗涤干净的方法是___________ 。
(3)滤液A的主要成分的化学式为___________ ;向其中加入稍过量的NH4HCO3溶液,生成沉淀的同时有一种气体(能使澄清石灰水变浑浊)产生,写出其化学方程式___________ 。
(4)若要将滤液A中的Fe2+沉淀完全,此时溶液中 最小是
最小是___________ (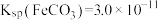 )。
)。
(5)如果煅烧不充分,产品中将有FeO存在,称取3.5 g氧化铁产品,加酸溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中,用酸化的0.01000 mol/L KMnO4溶液滴定至终点,重复滴定2~3次,消耗酸性KMnO4溶液体积的平均值为20.00 mL。
①酸性KMnO4溶液应盛装在___________ (填“酸式”或“碱式”)滴定管。
②上述产品中杂质FeO的质量分数为___________ (保留两位小数)。

(1)Na2CO3溶液是用来除去铁屑表面附着油污,原因是Na2CO3溶液呈碱性,用离子方程式表示其呈碱性的主要原因
(2)实验室进行过滤操作所用到的玻璃仪器有
(3)滤液A的主要成分的化学式为
(4)若要将滤液A中的Fe2+沉淀完全,此时溶液中
 最小是
最小是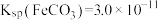 )。
)。(5)如果煅烧不充分,产品中将有FeO存在,称取3.5 g氧化铁产品,加酸溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中,用酸化的0.01000 mol/L KMnO4溶液滴定至终点,重复滴定2~3次,消耗酸性KMnO4溶液体积的平均值为20.00 mL。
①酸性KMnO4溶液应盛装在
②上述产品中杂质FeO的质量分数为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、 、
、 、
、 、
、 等)提取硒,设计流程如下:
等)提取硒,设计流程如下:
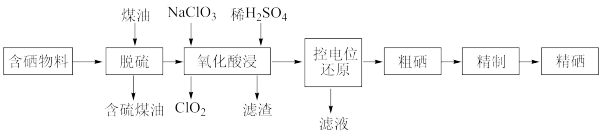
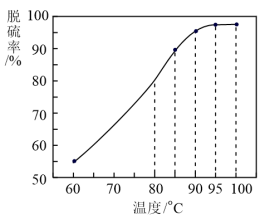
回答下列问题:
(1)“脱硫”时,测得脱硫率随温度的变化如上(如图)。随着温度的升高,脱硫率呈上升趋势,其原因是_____ 。最佳温度是_____ 。
(2)“氧化酸浸”中, 转化成
转化成 ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(3)采用硫[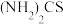 ]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
①控制电位在 范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为
范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为_____ 。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_____ V。
(4)粗硒的精制过程: 浸 出[Se转化成硒代硫酸钠(
浸 出[Se转化成硒代硫酸钠( )]
)] 净化
净化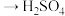 酸化等步骤。
酸化等步骤。
①净化后的溶液中 达到
达到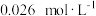 ,此时溶液中的
,此时溶液中的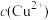 的最大值为
的最大值为_____ 。精硒中基本不含铜[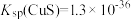 ]
]
②硒代硫酸钠酸化生成硒的化学方程式为_____ 。
 、
、 、
、 、
、 等)提取硒,设计流程如下:
等)提取硒,设计流程如下:

回答下列问题:
(1)“脱硫”时,测得脱硫率随温度的变化如上(如图)。随着温度的升高,脱硫率呈上升趋势,其原因是
(2)“氧化酸浸”中,
 转化成
转化成 ,该反应的离子方程式为
,该反应的离子方程式为(3)采用硫[
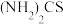 ]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。| 名称 |  / / |  / / |  / / |  / / |  / / |  / / |
电位/ | 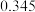 | 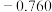 | 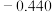 |  | 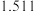 | 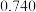 |
 范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为
范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在
(4)粗硒的精制过程:
 浸 出[Se转化成硒代硫酸钠(
浸 出[Se转化成硒代硫酸钠( )]
)] 净化
净化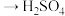 酸化等步骤。
酸化等步骤。①净化后的溶液中
 达到
达到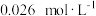 ,此时溶液中的
,此时溶液中的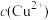 的最大值为
的最大值为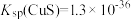 ]
]②硒代硫酸钠酸化生成硒的化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硼泥主要由MgO和 组成,含有
组成,含有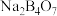 、
、 、
、 、
、 等杂质。用硼泥生产氢氧化镁的工艺流程如图所示:
等杂质。用硼泥生产氢氧化镁的工艺流程如图所示:
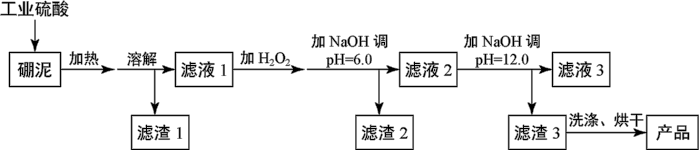
已知某些氢氧化物沉淀的pH如下表所示:
(1)滤渣1除含有 外,还含有
外,还含有___________ 。加入硫酸时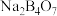 发生反应的离子方程式为:
发生反应的离子方程式为:___________ 。
(2)向滤液1中加入 ,发生反应的离子方程式为:
,发生反应的离子方程式为:___________ 。
(3)滤渣2的主要成分是___________ ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为___________ 。
(4)证明滤渣3已洗涤干净的实验操作___________ 。
(5)若取a吨硼泥为原料,最后得到b吨 产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为___________ (用含有a、b的代数式表示)。
 组成,含有
组成,含有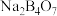 、
、 、
、 、
、 等杂质。用硼泥生产氢氧化镁的工艺流程如图所示:
等杂质。用硼泥生产氢氧化镁的工艺流程如图所示:
已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | 开始沉淀的pH | 完全沉淀的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
 外,还含有
外,还含有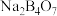 发生反应的离子方程式为:
发生反应的离子方程式为:(2)向滤液1中加入
 ,发生反应的离子方程式为:
,发生反应的离子方程式为:(3)滤渣2的主要成分是
(4)证明滤渣3已洗涤干净的实验操作
(5)若取a吨硼泥为原料,最后得到b吨
 产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下:
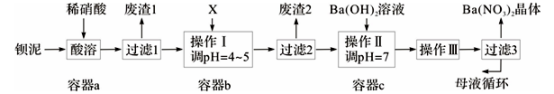
已知:i .Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7。
ii .Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小。
iii. Kap(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)Ba(FeO2)2中Fe的化合价是____ 。
(2)二氧化碳与水作用形成的碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式________________________ 。
(3)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式和必要的文字说明提纯原理:__________________ 。
(4)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为:__________ 。
(5)该厂结合本厂实际,选用的X为_____ (从下列选项中选择);废渣2为______ (写出化学式)。
① BaCl2 ②Ba(NO3)2 ③BaCO3 ④ Ba(OH)2
(6)过滤3后的母液应循环到容器____ 中。(填“a”、“b”或“c”)
(7)称取w g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m g,则该Ba(NO3)2的纯度为____ 。

已知:i .Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7。
ii .Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小。
iii. Kap(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)Ba(FeO2)2中Fe的化合价是
(2)二氧化碳与水作用形成的碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式
(3)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式和必要的文字说明提纯原理:
(4)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为:
(5)该厂结合本厂实际,选用的X为
① BaCl2 ②Ba(NO3)2 ③BaCO3 ④ Ba(OH)2
(6)过滤3后的母液应循环到容器
(7)称取w g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m g,则该Ba(NO3)2的纯度为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】利用酸解法制钛白粉产生的废液[含有大量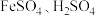 和少量
和少量 、
、 ],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
],生产铁红和补血剂乳酸亚铁。其生产步骤如下:

已知: 可溶于水,在水中可以电离为
可溶于水,在水中可以电离为 和
和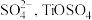 水解成
水解成 沉淀为可逆反应;乳酸亚铁晶体的化学式为:
沉淀为可逆反应;乳酸亚铁晶体的化学式为: 。请回答:
。请回答:
(1)步骤①加入铁屑的目的一是还原少量 ;二是使少量
;二是使少量 转化为
转化为 滤渣,用平衡移动的原理解释得到滤渣的原因
滤渣,用平衡移动的原理解释得到滤渣的原因________ 。
(2)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为________ 。
(3)步骤④的离子方程式是______ 。
(4)步骤⑥所得溶液需隔绝空气______ 、________ 过滤、洗涤、干燥得乳酸亚铁晶体。该晶体存放时应____________ 。
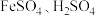 和少量
和少量 、
、 ],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
已知:
 可溶于水,在水中可以电离为
可溶于水,在水中可以电离为 和
和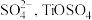 水解成
水解成 沉淀为可逆反应;乳酸亚铁晶体的化学式为:
沉淀为可逆反应;乳酸亚铁晶体的化学式为: 。请回答:
。请回答:(1)步骤①加入铁屑的目的一是还原少量
 ;二是使少量
;二是使少量 转化为
转化为 滤渣,用平衡移动的原理解释得到滤渣的原因
滤渣,用平衡移动的原理解释得到滤渣的原因(2)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为
(3)步骤④的离子方程式是
(4)步骤⑥所得溶液需隔绝空气
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用含锌物料(含 FeO、CuO、FeS、CuS 等杂质)制取活性 ZnO 的流程如下:
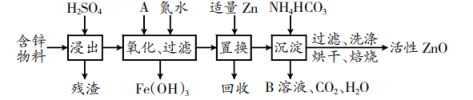
已知:各离子开始沉淀及完全沉淀时的 pH 如表所示。
(1)含锌废料中的少量 CuS 和 ZnS,加入硫酸后 ZnS 可以溶解而 CuS 不溶,则相同温度下Ksp(CuS)_______ Ksp(ZnS)(选填“>”、“<”或“=”)。
(2)第二步中先加入 A 物质的目的是_______ ,物质 A 可使用下列物质中的 _______ 。
A. O2 B. KMnO4 C. H2O2 D. Cl2
(3)加入氨水的目的是调节溶液的 pH,pH 应控制的范围是_______ 。
(4)加入 Zn 粉发生反应的离子方程式有_______ 。
(5)B 溶液溶质的化学式是_______ ,其在农业生产中的一种用途是 _______ 。

已知:各离子开始沉淀及完全沉淀时的 pH 如表所示。
| 离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 6.34 | 1.48 | 6.2 | 4.7 |
| 完全沉淀的pH | 9.7 | 3.2 | 8.0 | 6.7 |
(2)第二步中先加入 A 物质的目的是
A. O2 B. KMnO4 C. H2O2 D. Cl2
(3)加入氨水的目的是调节溶液的 pH,pH 应控制的范围是
(4)加入 Zn 粉发生反应的离子方程式有
(5)B 溶液溶质的化学式是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】三氯化铬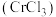 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
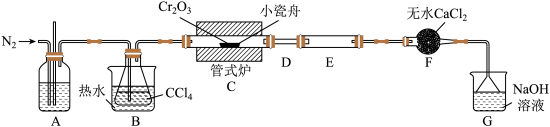
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:① (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;
②碱性条件下, 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。
回答下列问题:
(1)基态 原子的简化核外电子排布式为
原子的简化核外电子排布式为___________ 。
(2)无水 的作用是
的作用是___________ 。
(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过___________ (填操作方法)使实验继续进行。
(4)装置G中发生生成两种盐的反应的化学方程式为___________ 。
(5)测定产品中 质量分数的实验步骤如下:
质量分数的实验步骤如下:
I.取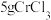 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;
II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;
III.取 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。
①该样品中 的质量分数为
的质量分数为___________  (保留小数点后两位,
(保留小数点后两位,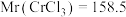 )
)
②下列操作将导致产品中 质量分数测定值偏低的是
质量分数测定值偏低的是___________ (填标号)。
A.步骤I中未继续加热一段时间
B.步骤III中所用 溶液已变质
溶液已变质
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
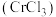 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:①
 (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;②碱性条件下,
 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。回答下列问题:
(1)基态
 原子的简化核外电子排布式为
原子的简化核外电子排布式为(2)无水
 的作用是
的作用是(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过
(4)装置G中发生生成两种盐的反应的化学方程式为
(5)测定产品中
 质量分数的实验步骤如下:
质量分数的实验步骤如下:I.取
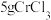 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使
 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;III.取
 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。①该样品中
 的质量分数为
的质量分数为 (保留小数点后两位,
(保留小数点后两位,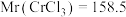 )
)②下列操作将导致产品中
 质量分数测定值偏低的是
质量分数测定值偏低的是A.步骤I中未继续加热一段时间
B.步骤III中所用
 溶液已变质
溶液已变质C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
您最近半年使用:0次





