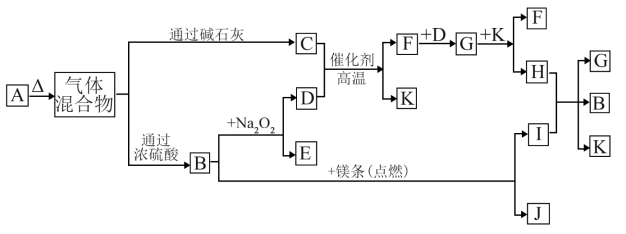
测定铜的相对原子质量。氨气是一种无色、有强烈的刺激气味的气体。氨气具有还原性,可以与灼热的氧化铜反应可得到氮气和金属铜。某课外小组利用该反应和下列装置测定Cu的相对原子质量。

(1)按正确的顺序连接上述实验装置:___________ 。
(2)在使用石英管进行加热时,需要对通入石英管的气体进行干燥,否则在较高的温度下,若气体不纯则有可能引起装置炸裂。D装置为U形干燥管,其目的就是干燥氨气,防止通入C中引起石英管破裂。B中可选用的干燥剂是
(3)C试管被用于制备反应所需要的氨气,其中盛装的是足量的氯化铵和氢氧化钙的混合物。C中的反应的化学方程式为___________ 。
(4)B中观察到的现象是___________ ,实验时,E中收集到的物质是___________ 。
(5)为准确测定铜的相对原子质量,课外小组正确组建装置进行实验,并在实验中测得如下数据:
①实验前,称量空B管的质量为ag:
②在B管中装入药品,称得B管和CuO样品的总质量为bg:
③待充分加热后,撤去酒精灯,使B管和Cu粉冷却到室温,再称量其总质量为cg。
根据以上数据,列出计算Cu的相对原子质量的计算式: =
=___________ 。(用含字母的代数式表示)

(1)按正确的顺序连接上述实验装置:
(2)在使用石英管进行加热时,需要对通入石英管的气体进行干燥,否则在较高的温度下,若气体不纯则有可能引起装置炸裂。D装置为U形干燥管,其目的就是干燥氨气,防止通入C中引起石英管破裂。B中可选用的干燥剂是
| A.浓硫酸 | B.无水 | C.无水硫酸铜 | D.碱石灰 |
(4)B中观察到的现象是
(5)为准确测定铜的相对原子质量,课外小组正确组建装置进行实验,并在实验中测得如下数据:
①实验前,称量空B管的质量为ag:
②在B管中装入药品,称得B管和CuO样品的总质量为bg:
③待充分加热后,撤去酒精灯,使B管和Cu粉冷却到室温,再称量其总质量为cg。
根据以上数据,列出计算Cu的相对原子质量的计算式:
 =
=
更新时间:2023-04-24 11:06:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组制取氨气,并利用氨气和氧化铜反应来验证氨气分子中氮、氢原子的个数比,按如图所示装置进行实验。已知:氨气与灼热的氧化铜反应,生成铜、水和氮气。
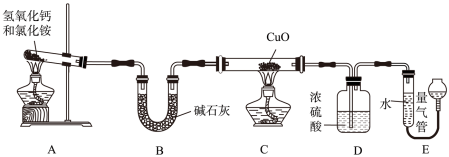
(1)装置A 中发生反应的化学方程式为_______ 。
(2)实验中,先断开C与D,加热装置_______ (填“A”或“C”)片刻,再连接C与D,加热另一个装置,其目的是_______ 。
(3)装置C 的玻璃管中发生反应的化学方程式为_______ ,若固体的质量减少3.2g,则该反应中转移电子的物质的量为_______ 。
(4)称量反应前后,玻璃管(含固体物质)的质量分别为m1g、m2g;生成的氮气在标准状况下的体积为VL。用所测数据计算出氨气分子中氮、氢原子个数之比为_______ 。
(5)小组同学还测定了反应前后装置D(含药品)的质量和生成的氮气体积(在标准状况下)。由此数据计算出的氨气分子中氮、氢原子个数比小于理论值,其原因是_______ 。

(1)装置A 中发生反应的化学方程式为
(2)实验中,先断开C与D,加热装置
(3)装置C 的玻璃管中发生反应的化学方程式为
(4)称量反应前后,玻璃管(含固体物质)的质量分别为m1g、m2g;生成的氮气在标准状况下的体积为VL。用所测数据计算出氨气分子中氮、氢原子个数之比为
(5)小组同学还测定了反应前后装置D(含药品)的质量和生成的氮气体积(在标准状况下)。由此数据计算出的氨气分子中氮、氢原子个数比小于理论值,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组的同学利用下图所示实验装置进行 NH3 的制备、性质等实验。
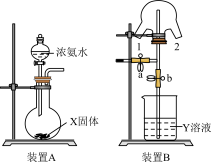
(1)装置 A 中的烧瓶内的 X 固体可选________
A.硫酸铜 B.氯化钙 C.五氧化二磷 D.生石灰
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,工业上也常用来检验氯气的管道是否漏气,请写出反应的化学方程式:___________
(3) 为防止环境污染, 以下装置( 盛放的液体均为水) 可用于吸收多余氨气的是_____
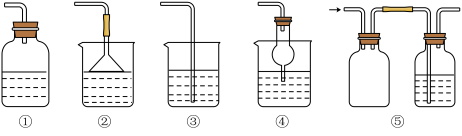
(4)有四个干燥的烧瓶,在常温常压下,向①瓶中装入干燥、纯净的氨气,②瓶中装入干燥的含一半空气的氨气,③瓶中装入干燥、纯净的二氧化氮,④瓶中装入干燥的体积比V(NO2):V(O2)=4∶1 的混合气体。做喷泉实验时四个烧瓶中所得溶液的物质的量浓度之比为(假设溶质不扩散)___________
A.2∶1∶2∶2 B.5∶5∶5∶4
C.1∶1∶1∶1 D.4∶4∶4∶5
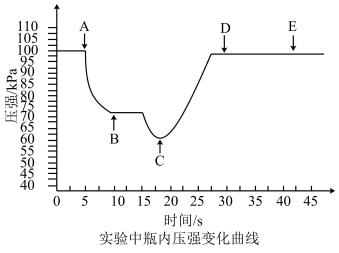
(5)可用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理:装置 A 与装置 B 相连,打开 a,关闭 b,开始实验,使三颈瓶内充满 NH3。将吸有 2 mL H2O 的胶头滴管塞进颈口 1,通过颈口 2 将数据采集器的探头插入三颈瓶中。打开 b,关闭 a,挤压胶头滴管,进行喷泉实验,电脑绘制三颈瓶内气压变化曲线如下图。该图中_______ 点时喷泉最剧烈。

(1)装置 A 中的烧瓶内的 X 固体可选
A.硫酸铜 B.氯化钙 C.五氧化二磷 D.生石灰
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,工业上也常用来检验氯气的管道是否漏气,请写出反应的化学方程式:
(3) 为防止环境污染, 以下装置( 盛放的液体均为水) 可用于吸收多余氨气的是
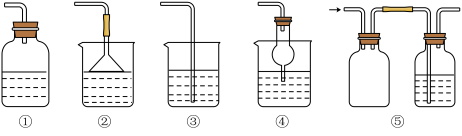
(4)有四个干燥的烧瓶,在常温常压下,向①瓶中装入干燥、纯净的氨气,②瓶中装入干燥的含一半空气的氨气,③瓶中装入干燥、纯净的二氧化氮,④瓶中装入干燥的体积比V(NO2):V(O2)=4∶1 的混合气体。做喷泉实验时四个烧瓶中所得溶液的物质的量浓度之比为(假设溶质不扩散)
A.2∶1∶2∶2 B.5∶5∶5∶4
C.1∶1∶1∶1 D.4∶4∶4∶5
(5)可用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理:装置 A 与装置 B 相连,打开 a,关闭 b,开始实验,使三颈瓶内充满 NH3。将吸有 2 mL H2O 的胶头滴管塞进颈口 1,通过颈口 2 将数据采集器的探头插入三颈瓶中。打开 b,关闭 a,挤压胶头滴管,进行喷泉实验,电脑绘制三颈瓶内气压变化曲线如下图。该图中

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮化铬(CrN)薄膜具有韧性高、耐磨性好、涂层结合强度高、更好的抗高温氧化性和抗腐蚀性以及内应力低等优点,在汽车工业、航空航天等领域取得了很好的应用效果。某化学兴趣小组利用下列装置进行氮化铬的制备(部分夹持装置已略),回答下列问题:
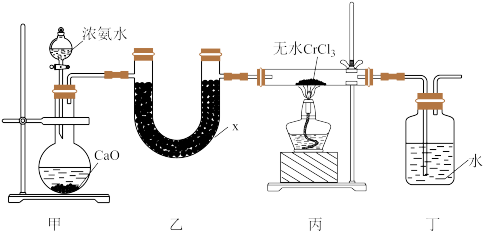
(1)仪器x的名称为________ ,x中盛有的试剂为干燥剂,该干燥剂可以是________ (填字母)。
a.浓硫酸 b.碱石灰 c.CaO d.无水CaCl2
(2)装置甲中CaO可用NaOH固体代替,其原因是_______________________________________________ 。
(3)若装置丙玻璃管中产生大量白烟,则发生反应的化学方程式为__________________________________ 。
(4)装置丁洗气瓶中水的作用是________________________________________ 。该装置是否合适?合适则写出合适的理由,不合适则说明改进措施:_____________________________________________________
(5)实验前,在装置丙中加入15.850g CrCl3,实验结束后,取出装置丙中的固体加热至质量不再减少,称量剩余固体质量为7.525g,则制备的产品纯度为______ %(保留小数点后一位)。

(1)仪器x的名称为
a.浓硫酸 b.碱石灰 c.CaO d.无水CaCl2
(2)装置甲中CaO可用NaOH固体代替,其原因是
(3)若装置丙玻璃管中产生大量白烟,则发生反应的化学方程式为
(4)装置丁洗气瓶中水的作用是
(5)实验前,在装置丙中加入15.850g CrCl3,实验结束后,取出装置丙中的固体加热至质量不再减少,称量剩余固体质量为7.525g,则制备的产品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
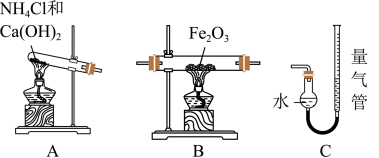
【推荐2】某研究性学习小组对实验室 制取、收集、吸收,以及
制取、收集、吸收,以及 的还原性探究进行了如下实验设计。回答下列问题:
的还原性探究进行了如下实验设计。回答下列问题:
Ⅰ. 的收集和吸收
的收集和吸收
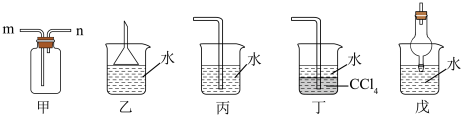
(1)若用图甲装置进行排空气法收集 ,气体应从
,气体应从_____ (填“m”或“n”)口进入。
(2)已知 难溶于
难溶于 。图乙、丙、丁、戊四种装置中,不能用来吸收
。图乙、丙、丁、戊四种装置中,不能用来吸收 的是
的是_____ 。
Ⅱ. 的还原性探究
的还原性探究
利用如图所示装置,进行 还原
还原 的反应。
的反应。
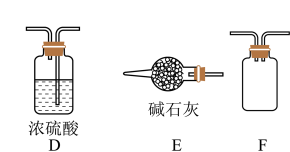
已知: 与
与 反应生成
反应生成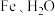 和无毒气体
和无毒气体 ,且
,且 不能被浓硫酸和碱石灰吸收。
不能被浓硫酸和碱石灰吸收。
(3)采用 装置作为制取
装置作为制取 的发生装置,写出该装置中发生反应的化学方程式:
的发生装置,写出该装置中发生反应的化学方程式:_____ 。
(4)按气流方向,装置连接顺序为_____ 。
 _____
_____ _____
_____ _____
_____ _____
_____ (填序号,每个装置只用一次)。装置连接后,首先应进行的操作是
(填序号,每个装置只用一次)。装置连接后,首先应进行的操作是_____ 。
(5)实验结束时,应先熄灭_____ (填“A”或“B”)装置的酒精灯。
(6)若称取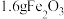 ,完全反应后,测得生成气体
,完全反应后,测得生成气体 的体积为
的体积为 (标准状况下),通过计算推测
(标准状况下),通过计算推测 中
中 与
与 反应的化学方程式为
反应的化学方程式为_____ 。
 制取、收集、吸收,以及
制取、收集、吸收,以及 的还原性探究进行了如下实验设计。回答下列问题:
的还原性探究进行了如下实验设计。回答下列问题:Ⅰ.
 的收集和吸收
的收集和吸收(1)若用图甲装置进行排空气法收集
 ,气体应从
,气体应从(2)已知
 难溶于
难溶于 。图乙、丙、丁、戊四种装置中,不能用来吸收
。图乙、丙、丁、戊四种装置中,不能用来吸收 的是
的是
Ⅱ.
 的还原性探究
的还原性探究利用如图所示装置,进行
 还原
还原 的反应。
的反应。

已知:
 与
与 反应生成
反应生成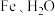 和无毒气体
和无毒气体 ,且
,且 不能被浓硫酸和碱石灰吸收。
不能被浓硫酸和碱石灰吸收。(3)采用
 装置作为制取
装置作为制取 的发生装置,写出该装置中发生反应的化学方程式:
的发生装置,写出该装置中发生反应的化学方程式:(4)按气流方向,装置连接顺序为
 _____
_____ _____
_____ _____
_____ _____
_____ (填序号,每个装置只用一次)。装置连接后,首先应进行的操作是
(填序号,每个装置只用一次)。装置连接后,首先应进行的操作是(5)实验结束时,应先熄灭
(6)若称取
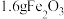 ,完全反应后,测得生成气体
,完全反应后,测得生成气体 的体积为
的体积为 (标准状况下),通过计算推测
(标准状况下),通过计算推测 中
中 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海水是人类宝贵的自然资源,从海水中可以提取多种化工原料,部分流程如图所示:
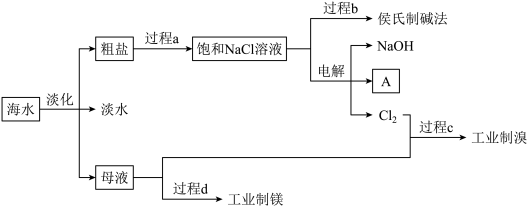
请回答下列问题:
(1)过程a为粗盐的精制。除去粗盐中的 、
、 、
、 时,需向经简单处理过的粗盐溶液中依次加入过量的
时,需向经简单处理过的粗盐溶液中依次加入过量的_______ 溶液、NaOH溶液以及_______ 溶液,过滤后加入适量盐酸。
(2)过程b的部分流程如下:
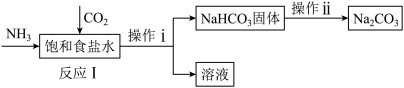
①实验室可用浓氨水与生石灰混合制取NH3,其化学方程式为_______ 。
②进行反应Ⅰ时,应先通入_______ (填“NH3”或“CO2”);实验室进行操作ⅰ时,所需要的硅酸盐仪器主要有_______ 。
③检验Na2CO3中含有的NaCl所需要的试剂为_______ (填名称)。
(3)电解饱和食盐水时会产生单质A,则单质A的化学式为_______ 。
(4)过程c为“吹出法”制溴。两次通入Cl2的目的是富集浓缩溴,若最终获得1molBr2,理论上需消耗的Cl2在标准状况下的体积为_______ L。
(5)过程d中制取无水MgCl2是关键。将 晶体加入二氯亚砜(SOCl2)中,加热即可获得三种产物,无水MgCl2和两种酸性气体,试写出该反应的化学方程式:
晶体加入二氯亚砜(SOCl2)中,加热即可获得三种产物,无水MgCl2和两种酸性气体,试写出该反应的化学方程式:_______ 。

请回答下列问题:
(1)过程a为粗盐的精制。除去粗盐中的
 、
、 、
、 时,需向经简单处理过的粗盐溶液中依次加入过量的
时,需向经简单处理过的粗盐溶液中依次加入过量的(2)过程b的部分流程如下:

①实验室可用浓氨水与生石灰混合制取NH3,其化学方程式为
②进行反应Ⅰ时,应先通入
③检验Na2CO3中含有的NaCl所需要的试剂为
(3)电解饱和食盐水时会产生单质A,则单质A的化学式为
(4)过程c为“吹出法”制溴。两次通入Cl2的目的是富集浓缩溴,若最终获得1molBr2,理论上需消耗的Cl2在标准状况下的体积为
(5)过程d中制取无水MgCl2是关键。将
 晶体加入二氯亚砜(SOCl2)中,加热即可获得三种产物,无水MgCl2和两种酸性气体,试写出该反应的化学方程式:
晶体加入二氯亚砜(SOCl2)中,加热即可获得三种产物,无水MgCl2和两种酸性气体,试写出该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】物质类别和元素的价态是学习研究物质性质的两个重要角度。根据硫元素的价类二维图回答问题:

(1)X的电子式为_______ ,若Z为钠的酸式盐,则25℃时,Z溶液显_______ (填“酸性”、“碱性”或“中性”)(25℃时, 的电离平衡常数为:
的电离平衡常数为: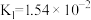 ,
,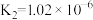 )。
)。
(2)①25℃时,取等体积的浓度均为0.1mol/L的X、W溶液,分别用等浓度的NaOH溶液中和,则消耗的NaOH溶液的体积为V1和V2,则V1_______ V2 (填“>”、“<”或“=”)。
②25℃时,将 的NaOH溶液与
的NaOH溶液与 的W溶液按照体积比为
的W溶液按照体积比为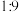 混合(忽略体积变化),测混合后溶液的pH=
混合(忽略体积变化),测混合后溶液的pH=_______ 。
(3)下表是 和
和 在常温下的电离平衡常数:
在常温下的电离平衡常数:
向 溶液中通入少量
溶液中通入少量 ,离子方程式为
,离子方程式为_______ 。
(4)某居民区靠近硫酸工厂,为监测该居民区的空气中Y的含量是否超标(已知居民区的空气中Y的含量以不超过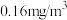 为达标),某化学小组进行如下实验:将标准状况下的空气20.00L (含
为达标),某化学小组进行如下实验:将标准状况下的空气20.00L (含 、
、 、
、 、Y气体等),缓慢通入足量氯水中,在所得溶液中加入稍过量的
、Y气体等),缓慢通入足量氯水中,在所得溶液中加入稍过量的 溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,测得其质量为0.466g。
溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,测得其质量为0.466g。
①将上述空气缓慢通入足量氯水后所得溶液的pH_______ (填“增大”或“减小”)。
②检验沉淀是否洗涤干净的方法是_______ 。
③通过计算得出 的含量为
的含量为_______ 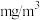 ,该居民区的空气中Y的含量
,该居民区的空气中Y的含量_______ 达标(填“已”或“未”)。

(1)X的电子式为
 的电离平衡常数为:
的电离平衡常数为: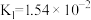 ,
,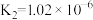 )。
)。(2)①25℃时,取等体积的浓度均为0.1mol/L的X、W溶液,分别用等浓度的NaOH溶液中和,则消耗的NaOH溶液的体积为V1和V2,则V1
②25℃时,将
 的NaOH溶液与
的NaOH溶液与 的W溶液按照体积比为
的W溶液按照体积比为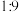 混合(忽略体积变化),测混合后溶液的pH=
混合(忽略体积变化),测混合后溶液的pH=(3)下表是
 和
和 在常温下的电离平衡常数:
在常温下的电离平衡常数: |  |
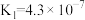 , ,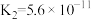 | 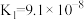 , ,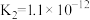 |
 溶液中通入少量
溶液中通入少量 ,离子方程式为
,离子方程式为(4)某居民区靠近硫酸工厂,为监测该居民区的空气中Y的含量是否超标(已知居民区的空气中Y的含量以不超过
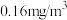 为达标),某化学小组进行如下实验:将标准状况下的空气20.00L (含
为达标),某化学小组进行如下实验:将标准状况下的空气20.00L (含 、
、 、
、 、Y气体等),缓慢通入足量氯水中,在所得溶液中加入稍过量的
、Y气体等),缓慢通入足量氯水中,在所得溶液中加入稍过量的 溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,测得其质量为0.466g。
溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,测得其质量为0.466g。①将上述空气缓慢通入足量氯水后所得溶液的pH
②检验沉淀是否洗涤干净的方法是
③通过计算得出
 的含量为
的含量为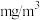 ,该居民区的空气中Y的含量
,该居民区的空气中Y的含量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】亚硝酰氯(NOCl)是有机物合成中的重要试剂,是一种红褐色液体或黄色气体,遇水易水解。某化学小组利用NO和Cl2在实验室中制备NOCl,装置如图。
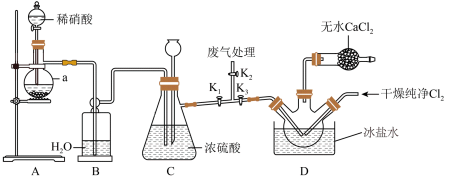
已知:沸点Cl2为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与O2反应。
回答下列问题:
(1)仪器a的名称:______ 。
(2)NO和氯气混合前,先关闭K3,打开K1、K2,操作的目的为______ 。
(3)装置C中长颈漏斗的作用是______ 。
(4)装置D中的温度区间应控制在_______ 。
(5)上述实验装置有一处不足,请指出不足之处:______ 。
(6)亚硝酰氯(NOCl)纯度的测定。取D中所得液体20g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶液于锥形瓶中,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知Ag2CrO4为砖红色固体)。
①滴定终点的现象:当滴入最后半滴AgNO3标准溶液后,______ 。
②亚硝酰氯(NOCl)的质量分数为_______ 。

已知:沸点Cl2为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与O2反应。
回答下列问题:
(1)仪器a的名称:
(2)NO和氯气混合前,先关闭K3,打开K1、K2,操作的目的为
(3)装置C中长颈漏斗的作用是
(4)装置D中的温度区间应控制在
(5)上述实验装置有一处不足,请指出不足之处:
(6)亚硝酰氯(NOCl)纯度的测定。取D中所得液体20g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶液于锥形瓶中,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知Ag2CrO4为砖红色固体)。
①滴定终点的现象:当滴入最后半滴AgNO3标准溶液后,
②亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】测血钙的含量时,进行如下实验:
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4 mol./L的KMnO4溶液。
(1)写出用KMn04滴定H2C2O4的离子方程式___________ 。
(2)判断滴定终点的方法是____________ 。
(3)③步骤中取酸性KMnO4溶液溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的血钙质量分数_______ (填“偏大”、“偏小”或“无影响”)。
(4)计算:血液中含钙离子的浓度为_____ mol/L。
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4 mol./L的KMnO4溶液。
(1)写出用KMn04滴定H2C2O4的离子方程式
(2)判断滴定终点的方法是
(3)③步骤中取酸性KMnO4溶液溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的血钙质量分数
(4)计算:血液中含钙离子的浓度为
您最近一年使用:0次