下列说法正确的是
| A.SO2与CO2的分子立体构型均为直线形 |
| B. SiO2的键长大于CO2的键长,所以SiO2的熔点比CO2高 |
| C.H2O和NH3中的分子的极性和共价键的极性均相同 |
| D.分子晶体中一定存在共价键 |
更新时间:2023-04-27 13:43:05
|
相似题推荐
【推荐1】S和O可组成一系列负二价阴离子,结构如图。下列说法正确的是
| 硫酸根 | 焦硫酸根 | 连四硫酸根 | 硫代硫酸根 | 过二硫酸根 |
 | 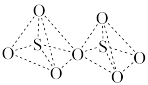 |  |  |  |
A.电负性 ,该系列离子中不存在非极性共价键 ,该系列离子中不存在非极性共价键 |
B.1mol焦硫酸根在水溶液中得2mol电子可生成 |
| C.2mol硫代硫酸根被氧化为1mol连四硫酸根转移2mol电子 |
| D.过二硫酸根具有极强氧化性,原因是其中S元素处于+7价 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述中,不正确的是
| A.含有共价键的物质一定是共价化合物 | B.H2O2中既含有极性键又含有非极性键 |
| C.CaO和NaCl晶体熔化时要破坏离子键 | D.H2SO4在熔融态不导电,属于分子晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】结构决定性质,下列判断正确的是
A.第二电离能: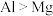 |
B.共价键键能: |
C.晶体的熔点:金刚石 晶体硅 晶体硅 |
D.分子的极性强弱: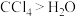 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具润滑性,其单层局部结构如图所示,下列关于该化合物的说法不正确 的是


| A.与石墨相比,(CF)x抗氧化性减弱 |
| B.与石墨相比,(CF)x导电性减弱 |
| C.(CF)x中C—C的键长比C—F长 |
| D.1 mol (CF)x中含有2.5x mol共价单键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】实验室常用氟化钙固体和浓硫酸混合加热制HF:CaF2+H2SO4(浓) CaSO4+2HF↑。下列关于该反应的说法错误的是
CaSO4+2HF↑。下列关于该反应的说法错误的是
 CaSO4+2HF↑。下列关于该反应的说法错误的是
CaSO4+2HF↑。下列关于该反应的说法错误的是| A.该反应利用了浓硫酸的酸性和难挥发性 |
| B.CaF2晶体中Ca2+和F-的配位数之比为1:2 |
| C.影响H2SO4和CaSO4熔点的作用力不同 |
| D.HF是极性分子且分子极性强于HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】光气 是一种重要的有机中间体。反应
是一种重要的有机中间体。反应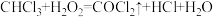 可用于制备光气。下列有关叙述正确的是
可用于制备光气。下列有关叙述正确的是
 是一种重要的有机中间体。反应
是一种重要的有机中间体。反应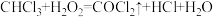 可用于制备光气。下列有关叙述正确的是
可用于制备光气。下列有关叙述正确的是A. 为非极性分子 为非极性分子 | B.氯原子的结构示意图为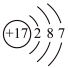 |
C. 的电子式为 的电子式为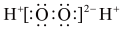 | D.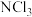 分子的空间构型为平面三角形 分子的空间构型为平面三角形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述正确的是
| A.离子晶体中,只存在离子键,不可能存在其它化学键 |
| B.可燃冰中甲烷分子与水分子之间存在氢键 |
C.Na2O2、NaHSO4晶体中的阴、阳离子个数比均为1 2 2 |
| D.晶体熔点:金刚石>食盐>冰>干冰 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科学家在相当于110万大气压下合成了一种稳定的氦钠化合物,结构如图所示:小球代表Na,正方体代表He,小正方体代表共用电子,共用电子被迫集中在晶体结构的立方空间内。下列说法错误的是


| A.该物质的化学式为Na2He | B.极高的压力,可以影响He的化学性质 |
| C.该物质固态时能够导电 | D.Na的配位数为4 |
您最近一年使用:0次

 杂化
杂化 键和π键
键和π键 的结构,图(b)为固体
的结构,图(b)为固体 中存在的三聚分子。下列说法不正确的是
中存在的三聚分子。下列说法不正确的是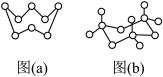
 的熔、沸点高很多
的熔、沸点高很多


