下列实验操作正确且能达到目的的是
| 选项 | 目的 | 操作 |
| A. | 根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 | 取5mL0.1mol/LFeCl3溶液,滴加0.1mol/LKI溶液1mL,充分反应 |
| B. | 探究浓度对反应速率的影响 | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液,观察实验现象 |
| C. | 证明氧化性:Fe3+>I2 | 向黄色的Fe(NO3)3溶液中滴加氢碘酸 |
| D. | 证明非金属性:C>Si | 用SiO2与焦炭在高温条件下制备粗硅 |
| A.A | B.B | C.C | D.D |
更新时间:2023-04-27 18:03:58
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】将6.4g铜投入30mL一定浓度的硝酸中,恰好完全反应,产生标准状况下的NO和NO2混合气体共2.24L。则下列叙述正确的是
| A.NO体积为0.56L | B.原硝酸浓度10.0mol/L |
| C.NO和NO2物质的量之比为2∶1 | D.体现酸性的硝酸为0.1mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列离子方程式正确的是
A.小苏打中加入过量的澄清石灰水: |
B.偏铝酸钠溶液中通入过量的CO2: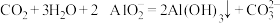 |
C. 溶液使酸性 溶液使酸性 溶液褪色: 溶液褪色: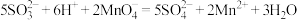 |
D. 溶液中加入过量HI溶液: 溶液中加入过量HI溶液: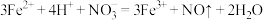 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某白色固体样品,可能含有 、
、 、
、 、
、 、
、 中的一种或几种。对该样品进行如下实验:
中的一种或几种。对该样品进行如下实验:
①取少量固体加入足量水中,固体部分溶解;
②取①中滤液做焰色试验,透过蓝色钴玻璃未观察到紫色;
③取①中滤渣,向其中加入足量的盐酸,产生气泡,固体部分溶解.
下列说法不正确的是
 、
、 、
、 、
、 、
、 中的一种或几种。对该样品进行如下实验:
中的一种或几种。对该样品进行如下实验:①取少量固体加入足量水中,固体部分溶解;
②取①中滤液做焰色试验,透过蓝色钴玻璃未观察到紫色;
③取①中滤渣,向其中加入足量的盐酸,产生气泡,固体部分溶解.
下列说法不正确的是
A.固体粉末中一定不含 |
B.固体粉末中一定含有 和 和 |
C.取①中滤液,加入硝酸酸化的 溶液,若未产生白色沉淀,则样品中无 溶液,若未产生白色沉淀,则样品中无 |
D.为进一步确定原样品组成,可以向③未溶解的固体中加入 溶液 溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列叙述正确的是( )
| A.酸性氧化物均与水反应生成对应的酸 |
| B.将NaOH溶液逐滴加入FeCl3溶液可制备Fe(OH)3胶体 |
| C.电化学腐蚀是造成金属腐蚀的主要原因 |
| D.碱石灰、玻璃、生石灰、漂白粉都是混合物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后,一定不可能出现的情况是
| A.溶液中不含Cu2+ | B.溶液中含有Fe3+、Cu2、Fe2+ |
| C.剩余固体只有铁 | D.剩余固体中只有Cu |
您最近一年使用:0次
【推荐2】向100mL由稀 与稀
与稀 组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
 与稀
与稀 组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
A.0A段的离子反应为 |
B.AB段的离子反应为 |
C.反应开始前溶液中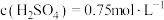 |
D.BC段的离子反应为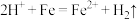 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】化学是一门以实验为基础的科学,其中控制变量思想在探究实验中有重要应用。某研究小组以反应 为例探究外界条件对化学反应速率的影响。实验时,分别量取
为例探究外界条件对化学反应速率的影响。实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法正确的是
溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法正确的是
 为例探究外界条件对化学反应速率的影响。实验时,分别量取
为例探究外界条件对化学反应速率的影响。实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法正确的是
溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法正确的是| 实验序号 | 实验温度/℃ | 酸性 溶液 溶液 |  溶液 溶液 |  | 溶液颜色褪至无色所用时间/s | ||
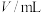 |  | 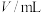 |  | 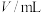 | |||
| ① | 20 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| ② | 20 | 2 | 0.02 | 2 | 0.1 | 2 | 8 |
| ③ | 45 | 2 | 0.02 | 2 | 0.1 | x |  |
| A.x=3 |
B.用 的 的 溶液也能达到目的 溶液也能达到目的 |
C. , ,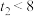 |
| D.利用实验①③探究温度对化学反应速率的影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某反应A(g)+B(g)→C(g)+D(g)的速率方程为v=k•cm(A)•cn(B),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为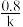 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:
下列说法不正确 的是
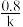 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:| c(A)/(mol•L-1) | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 | c1 |
| c(B)/(mol•L-1) | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 | c2 |
| v/(10-3mol•L-1•min-1) | 1.6 | 3.2 | v1 | 3.2 | v2 | 4.8 |
| A.上述表格中的c1=0.75、v2=6.4 |
| B.该反应的速率常数k=6.4×10-3min-1 |
| C.在过量的B存在时,反应掉93.75%的A所需的时间是500min |
| D.升温、加入催化剂、缩小容积(加压),使k增大导致反应的瞬时速率加快 |
您最近一年使用:0次

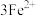 +NO
+NO +
+ =NO↑+
=NO↑+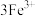 +2H2O
+2H2O +
+ +
+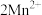 +2H2O
+2H2O +HCO
+HCO =MgCO3↓+H2O
=MgCO3↓+H2O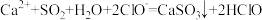
 含
含 、FeO、
、FeO、 、
、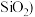 中加入适量硫酸溶液,分别取浸取液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
中加入适量硫酸溶液,分别取浸取液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是 :
: 、
、 、
、 、
、
 、
、 、
、 、
、
 、
、 、
、


