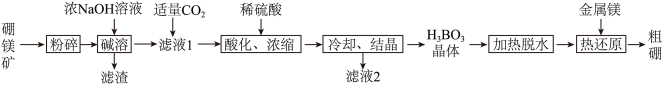
单质硼是高效的中子吸收剂,一种利用硼镁矿(Mg2B2O5•H2O)制备粗硼的工艺流程如图所示。
(1)Mg2B2O5•H2O中硼元素的化合价为_____ 。
(2)碱溶后所得滤液1的主要成分为NaBO2,则滤渣为(填化学式)_____ 。
(3)向滤液1中通入适量CO2后得到硼砂(Na2B4O7•10H2O),将硼砂溶于热水后,用硫酸调节溶液的pH值为2~3以制备H3BO3,该反应的离子方程式为_____ ,已知H3BO3是一元弱酸,但自身不能电离出氢离子,其电离方程式为_____ 。
(4)滤液2的主要成分是_____ (填化学式)。
(5)加热硼酸脱水得到氧化物,热还原得到粗硼的化学方程式为_____ ,上述滤渣经过一系列转化可得金属镁,若硼镁矿中硼、镁元素充分利用,理论上制得1.1吨硼时,需要额外提供金属镁的质量为_____ kg。
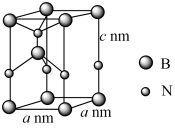
(6)单质硼是制备功能陶瓷BN的原料,某种BN功能陶瓷晶体属于四方晶系,晶胞参数如图。该功能材料的化学式为_____ ,设NA为阿佛加德罗常数的值,该BN晶体的密度为_____ g•cm-3。

(1)Mg2B2O5•H2O中硼元素的化合价为
(2)碱溶后所得滤液1的主要成分为NaBO2,则滤渣为(填化学式)
(3)向滤液1中通入适量CO2后得到硼砂(Na2B4O7•10H2O),将硼砂溶于热水后,用硫酸调节溶液的pH值为2~3以制备H3BO3,该反应的离子方程式为
(4)滤液2的主要成分是
(5)加热硼酸脱水得到氧化物,热还原得到粗硼的化学方程式为
(6)单质硼是制备功能陶瓷BN的原料,某种BN功能陶瓷晶体属于四方晶系,晶胞参数如图。该功能材料的化学式为

更新时间:2023-05-26 23:09:46
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】NiSO4·6H2O是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生产电池、医药工业、催化行业以及印染工业等行业中。由一种废料(主要成分是铁镍合金,还含有铜、镁、硅的氧化物)为原料制取NiSO4·6H2O步骤如下:
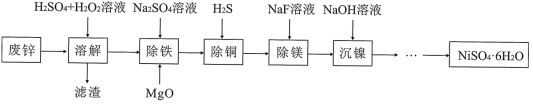
已知:①镍能溶于稀酸但溶解不完全,通常表现为+2价;
②常温下Ksp(MgF2)=6.4×10-9, Ka(HF)=6.3×10-4;
(1)“溶解”时加入H2O2溶液的目的是___________ 。
(2)“除铁”时生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出其离子方程式___________ 。
(3)向“除铜”后的滤液中加入NaF溶液,使Mg2+转化为MgF2沉淀除去。若溶液的pH偏低,将会导致MgF2沉淀不完全,其原因是___________ 。
(4)“沉镍”后所得滤液中,可循环使用的主要溶质为___________ (填化学式)。
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的化学方程式为___________ 。
(6)在制备NiSO4·6H2O晶体时,常用无水乙醇代替蒸馏水做洗涤剂,原因是___________ 。

已知:①镍能溶于稀酸但溶解不完全,通常表现为+2价;
②常温下Ksp(MgF2)=6.4×10-9, Ka(HF)=6.3×10-4;
(1)“溶解”时加入H2O2溶液的目的是
(2)“除铁”时生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出其离子方程式
(3)向“除铜”后的滤液中加入NaF溶液,使Mg2+转化为MgF2沉淀除去。若溶液的pH偏低,将会导致MgF2沉淀不完全,其原因是
(4)“沉镍”后所得滤液中,可循环使用的主要溶质为
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的化学方程式为
(6)在制备NiSO4·6H2O晶体时,常用无水乙醇代替蒸馏水做洗涤剂,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海水中蕴藏着丰富的资源,经加工处理可制取钠、氯气、溴和碘等化学物质。
(1)已知 难溶于水,是黄色沉淀。
难溶于水,是黄色沉淀。 的一种制备方法如图所示:
的一种制备方法如图所示:

加入 粉进行转化反应最终得到
粉进行转化反应最终得到 溶液的离子方程式为
溶液的离子方程式为__________________________ 。
(2)已知氧化性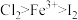 ,在通入
,在通入 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为_________________________ ;若反应物用量比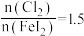 时,氧化产物为
时,氧化产物为_____________ (填化学式)。
(3)以 为原料制备
为原料制备 的方法是:先向
的方法是:先向 溶液中加入足量的
溶液中加入足量的 (与
(与 为同类盐),生成碘化物;再向混合溶液中加入酸化的
为同类盐),生成碘化物;再向混合溶液中加入酸化的 溶液,反应得到
溶液,反应得到 。上述过程制备
。上述过程制备 的离子方程式为
的离子方程式为_______________________________ ②_______________________________
(4)提取粗盐后的母液中含较高浓度的溴元素。用以获取液溴,流程如下。

①“萃取”时,使用一定体积的有机萃取剂,为提高 的萃取率,应采取的措施为
的萃取率,应采取的措施为___________________ ,萃取后静置,进行_________________ (填操作名称),可得到溴的有机溶液。
②“反萃取”时, 与
与 溶液反应生成
溶液反应生成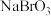 与
与 。该反应生成的
。该反应生成的 与
与 物质的量之比为
物质的量之比为_______________ 。
(1)已知
 难溶于水,是黄色沉淀。
难溶于水,是黄色沉淀。 的一种制备方法如图所示:
的一种制备方法如图所示:
加入
 粉进行转化反应最终得到
粉进行转化反应最终得到 溶液的离子方程式为
溶液的离子方程式为(2)已知氧化性
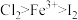 ,在通入
,在通入 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为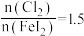 时,氧化产物为
时,氧化产物为(3)以
 为原料制备
为原料制备 的方法是:先向
的方法是:先向 溶液中加入足量的
溶液中加入足量的 (与
(与 为同类盐),生成碘化物;再向混合溶液中加入酸化的
为同类盐),生成碘化物;再向混合溶液中加入酸化的 溶液,反应得到
溶液,反应得到 。上述过程制备
。上述过程制备 的离子方程式为
的离子方程式为(4)提取粗盐后的母液中含较高浓度的溴元素。用以获取液溴,流程如下。

①“萃取”时,使用一定体积的有机萃取剂,为提高
 的萃取率,应采取的措施为
的萃取率,应采取的措施为②“反萃取”时,
 与
与 溶液反应生成
溶液反应生成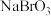 与
与 。该反应生成的
。该反应生成的 与
与 物质的量之比为
物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】锰元素能形成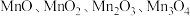 等多种氧化物,其中大颗粒
等多种氧化物,其中大颗粒 是重要的电池材料。工业上以碳酸锰矿(主要成分为
是重要的电池材料。工业上以碳酸锰矿(主要成分为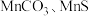 ),和软锰矿(主要成分为
),和软锰矿(主要成分为 )为原料制取
)为原料制取 。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
已知: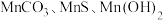 常温下皆为难溶于水的固体,硫化氢
常温下皆为难溶于水的固体,硫化氢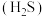 是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
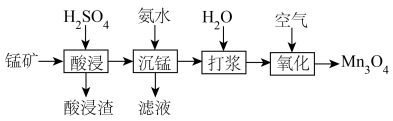
(1)“酸浸”: 溶于硫酸的离子方程式:
溶于硫酸的离子方程式:___________ 。
(2)“打浆”:将所得 制成悬浊液,可加快“氧化”反应速率的原因是
制成悬浊液,可加快“氧化”反应速率的原因是___________ 。
(3)“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。
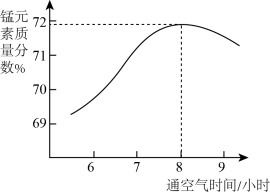
通空气超过8小时,产物中锰元素质量分数减小的原因是___________ 。
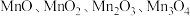 等多种氧化物,其中大颗粒
等多种氧化物,其中大颗粒 是重要的电池材料。工业上以碳酸锰矿(主要成分为
是重要的电池材料。工业上以碳酸锰矿(主要成分为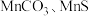 ),和软锰矿(主要成分为
),和软锰矿(主要成分为 )为原料制取
)为原料制取 。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。已知:
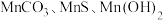 常温下皆为难溶于水的固体,硫化氢
常温下皆为难溶于水的固体,硫化氢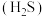 是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
(1)“酸浸”:
 溶于硫酸的离子方程式:
溶于硫酸的离子方程式:(2)“打浆”:将所得
 制成悬浊液,可加快“氧化”反应速率的原因是
制成悬浊液,可加快“氧化”反应速率的原因是(3)“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。

通空气超过8小时,产物中锰元素质量分数减小的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜具有多种化合物,在工业生产中有重要作用。如醋酸二氨合铜溶液用来吸收合成氨工业中的CO,防止催化剂中毒,该反应是:[Cu(NH3)2]Ac+CO+NH3⇌[Cu(NH3)3CO]Ac(Ac-代表CH3COO-)。回答下列问题:
(1)基态铜原子的核外电子排布式为_______ 。
(2)C、N、O三种元素的电负性由大到小的顺序为_______ 。
(3)NH3的VSEPR构型为_______ ,CO的电子式为_______ 。
(4)配合物[Cu(NH3)3CO]Ac中铜元素的化合价为_______ ,中心原子的配位数为_______ ,CH3COO-中碳原子的杂化方式为_______ ,该化合物存在的化学键类型为_______ 。
(5)从电子排布的角度解释一价铜比二价铜稳定的原因_______ 。
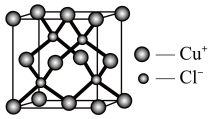
(6)铜的另一种化合物CuCl可用作有机合成的催化剂,其晶胞结构如图所示,则晶胞中Cu的配位数为_______ ,已知晶胞中Cu与Cl的最短距离为apm,则晶体密度ρ=_______ g/cm3(用NA表示阿伏加德罗常数)。
(1)基态铜原子的核外电子排布式为
(2)C、N、O三种元素的电负性由大到小的顺序为
(3)NH3的VSEPR构型为
(4)配合物[Cu(NH3)3CO]Ac中铜元素的化合价为
(5)从电子排布的角度解释一价铜比二价铜稳定的原因
(6)铜的另一种化合物CuCl可用作有机合成的催化剂,其晶胞结构如图所示,则晶胞中Cu的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】C、O、Si、S、Fe是重要的化学元素,在中学化学中对它们的单质和化合物的研究颇多。
(1)C、O、Si三种元素第一电离能由大到小的顺序是_______________________ 。
(2)CS2是重要的溶剂,CS2中C原子的杂化方式为_____________ ,其空间构型为_______________ 。
(3)基态Fe原子中,核外电子占据最高能层的符号是________ ,占据该能层电子的电子云轮廓图形状为_______________ 。
(4)晶胞推导有助于我们理解晶体结构。
①将NaCl晶胞(如右图)中的所有C1-去掉,并将Na+全部换成Si原子,再在间隔的“小立方体”中心处各放置一个Si原子便构成了晶体Si的一个晶胞,若再在每两个距离最近的Si原子中心连线的中点处增添一个O原子,便构成了SiO2晶胞。由此可推算SiO2晶胞中有______ 个Si原子,______ 个O原子。
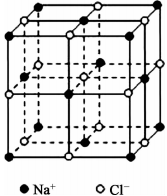
②简述利用NaCl晶胞推导出CsC1晶胞的方法:____________________________________ 。
(1)C、O、Si三种元素第一电离能由大到小的顺序是
(2)CS2是重要的溶剂,CS2中C原子的杂化方式为
(3)基态Fe原子中,核外电子占据最高能层的符号是
(4)晶胞推导有助于我们理解晶体结构。
①将NaCl晶胞(如右图)中的所有C1-去掉,并将Na+全部换成Si原子,再在间隔的“小立方体”中心处各放置一个Si原子便构成了晶体Si的一个晶胞,若再在每两个距离最近的Si原子中心连线的中点处增添一个O原子,便构成了SiO2晶胞。由此可推算SiO2晶胞中有

②简述利用NaCl晶胞推导出CsC1晶胞的方法:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为__________ 洪特规则内容_____________
泡利不相容原理内容______________________
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)__________ I1(Cu)(填“大于”或“小于”)。原因是__________
(3)ZnF2具有较高的熔点(872℃ ),其化学键类型是__________ ;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是__________
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为__________ ,配位数为____ 六棱柱底边边长为a cm,高为c cm,阿伏加 德罗常数的值为NA,Zn的密度为__________ g·cm-3(列出计算式)。

(1)Zn原子核外电子排布式为
泡利不相容原理内容
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(3)ZnF2具有较高的熔点(872℃ ),其化学键类型是
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】 (二氯六氨合镍)是一种镍的配合物,实验室制备过程及部分装置如下:
(二氯六氨合镍)是一种镍的配合物,实验室制备过程及部分装置如下: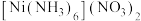 、
、 均为可溶于水、不溶于浓氨水和乙醇的蓝紫色晶体,水溶液均显碱性。
均为可溶于水、不溶于浓氨水和乙醇的蓝紫色晶体,水溶液均显碱性。
② 在热水中分解。
在热水中分解。
请回答:
(1)步骤Ⅰ、Ⅱ中须要控制反应温度在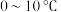 ,分别可采取的措施是
,分别可采取的措施是___________ 、___________ 。
(2)①步骤Ⅲ可在如图装置中进行,方框内装置 的作用是
的作用是___________ 。

②步骤Ⅲ经多步操作可获得蓝紫色晶2,针对多步操作,从下列选项选择合适操作(操作不能重复使用)并排序:蓝紫色晶体1→___→f→___→___→___→室温真空干燥________ 。
a.加入一定量的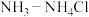 溶液 b.一定量的盐酸溶液
溶液 b.一定量的盐酸溶液
c.减压过滤 d.依次用浓氨水、乙醇洗涤
e.依次用稀氨水、冷水洗涤 f.用冰盐浴冷却
(3) 产品的纯度可用滴定法测定。某小组用沉淀滴定法测定制备的产品中
产品的纯度可用滴定法测定。某小组用沉淀滴定法测定制备的产品中 的质量分数,实验中以
的质量分数,实验中以 溶液作标准液,滴加少是
溶液作标准液,滴加少是 溶液作为指示剂。已知
溶液作为指示剂。已知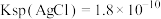 ,
,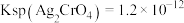 。
。
①下列关于滴定分析的操作,不正确的是___
A.锥形瓶中既可以盛放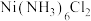 溶液,也可以盛放
溶液,也可以盛放 溶液
溶液
B.在接近滴定终点时,需用蒸馏水直接把该仪器尖端悬挂的液滴冲入锥形瓶
C.为减少沉淀吸附现象,滴定过程中需充分摇动锥形瓶中溶液,即时释放
D.滴定前,需用经干燥处理的 配成标准液来标定
配成标准液来标定 溶液,若
溶液,若 未干燥将使产品纯度计算结果偏大
未干燥将使产品纯度计算结果偏大
E. 溶液可装在使用聚四氟乙烯活塞的酸碱通用滴定管
溶液可装在使用聚四氟乙烯活塞的酸碱通用滴定管
②结果发现 质量分数明显偏高。分析其原因,发现配制
质量分数明显偏高。分析其原因,发现配制 待测液时少加了一种试剂。该试剂是
待测液时少加了一种试剂。该试剂是___ (填“稀盐酸”或“稀硝酸”或“稀硫酸”),添加该试剂的理由是___ 。
 (二氯六氨合镍)是一种镍的配合物,实验室制备过程及部分装置如下:
(二氯六氨合镍)是一种镍的配合物,实验室制备过程及部分装置如下: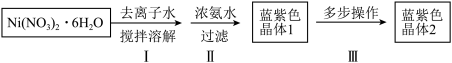
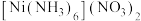 、
、 均为可溶于水、不溶于浓氨水和乙醇的蓝紫色晶体,水溶液均显碱性。
均为可溶于水、不溶于浓氨水和乙醇的蓝紫色晶体,水溶液均显碱性。②
 在热水中分解。
在热水中分解。请回答:
(1)步骤Ⅰ、Ⅱ中须要控制反应温度在
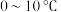 ,分别可采取的措施是
,分别可采取的措施是(2)①步骤Ⅲ可在如图装置中进行,方框内装置
 的作用是
的作用是
②步骤Ⅲ经多步操作可获得蓝紫色晶2,针对多步操作,从下列选项选择合适操作(操作不能重复使用)并排序:蓝紫色晶体1→___→f→___→___→___→室温真空干燥
a.加入一定量的
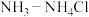 溶液 b.一定量的盐酸溶液
溶液 b.一定量的盐酸溶液c.减压过滤 d.依次用浓氨水、乙醇洗涤
e.依次用稀氨水、冷水洗涤 f.用冰盐浴冷却
(3)
 产品的纯度可用滴定法测定。某小组用沉淀滴定法测定制备的产品中
产品的纯度可用滴定法测定。某小组用沉淀滴定法测定制备的产品中 的质量分数,实验中以
的质量分数,实验中以 溶液作标准液,滴加少是
溶液作标准液,滴加少是 溶液作为指示剂。已知
溶液作为指示剂。已知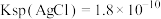 ,
,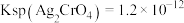 。
。①下列关于滴定分析的操作,不正确的是
A.锥形瓶中既可以盛放
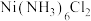 溶液,也可以盛放
溶液,也可以盛放 溶液
溶液B.在接近滴定终点时,需用蒸馏水直接把该仪器尖端悬挂的液滴冲入锥形瓶
C.为减少沉淀吸附现象,滴定过程中需充分摇动锥形瓶中溶液,即时释放

D.滴定前,需用经干燥处理的
 配成标准液来标定
配成标准液来标定 溶液,若
溶液,若 未干燥将使产品纯度计算结果偏大
未干燥将使产品纯度计算结果偏大E.
 溶液可装在使用聚四氟乙烯活塞的酸碱通用滴定管
溶液可装在使用聚四氟乙烯活塞的酸碱通用滴定管②结果发现
 质量分数明显偏高。分析其原因,发现配制
质量分数明显偏高。分析其原因,发现配制 待测液时少加了一种试剂。该试剂是
待测液时少加了一种试剂。该试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫代乙醇酸( )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
回答下列问题:
(1) 可通过以下反应制备:
可通过以下反应制备: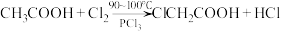 。
。
①简述 小于
小于 的原因:
的原因:___________ 。
② 属于
属于___________ (填“极性”或“非极性”)分子。
(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是___________ (填标号)。
(3)检查完气密性后,关闭 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。
①制备 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是___________ 。
②实验时不能用25%硝酸代替装置A中25%磷酸的原因是___________ 。
③装置C的作用是___________ 。
④装置D中多孔球泡的作用是___________ ;写出装置D中刚开始反应的离子方程式:___________ 。
⑤经过一系列分离提纯可获得 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是___________ 。
 )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。回答下列问题:
(1)
 可通过以下反应制备:
可通过以下反应制备: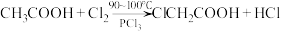 。
。①简述
 小于
小于 的原因:
的原因:②
 属于
属于(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是
| 操作 |
|
|
|
|
| 选项 | a | b | c | d |
(3)检查完气密性后,关闭
 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。①制备
 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是②实验时不能用25%硝酸代替装置A中25%磷酸的原因是
③装置C的作用是
④装置D中多孔球泡的作用是
⑤经过一系列分离提纯可获得
 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
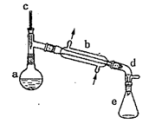
【推荐3】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:
可能用到的有关数据如下:
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是_______________________ ;b的名称是____________________ ;
(2)a中发生主要反应的化学方程式为_____________________________________ ;本实验最容易产生的有机副产物的结构简式为___________________ 。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________________ ,操作X的名称为_________________ 。
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______ 种不同化学环境的氢原子。
② 本实验所得环己烯的产率是______________ 。

可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是
(2)a中发生主要反应的化学方程式为
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有
② 本实验所得环己烯的产率是
您最近一年使用:0次