某同学进行如下实验:
已知:i.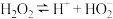 、
、
ii.BaO2是一种白色难溶于水的固体
下列说法不合理 的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 | 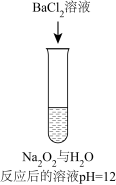 |  | 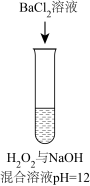 |  |  |
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
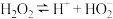 、
、
ii.BaO2是一种白色难溶于水的固体
下列说法
| A.实验①和②说明BaO2可溶于酸 |
| B.实验①和③得到的沉淀组成一样 |
| C.实验⑤的白色沉淀经检验为BaSO4,说明溶解度BaO2>BaSO4 |
| D.可用BaCl2、MnO2、H2O检验长期放置的Na2O2中是否含有Na2CO3 |
更新时间:2023-06-27 13:31:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】合成氨及其相关工业中,部分物质间的转化关系如图所示。下列说法正确的是


| A.反应Ⅰ、Ⅱ、Ⅲ、Ⅴ均属于氧化还原反应 |
| B.反应Ⅳ和Ⅵ中的部分产物可在上述流程中循环使用 |
| C.甲、乙、丙和丁四种物质中都含有氮元素 |
| D.制取物质丁时,先向饱和氯化钠溶液中通CO2至饱和再通NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某白色固体粉末由NaNO3、KCl、CuSO4、CaCO3、BaCl2中的一种或几种组成,进行如下实验:①进行焰色反应,火焰颜色呈黄色;②混合物溶于水,得到澄清透明溶液;③向②所得的溶液中通入NH3,产生沉淀,该白色粉末一定含有
| A.BaCl2、NaNO3 | B.KCl、CuSO4 | C.KCl、CaCO3、NaNO3 | D.CuSO4、NaNO3 |
您最近一年使用:0次
【推荐1】一定温度下,溴化银在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是


| A.向溴化银悬浊液中加入溴化钠溶液,溴化银的Ksp减小 |
| B.图中a点对应的是不饱和溶液 |
| C.向c点对应的溶液中加入少量0.1mol·L-1AgNO3溶液,则c(Br-)增大 |
| D.升高温度可以实现c点对应的溶液到b点对应的溶液的转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列指定反应的离子方程式正确的是
A.向 溶液中滴入少量 溶液中滴入少量 溶液: 溶液: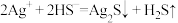 |
B.向二元弱酸亚磷酸 溶液中滴入少量烧碱溶液: 溶液中滴入少量烧碱溶液: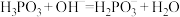 |
C.向 溶液中通入过量 溶液中通入过量 : : |
D. 通入石灰乳中制取漂白粉: 通入石灰乳中制取漂白粉: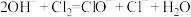 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】从照相底片未曝光的溴化银中回收银单质。工艺流程如下:
①未曝光的溴化银(AgBr)常用硫代硫酸钠 溶解(
溶解( 离子结构如图所示),反应生成含有
离子结构如图所示),反应生成含有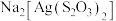 的废定影液
的废定影液
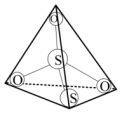
②在废定影液中加入 溶液使
溶液使 中的银转化为
中的银转化为 ,并使定影液再生
,并使定影液再生
③ 在空气中焙烧再转化为Ag和
在空气中焙烧再转化为Ag和
④通过电解法进行精炼银
下列说法正确的是
①未曝光的溴化银(AgBr)常用硫代硫酸钠
 溶解(
溶解( 离子结构如图所示),反应生成含有
离子结构如图所示),反应生成含有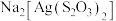 的废定影液
的废定影液
②在废定影液中加入
 溶液使
溶液使 中的银转化为
中的银转化为 ,并使定影液再生
,并使定影液再生③
 在空气中焙烧再转化为Ag和
在空气中焙烧再转化为Ag和
④通过电解法进行精炼银
下列说法正确的是
A.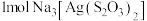 中含有 中含有 键数为8mol 键数为8mol |
B.流程②中,向 溶液中加入少量NaOH, 溶液中加入少量NaOH, 的值减少 的值减少 |
C.流程③中, 在过量的空气中焙烧可以直接转化为 在过量的空气中焙烧可以直接转化为 |
D.流程④中,精炼银时使用 溶液做电解液,纯银作阳极 溶液做电解液,纯银作阳极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列类比或推理合理的是
| 已知 | 方法 | 结论 | |
| A | 沸点: | 类比 | 沸点: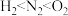 |
| B | 酸性: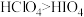 | 类比 | 酸性: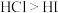 |
| C | 金属性: | 推理 | 氧化性: |
| D |  : : | 推理 | 溶解度: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.pH<7的溶液一定是酸性溶液 |
| B.常温时,pH=5的溶液和pH=3的溶液相比,前者c(OH-)是后者100倍 |
| C.25℃时,向饱和AgCl水溶液中加入盐酸,Ksp变小 |
| D.25℃时,向CaCl2溶液中通入CO2,有白色沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】为验证银氨溶液中也存在[Ag(NH3)2]+(aq) Ag+(aq)+2NH3(aq)络合平衡体系,特设计如图实验:
Ag+(aq)+2NH3(aq)络合平衡体系,特设计如图实验:
下列说法不正确的是
 Ag+(aq)+2NH3(aq)络合平衡体系,特设计如图实验:
Ag+(aq)+2NH3(aq)络合平衡体系,特设计如图实验:| 实验 | 试剂 | 现象 | |
| 试管 | 滴管 | ||
| 2mL[Ag(NH3)2]+溶液 | 6滴0.1mol•L-1KCl溶液 | I中无明显现象 |
| 6滴饱和KCl溶液 | II中产生白色沉淀 | ||
| 6滴0.1mol•L-1KI溶液 | III中产生黄色沉淀 | ||
| 6滴0.1mol•L-1HCl溶液 | IV中产生白色沉淀 | ||
| A.通过I、II对比,说明II中能生成沉淀的原因是c(Cl-)•c(Ag+)>Ksp(AgCl) |
| B.通过I、III对比,说明Ksp(AgCl)>Ksp(AgI) |
| C.通过I、IV对比,说明NH3与H+的结合能力小于与Ag+的结合能力 |
| D.络合平衡与难溶电解质的溶解平衡都是化学平衡的一种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验现象预测正确的是( )
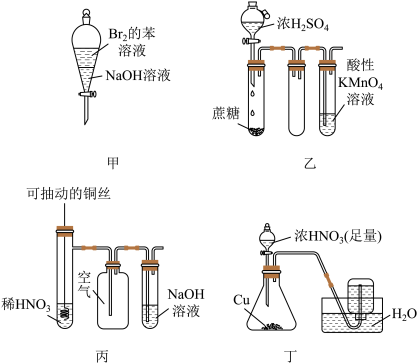

| A.实验甲:振荡后静置,上层溶液颜色保持不变 |
| B.实验乙:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验丙:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
D.实验丁:反应最终,集气瓶中有 为无色气体, 为无色气体, 为无色液体 为无色液体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验方案不能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 向1mL0.1mol·L-1MgCl2溶液中滴加1-2滴0.1mol·L-1NaOH溶液,再滴加2滴0.1mol·L-1FeCl3溶液,观察沉淀颜色的变化 | 比较Ksp[Mg(OH)2]、Ksp[Fe(OH)3]大小 |
| B | 室温下,用pH试纸测0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,比较溶液pH大小 | 比较CH3COOH、HClO酸性强弱 |
| C | 在HCl气流中加热蒸干FeCl3溶液 | 制备无水FeCl3晶体 |
| D | 向1mL0.1mol·L-1 FeCl3溶液中滴加2mL0.1mol·L-1KI溶液,充分反应,滴加几滴KSCN溶液后变成红色 | 验证FeCl3与KI的反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次






 的
的 溶液,再滴加5滴
溶液,再滴加5滴 溶液。比较
溶液。比较 与
与 溶解度的大小
溶解度的大小 :
: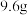 ;
;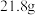 。室温下,比较
。室温下,比较


