实验I:定性探究影响化学反应速率的外界因素
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2 2H2O+O2↑
2H2O+O2↑
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2
 2H2O+O2↑
2H2O+O2↑| 影响因素 | 实验步骤 | 实验现象 | 实验结论 |
| 浓度 | 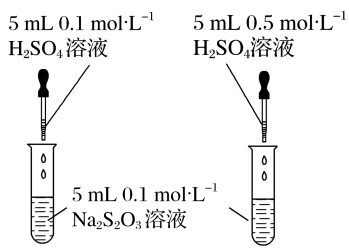 | 均出现 | 增大浓度,化学反应速率 |
| 温度 | 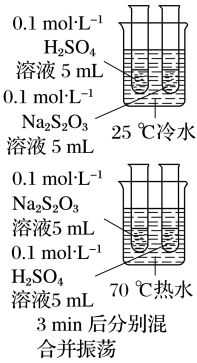 | 混合后均出现 | 升高温度,化学反应速率 |
| 催化剂 | 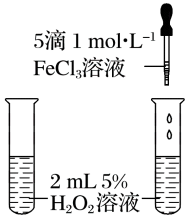 | 前者 | 催化剂能 |
2023高二上·全国·专题练习 查看更多[2]
(已下线)【知识图鉴】单元讲练测选择性必修1第2单元01讲核心(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
更新时间:2023-07-06 20:23:28
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】反应A (g)+B (s) C(g); ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“ 减慢”或“不变”)。
C(g); ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“ 减慢”或“不变”)。
(1)升温____________ ;
(2)加正催化剂______________ ;
(3)增大容器容积___________ ;
(4)加入C_________________ 。
 C(g); ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“ 减慢”或“不变”)。
C(g); ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“ 减慢”或“不变”)。(1)升温
(2)加正催化剂
(3)增大容器容积
(4)加入C
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在密闭容器中进行如下反应: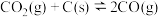
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
(1)增加 的量,则平衡
的量,则平衡___________ (填“逆移”“正移”或“不移”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)恒温条件,增大反应容器的容积,则平衡___________ ,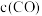
___________ (填“增大”“减小”或“不变”,下同)
(3)保持反应容器的容积和温度不变,通入He气,则平衡___________ ,
___________ 。
(4)保持反应容器的压强不变,通入Ar气,则平衡___________ ,
___________ 。
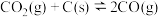
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。(1)增加
 的量,则平衡
的量,则平衡
(2)恒温条件,增大反应容器的容积,则平衡
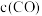
(3)保持反应容器的容积和温度不变,通入He气,则平衡

(4)保持反应容器的压强不变,通入Ar气,则平衡

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:
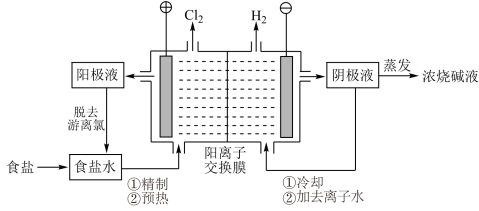
(1)电解饱和食盐水的化学方程式为__________ 。
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是__________ (填字母序号)。
a. b.
b.
c.热空气吹出 d.降低阳极区液面上方的气压
Ⅱ.食盐水中的 若进入电解槽,可被电解产生的
若进入电解槽,可被电解产生的 氧化为,并进一步转化为
氧化为,并进一步转化为 。
。 可继续被氧化为高碘酸根
可继续被氧化为高碘酸根 ,与
,与 结合生成溶解度较小的
结合生成溶解度较小的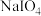 沉积于阳离子交换膜上,影响膜的寿命。
沉积于阳离子交换膜上,影响膜的寿命。
(3)从元素性质角度解释 中碘元素的为
中碘元素的为 价的原因:
价的原因:__________ 。
(4) 被氧化为
被氧化为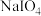 的化学方程式为
的化学方程式为__________ 。
Ⅲ.在酸性条件下加入稍过量的 溶液,可将食盐水中的
溶液,可将食盐水中的 转化为
转化为 ,再进一步除去。通过测定体系的吸光度,可以检测不同pH下
,再进一步除去。通过测定体系的吸光度,可以检测不同pH下 的生成量随时间的变化,如下图所示。
的生成量随时间的变化,如下图所示。

已知:吸光度越高表明该体系中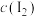 越大。
越大。
(5)结合化学用语解释 时,不同pH体系吸光度不同的原因:
时,不同pH体系吸光度不同的原因:__________ 。
(6) 时,体系的吸光度很快达到最大值,之后快速下降,且溶液中仍有
时,体系的吸光度很快达到最大值,之后快速下降,且溶液中仍有 未完全反应。吸光度快速下降的可能原因:
未完全反应。吸光度快速下降的可能原因:__________ 。
(7)一种测定溶液中 浓度的方法为:取V mL溶液,将溶液中
浓度的方法为:取V mL溶液,将溶液中 等杂质离子除去后,加入
等杂质离子除去后,加入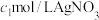 溶液
溶液 ,充分反应后,过量的
,充分反应后,过量的 用
用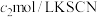 标准溶液滴定,消耗标准溶液
标准溶液滴定,消耗标准溶液 ,溶液中
,溶液中 浓度为
浓度为__________  。
。

(1)电解饱和食盐水的化学方程式为
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是
a.
 b.
b.
c.热空气吹出 d.降低阳极区液面上方的气压
Ⅱ.食盐水中的
 若进入电解槽,可被电解产生的
若进入电解槽,可被电解产生的 氧化为,并进一步转化为
氧化为,并进一步转化为 。
。 可继续被氧化为高碘酸根
可继续被氧化为高碘酸根 ,与
,与 结合生成溶解度较小的
结合生成溶解度较小的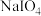 沉积于阳离子交换膜上,影响膜的寿命。
沉积于阳离子交换膜上,影响膜的寿命。(3)从元素性质角度解释
 中碘元素的为
中碘元素的为 价的原因:
价的原因:(4)
 被氧化为
被氧化为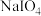 的化学方程式为
的化学方程式为Ⅲ.在酸性条件下加入稍过量的
 溶液,可将食盐水中的
溶液,可将食盐水中的 转化为
转化为 ,再进一步除去。通过测定体系的吸光度,可以检测不同pH下
,再进一步除去。通过测定体系的吸光度,可以检测不同pH下 的生成量随时间的变化,如下图所示。
的生成量随时间的变化,如下图所示。
已知:吸光度越高表明该体系中
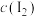 越大。
越大。(5)结合化学用语解释
 时,不同pH体系吸光度不同的原因:
时,不同pH体系吸光度不同的原因:(6)
 时,体系的吸光度很快达到最大值,之后快速下降,且溶液中仍有
时,体系的吸光度很快达到最大值,之后快速下降,且溶液中仍有 未完全反应。吸光度快速下降的可能原因:
未完全反应。吸光度快速下降的可能原因:(7)一种测定溶液中
 浓度的方法为:取V mL溶液,将溶液中
浓度的方法为:取V mL溶液,将溶液中 等杂质离子除去后,加入
等杂质离子除去后,加入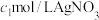 溶液
溶液 ,充分反应后,过量的
,充分反应后,过量的 用
用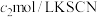 标准溶液滴定,消耗标准溶液
标准溶液滴定,消耗标准溶液 ,溶液中
,溶液中 浓度为
浓度为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在下列事实中,各是什么因素影响了化学反应速率?
(1)集气瓶中氢气和氯气的混合气体,在瓶外点燃镁条时,混合气体爆炸。________________
(2)熔化的KClO3放出气泡速率很慢,撒入少量MnO2很快产生气体。___________
(3)同浓度同体积的盐酸放入同样大小的镁条和铝条,产生气体有快有慢。___________________
(4)夏天食品易变质,而冬天不易发生该现象。___________________
(5)同样大小的石灰石分别在1mol•L-1盐酸和0.1mol•L-1盐酸中反应快慢不同。________________
(1)集气瓶中氢气和氯气的混合气体,在瓶外点燃镁条时,混合气体爆炸。
(2)熔化的KClO3放出气泡速率很慢,撒入少量MnO2很快产生气体。
(3)同浓度同体积的盐酸放入同样大小的镁条和铝条,产生气体有快有慢。
(4)夏天食品易变质,而冬天不易发生该现象。
(5)同样大小的石灰石分别在1mol•L-1盐酸和0.1mol•L-1盐酸中反应快慢不同。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硫酸是当今世界上最重要的化工产品之一,广泛应用于工业各个方面。硫酸的生产工艺几经改进,目前工业上主要采用接触法制备硫酸。接触室中发生如下反应:2SO2+O2 2SO3。
2SO3。
(1)上述生成SO3的反应属于_______
(2)该反应也是放热反应,下列说法不正确的是_______
(3)下列关于该反应的说法中,正确的是_______
 2SO3。
2SO3。(1)上述生成SO3的反应属于_______
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
| A.形成SO3中的硫氧键放出能量 |
| B.断开SO2中的硫氧键放出能量 |
| C.反应物的总能量大于生成物的总能量 |
| D.放热反应的逆反应一定是吸热反应 |
| A.增大接触室内炉气的压强对化学反应速率无影响 |
| B.升高温度能加快反应速率 |
| C.添加催化剂对反应速率无影响 |
| D.增大O2的浓度能使SO2完全转化 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: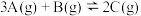 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。
(1)用 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
_______ 。
(2)在 末,
末, 的浓度为
的浓度为_______ 。
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率_______ ;
②充入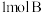 ,化学反应速率
,化学反应速率_______ ;
③将容器的体积变为 ,化学反应速率
,化学反应速率_______ 。
 密闭容器中发生反应:
密闭容器中发生反应: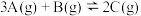 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。(1)用
 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
(2)在
 末,
末, 的浓度为
的浓度为(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率
②充入
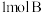 ,化学反应速率
,化学反应速率③将容器的体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,已知生物脱H2S的原理:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
请回答下列问题:
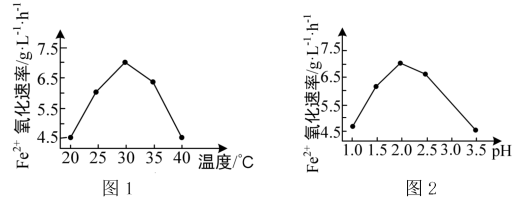
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是___ 。
(2)由图1和图2判断使用硫杆菌的最佳条件为___ 。若反应温度过高,反应速率下降,其原因是____ 。
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O请回答下列问题:
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是
(2)由图1和图2判断使用硫杆菌的最佳条件为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
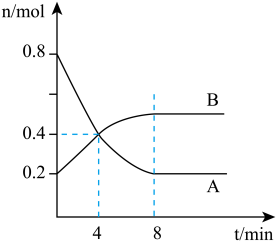
(1)该反应的化学方程式为________________ ;
(2)前4分钟,A的速率为__________________ ,平衡时A的转化率是_________
(3)第4min时,正、逆反应速率的大小关系为:v(正)__ v(逆);(填“>”、“<”或“=”)
(4)以下措施能加快反应速率的是___________ 。
A恒温恒容充入He使压强增大B缩小体积,使压强增大
C恒温恒压充入He D平衡后加入催化剂
(5)下列叙述能说明该反应已达到化学平衡状态的是________ 。
A容器内压强不再发生变化
B A的体积分数不再发生变化
C容器内气体原子总数不再发生变化
D相同时间内消耗2n molA的同时生成n mol B

(1)该反应的化学方程式为
(2)前4分钟,A的速率为
(3)第4min时,正、逆反应速率的大小关系为:v(正)
(4)以下措施能加快反应速率的是
A恒温恒容充入He使压强增大B缩小体积,使压强增大
C恒温恒压充入He D平衡后加入催化剂
(5)下列叙述能说明该反应已达到化学平衡状态的是
A容器内压强不再发生变化
B A的体积分数不再发生变化
C容器内气体原子总数不再发生变化
D相同时间内消耗2n molA的同时生成n mol B
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化学反应是有历程的。研究反应机理对于认识反应和调控反应意义重大。
I:NO和H2可以反应生成N2和水蒸气,该反应的历程包含下列两步:
① (慢)
(慢) 
②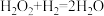 (快)
(快) 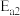
(1)该反应速率由___________ (填①或②)决定。
(2)活化能
___________ 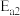 (填“>或<或=”)。
(填“>或<或=”)。
II:催化剂参与反应过程,能加快反应速率。
(3) 的速率很慢,NO和
的速率很慢,NO和 都可以作为该反应的催化剂,发生两步基元反应,快速生成
都可以作为该反应的催化剂,发生两步基元反应,快速生成 。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式
。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式___________ 、___________ 。
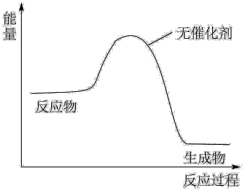
(4)请在下图中画出加入催化剂时的能量变化过程(在图上画出)(已知该两步反应均为放热反应)______ 。
I:NO和H2可以反应生成N2和水蒸气,该反应的历程包含下列两步:
①
 (慢)
(慢) 
②
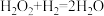 (快)
(快) 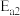
(1)该反应速率由
(2)活化能

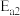 (填“>或<或=”)。
(填“>或<或=”)。II:催化剂参与反应过程,能加快反应速率。
(3)
 的速率很慢,NO和
的速率很慢,NO和 都可以作为该反应的催化剂,发生两步基元反应,快速生成
都可以作为该反应的催化剂,发生两步基元反应,快速生成 。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式
。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式(4)请在下图中画出加入催化剂时的能量变化过程(在图上画出)(已知该两步反应均为放热反应)

您最近一年使用:0次



