在下列事实中,各是什么因素影响了化学反应速率?
(1)集气瓶中氢气和氯气的混合气体,在瓶外点燃镁条时,混合气体爆炸。________________
(2)熔化的KClO3放出气泡速率很慢,撒入少量MnO2很快产生气体。___________
(3)同浓度同体积的盐酸放入同样大小的镁条和铝条,产生气体有快有慢。___________________
(4)夏天食品易变质,而冬天不易发生该现象。___________________
(5)同样大小的石灰石分别在1mol•L-1盐酸和0.1mol•L-1盐酸中反应快慢不同。________________
(1)集气瓶中氢气和氯气的混合气体,在瓶外点燃镁条时,混合气体爆炸。
(2)熔化的KClO3放出气泡速率很慢,撒入少量MnO2很快产生气体。
(3)同浓度同体积的盐酸放入同样大小的镁条和铝条,产生气体有快有慢。
(4)夏天食品易变质,而冬天不易发生该现象。
(5)同样大小的石灰石分别在1mol•L-1盐酸和0.1mol•L-1盐酸中反应快慢不同。
更新时间:2019-06-01 10:27:43
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】活化能:活化分子具有的平均能量与反应物分子具有的___________ 。
您最近一年使用:0次
【推荐2】CO2和CH4催化重整可制备合成气,对减缓燃料危机具有重要的意义,其反应历程示意图如图所示:

(1)该过程用化学反应方程式表示为___ ,反应的△H__ 0(填“<”“>”或“=”)。
(2)从起始到过渡态断裂的化学键有___ ,该过程__ (填“放出”或“吸收”)能量。

(1)该过程用化学反应方程式表示为
(2)从起始到过渡态断裂的化学键有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】实验I:定性探究影响化学反应速率的外界因素
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2 2H2O+O2↑
2H2O+O2↑
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2
 2H2O+O2↑
2H2O+O2↑| 影响因素 | 实验步骤 | 实验现象 | 实验结论 |
| 浓度 | 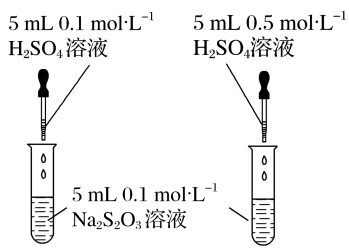 | 均出现 | 增大浓度,化学反应速率 |
| 温度 | 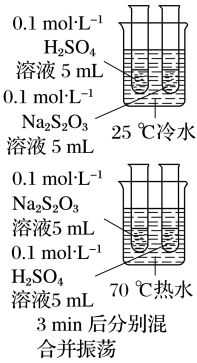 | 混合后均出现 | 升高温度,化学反应速率 |
| 催化剂 | 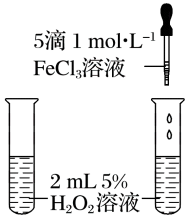 | 前者 | 催化剂能 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50 mL密度为 1.1 g/cm3的双氧水溶液中, 通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示。请依图回答下列问题:
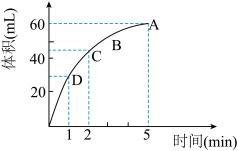
(1)放出一半气体所需要的时间为_____________ ;
(2)A、B、C、D各点反应速率快慢的顺序是______ 。
(3)在5min后,收集到的气体体积不再增加,原因是___________
(4)过氧化氢溶液的初始物质的量浓度为__________

(1)放出一半气体所需要的时间为
(2)A、B、C、D各点反应速率快慢的顺序是
(3)在5min后,收集到的气体体积不再增加,原因是
(4)过氧化氢溶液的初始物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】取10 mL 0.1 mol/L Na2S2O3溶液与10 mL 0.1 mol/L H2SO4溶液的混合溶液,分别置于冷水和热水中,请填写下列空白。
| 实验装置 | 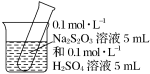 | 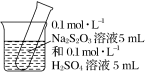 |
| 实验条件 | 冷水 | 热水 |
| 出现黄色浑浊的时间 | ||
| 实验结论 | ||
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定条件下,在2L的密闭容器中,A、B两种气体的物质的量随时间变化的曲线如图所示。回答下列问题:
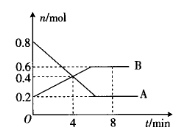
(1)该反应的化学方程式为_______ 。
(2)0~4min内,用B表示的化学反应速率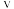 (B)=
(B)=_______ 。
(3)第4min时,正、逆反应速率的大小关系为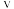 (正)
(正)_______ (填“>”、“<”或“=”) 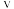 (逆)。
(逆)。
(4)下列措施能加快反应速率的是_______ (填字母)。
A.升高温度 B.恒温恒压下充入He C.使用催化剂
(5)有2molB生成时,放出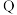 kJ的热量,则该反应达到图中平衡时放出的热量为
kJ的热量,则该反应达到图中平衡时放出的热量为_______ 。
①等于0.2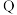 kJ ②小于0.2
kJ ②小于0.2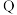 kJ ③大于0.2
kJ ③大于0.2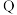 kJ
kJ

(1)该反应的化学方程式为
(2)0~4min内,用B表示的化学反应速率
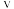 (B)=
(B)=(3)第4min时,正、逆反应速率的大小关系为
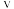 (正)
(正)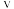 (逆)。
(逆)。(4)下列措施能加快反应速率的是
A.升高温度 B.恒温恒压下充入He C.使用催化剂
(5)有2molB生成时,放出
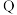 kJ的热量,则该反应达到图中平衡时放出的热量为
kJ的热量,则该反应达到图中平衡时放出的热量为①等于0.2
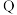 kJ ②小于0.2
kJ ②小于0.2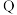 kJ ③大于0.2
kJ ③大于0.2 kJ
kJ
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在微电子工业中, 作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成
作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成 化学键时需要吸收或放出的能量。请回答下列问题:
化学键时需要吸收或放出的能量。请回答下列问题:
(1)几种化学键的键能如表,则 、
、 和
和 三种气体中,稳定性最强的物质为
三种气体中,稳定性最强的物质为_______ (填化学式),判断的依据为_______ ;反应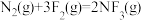 生成
生成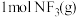 时,会
时,会_______ (填“吸收”或“放出”)_______ kJ能量
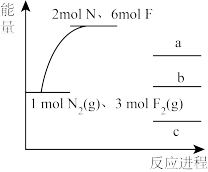
(2)根据上述数据,反应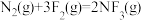 的能量变化与反应进程的关系如图,图中表示
的能量变化与反应进程的关系如图,图中表示 的能量是
的能量是_______ (填“a”、“b”或“c”);除选用合适的催化剂加快化学反应速率,还可以采取的措施为_______ 、_______ (请任写两条)
 作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成
作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成 化学键时需要吸收或放出的能量。请回答下列问题:
化学键时需要吸收或放出的能量。请回答下列问题:| 化学键 |  | F−F | N−F |
键能/ | 941.7 | 154.8 | 283.0 |
 、
、 和
和 三种气体中,稳定性最强的物质为
三种气体中,稳定性最强的物质为 生成
生成 时,会
时,会(2)根据上述数据,反应
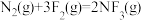 的能量变化与反应进程的关系如图,图中表示
的能量变化与反应进程的关系如图,图中表示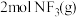 的能量是
的能量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】研究 、
、 、CO等大气污染气体的处理有重要意义。如图为
、CO等大气污染气体的处理有重要意义。如图为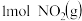 和
和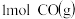 反应生成
反应生成 和
和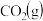 过程中的能量变化示意图。已知
过程中的能量变化示意图。已知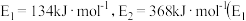 、
、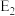 为反应的活化能
为反应的活化能 。
。
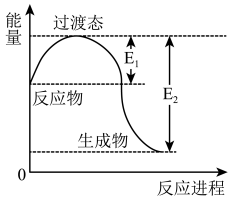
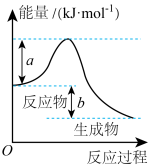
(1)则该反应放出的热量为_______ kJ。
(2)若在反应体系中加入催化剂,正反应速率_______ ,逆反应速率_______ ;E1_______ , E2_______ ; 
_______  以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。
。
(3)该条件下若 和
和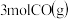 在密闭容器中充分反应后,放热140.4 kJ,则
在密闭容器中充分反应后,放热140.4 kJ,则 的转化率为
的转化率为_______ 。
 、
、 、CO等大气污染气体的处理有重要意义。如图为
、CO等大气污染气体的处理有重要意义。如图为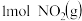 和
和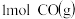 反应生成
反应生成 和
和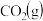 过程中的能量变化示意图。已知
过程中的能量变化示意图。已知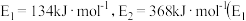 、
、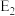 为反应的活化能
为反应的活化能 。
。
(1)则该反应放出的热量为
(2)若在反应体系中加入催化剂,正反应速率

 以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。
。(3)该条件下若
 和
和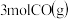 在密闭容器中充分反应后,放热140.4 kJ,则
在密闭容器中充分反应后,放热140.4 kJ,则 的转化率为
的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在密闭容器里,通入xmolH2(g)和ymolI2(g),改变下列条件,反应速率将如何变化?(填“增大、减小、或无影响”)
(1)若升高温度,速率______ ;
(2)若加入催化剂,速率______ ;
(3)若充入更多的H2,速率______ ;
(1)若升高温度,速率
(2)若加入催化剂,速率
(3)若充入更多的H2,速率
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某化学反应2A B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
根据上述数据,回答下列问题。
(1)在实验1、2中,有一个实验使用了催化剂。请利用表中数据判断哪个实验使用了催化剂,并说明理由____ 。
(2)根据表中数据可知,实验3一定达到化学平衡状态的时间是____ 。
A.10min后 B.20min后 C.30min后
 B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
(1)在实验1、2中,有一个实验使用了催化剂。请利用表中数据判断哪个实验使用了催化剂,并说明理由
(2)根据表中数据可知,实验3一定达到化学平衡状态的时间是
A.10min后 B.20min后 C.30min后
您最近一年使用:0次


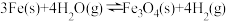 ,在一密闭容器中达到平衡,改变下列条件,判断其正反应速率变化情况。
,在一密闭容器中达到平衡,改变下列条件,判断其正反应速率变化情况。 的量,其正反应速率
的量,其正反应速率

