某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
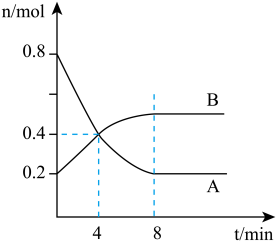
(1)该反应的化学方程式为________________ ;
(2)前4分钟,A的速率为__________________ ,平衡时A的转化率是_________
(3)第4min时,正、逆反应速率的大小关系为:v(正)__ v(逆);(填“>”、“<”或“=”)
(4)以下措施能加快反应速率的是___________ 。
A恒温恒容充入He使压强增大B缩小体积,使压强增大
C恒温恒压充入He D平衡后加入催化剂
(5)下列叙述能说明该反应已达到化学平衡状态的是________ 。
A容器内压强不再发生变化
B A的体积分数不再发生变化
C容器内气体原子总数不再发生变化
D相同时间内消耗2n molA的同时生成n mol B

(1)该反应的化学方程式为
(2)前4分钟,A的速率为
(3)第4min时,正、逆反应速率的大小关系为:v(正)
(4)以下措施能加快反应速率的是
A恒温恒容充入He使压强增大B缩小体积,使压强增大
C恒温恒压充入He D平衡后加入催化剂
(5)下列叙述能说明该反应已达到化学平衡状态的是
A容器内压强不再发生变化
B A的体积分数不再发生变化
C容器内气体原子总数不再发生变化
D相同时间内消耗2n molA的同时生成n mol B
更新时间:2019-06-17 08:22:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】如图表示800℃时,一个反应体系内A、B、C三种气体物质的浓度随时间变化的情况,t是反应时间。请回答:

(1)该反应的反应物是_______ 。
(2)该反应的化学方程式为_______ 。
(3)达到平衡状态的所需时间是2min,则该2min内A物质的平均反应速率为_______ 。

(1)该反应的反应物是
(2)该反应的化学方程式为
(3)达到平衡状态的所需时间是2min,则该2min内A物质的平均反应速率为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】A与B反应生成C,假定反应由A、B开始,它们的初始浓度均为1.0mol·L-1。反应进行2min后A的浓度为0.8 mol·L-1,B的浓度为0.6 mol·L-1,C的浓度为0.6 mol·L-1。
⑴2min内的平均速率为V(A)=_________ ,V(B)=________ ,V(C)=________ ;
⑵V(A):V(B):V(C)=___________________ ;
⑶该反应的化学方程式为:_______________________________________ 。
⑴2min内的平均速率为V(A)=
⑵V(A):V(B):V(C)=
⑶该反应的化学方程式为:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
(1)增加Fe的量,其正反应速率_________ (填“增大”“不变”或“减小”,下同),平衡________ 移动(填“不”“向正反应方向”或“向逆反应方向”,下同)。
(2)将容器的体积缩小一半,其正反应速率________ ,平衡________ 移动。
(3)保持体积不变,充入N2使体系压强增大,其正反应速率________ ,平衡____________ 移动。
(4)保持体积不变,充入水蒸气,其正反应速率________ ,平衡____________ 移动。
 Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:(1)增加Fe的量,其正反应速率
(2)将容器的体积缩小一半,其正反应速率
(3)保持体积不变,充入N2使体系压强增大,其正反应速率
(4)保持体积不变,充入水蒸气,其正反应速率
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】T℃时,向体积为1L的恒容密闭容器中通入1molH2和1molCl2,一定条件下发生反应H2(g)+Cl2(g) 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。

回答下列问题:
(1) tm时,υ正_______ υ逆(填“>”、“<”或“=”)。
(2) 0~tm内H2的平均反应速率υ(H2)=__________ 。
(3)若要增大HCl的生成速率可以采取的措施有____ 、____ 。(填写两种措施)
(4)下列说法能表明该反应已达到平衡状态的是___ (填序号)。
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向___ (填“正反应”、 “逆反应”或“不移动”)方向发生移动。
 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。
回答下列问题:
(1) tm时,υ正
(2) 0~tm内H2的平均反应速率υ(H2)=
(3)若要增大HCl的生成速率可以采取的措施有
(4)下列说法能表明该反应已达到平衡状态的是
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】研究CO2、CO的转化、应用等问题,既有利于环境保护,又有利于实现碳达峰、碳中和。中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是_____ (写两种)。

 C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】图Ⅰ、Ⅱ依次表示在酶浓度一定时,反应速率与反应物浓度、温度的关系。请据图回答下列问题:

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是___________ 。
(2)图Ⅱ中,催化效率最高的温度为___________ (填“ ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。
(3)图Ⅱ中, 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是___________ 。
(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内, 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为___________ (填“甲”或“乙”)。

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是
(2)图Ⅱ中,催化效率最高的温度为
 ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。(3)图Ⅱ中,
 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内,
 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】某实验小组探究H2O2分解的速率及影响因素,在相同温度下按照下表所示的方案完成实验。
(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是_____ 和_____ 。
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)______ 。
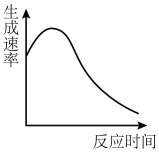
(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
①反应6min,H2O2分解了_______ %。
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=________ mol▪L-1▪min-1。
实验编号 | 反应物 |
① | 10 mL 0.5 mol ▪ L-1 H2O2溶液 |
② | 10 mL 1.0 mol ▪ L-1 H2O2溶液 |
③ | 10 mL 1.0 mol ▪ L-1 H2O2溶液+1mL H2O |
④ | 10 mL 1.0 mol ▪ L-1 H2O2溶液+1 mL 0.1 mol ▪ L-1 FeCl3溶液 |
(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)

(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
①反应6min,H2O2分解了
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
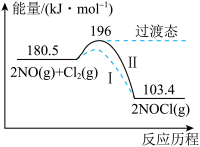
【推荐3】亚硝酰氯(NOCl)是有机合成中的重要试剂。通常条件下,NO和Cl2反应生成NOC1,其能量变化如图所示。
回答下列问题:
(1)曲线Ⅱ中正反应的活化能E1为_______________ ,逆反应的活化能E2为___________ 。 该反应能在通常情况下进行的主要原因是_____________________________ 。
(2)加入催化剂的曲线为_________________ (填“I”或“Ⅱ”)。加入催化剂,能提高化学反应速率的原因是_______________________________________________________ 。
(3)催化剂不能使平衡移动的原因是_________________________________________ 。
(4)上述合成NOCl(g)的热化学方程式为__________________________________ 。

回答下列问题:
(1)曲线Ⅱ中正反应的活化能E1为
(2)加入催化剂的曲线为
(3)催化剂不能使平衡移动的原因是
(4)上述合成NOCl(g)的热化学方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+ B(g) xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L-1·s-1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L-1·s-1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x =_________________
(2)从反应开始到10s,B的平均反应速率为______________
(3)平衡时容器中B的体积分数为___________________
(4)该温度下此反应的平衡常数表达式为_______________
(5)下列各项能表示该反应达到平衡状态是_____________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) = 2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体的物质的量不再变化
 xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L-1·s-1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L-1·s-1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:(1)x =
(2)从反应开始到10s,B的平均反应速率为
(3)平衡时容器中B的体积分数为
(4)该温度下此反应的平衡常数表达式为
(5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) = 2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体的物质的量不再变化
您最近半年使用:0次
【推荐2】恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g) xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x=____________
(2)从反应开始到10s,B的平均反应速率为____________
(3)从反应开始到40s达平衡状态,A的平均反应速率为____________
(4)平衡时容器中B的体积分数为____________
(5)下列各项能表示该反应达到平衡状态是____________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量n(A)∶n(B)=2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
 xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:(1)x=
(2)从反应开始到10s,B的平均反应速率为
(3)从反应开始到40s达平衡状态,A的平均反应速率为
(4)平衡时容器中B的体积分数为
(5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量n(A)∶n(B)=2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】铁器时代是人类发展史中一个极为重要的时代。铁的冶炼和铁器的制造经历了一个很长的时期。当人们在冶炼青铜的基础上逐渐掌握了冶炼铁的技术之后,铁器时代就到来了。回答下列问题:
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为: Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH= -28.5 kJ·mol-1
2Fe(s)+3CO2(g) ΔH= -28.5 kJ·mol-1
该反应的平衡常数表达式K=___________ ,升高温度,K值_____ (填“增大”“减小”或“不变”)。
(2)T ℃时,反应Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知
2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知 =4)
=4)
①平衡时CO 的转化率为_____ 。
②下列情况能说明上述反应达到平衡状态的是_____ (填字母)。
A.容器内气体密度保持不变 B.容器内气体压强保持不变 C.CO的消耗速率和CO2的生成速率相等
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为: Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ΔH= -28.5 kJ·mol-1
2Fe(s)+3CO2(g) ΔH= -28.5 kJ·mol-1该反应的平衡常数表达式K=
(2)T ℃时,反应Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知
2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知 =4)
=4)| 物质 | Fe2O3 | CO | Fe | CO2 |
| 起始/mol | 1.0 | 1.0 | 1.0 | 1.0 |
①平衡时CO 的转化率为
②下列情况能说明上述反应达到平衡状态的是
A.容器内气体密度保持不变 B.容器内气体压强保持不变 C.CO的消耗速率和CO2的生成速率相等
您最近半年使用:0次



