合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):
请回答下列问题:
(1)C,N,O的第一电离能由大到小的顺序为___________ 。
(2)写出基态Cu+的核外电子排布式________ 。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为________ 。
(4)写出与CO互为等电子体的离子_______ 。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子和N原子轨道的杂化类型分别为________ ;1 mol尿素分子中,σ键的数目为_________ 。

请回答下列问题:
(1)C,N,O的第一电离能由大到小的顺序为
(2)写出基态Cu+的核外电子排布式
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的离子
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子和N原子轨道的杂化类型分别为
14-15高三上·黑龙江·期末 查看更多[1]
(已下线)2014届黑龙江省哈三中高三上学期期末考试理综化学试卷
更新时间:2014-03-16 15:17:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E是原子序数依次增大 的六种短周期元素,其元素性质或原子结构如下。
(1)写出B、D的元素名称:B_______ 、D_______ 。
(2)元素F位于周期表的_______ 区,其价电子的排布式为_______ 。
(3)A、C和E三种元素的电负性由大到小的顺序:_______ (请填元素符号)
(4)已知元素A、B形成的(AB)2链状分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键之比为_______ 。
(5)烯丙醇(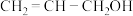 )分子中碳原子的杂化类型为
)分子中碳原子的杂化类型为_______ 。
(6)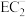 的空间构型为
的空间构型为_______ 。
(7)电解D与E形成的化合物的水溶液在工业上有着重要应用,请写出其电解的总化学方程式_______ 。
| 元素 | 元素性质或原子结构 |
| A | 原子核外有6种不同运动状态的电子 |
| B | 原子最高能级的不同轨道都有电子且自旋方向相同 |
| C | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| D | 在同周期元素中,原子半径最大、第一电离能最小 |
| E | 元素最高正价与最低负价代数和为6 |
| F | 基态原子的M层全充满,N层只有一个电子 |
(2)元素F位于周期表的
(3)A、C和E三种元素的电负性由大到小的顺序:
(4)已知元素A、B形成的(AB)2链状分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键之比为
(5)烯丙醇(
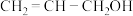 )分子中碳原子的杂化类型为
)分子中碳原子的杂化类型为(6)
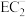 的空间构型为
的空间构型为(7)电解D与E形成的化合物的水溶液在工业上有着重要应用,请写出其电解的总化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】前四期元素A、B、C、D的原子序数依次增大,元素A核外电子有8种不同的运动状态;元素B的负一价离子的最外层电子数是次外层的4倍;元素C位于第四周期第ⅡA族;元素D最外层只有1个电子,次外层的所有原子轨道均充满电子。
(1)A原子核外有________ 种形状不同的原子轨道。
(2)与D同周期且同区的元素价层电子排布式为___________ 。
(3)上述四种元素中,第一电离能最小的是________________ (填元素符号)。
(4) AB2的立体构型为___________ ,其中A的杂化方式为______________ 。
(5)A2的熔点比DA的___________ (填“高”或“低”)。
(6) DA具有NaCl型结构,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得DA的晶胞参数为α=480pm,则r(A2-)=________ pm、r(D2+)=__________ pm。
(1)A原子核外有
(2)与D同周期且同区的元素价层电子排布式为
(3)上述四种元素中,第一电离能最小的是
(4) AB2的立体构型为
(5)A2的熔点比DA的
(6) DA具有NaCl型结构,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得DA的晶胞参数为α=480pm,则r(A2-)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大,A的质子数等于周期数,B与C的P轨道均有三个成单电子,D的最高正价与最低负价代数和为4,E的最外层只有一个电子, 内层轨道处于全充满状态。试回答下列问题。
(1)基态E原子的电子排布式为_________ ;C和D的第一电离能较大的________ (填元素符号)。
(2)DO32-中D原子的杂化类型为_________ ;A、D和氧元素组成的液态化合物A2DO4中存在的作用力有_____________ 。
(3)结构式为A—B=B—A的分子中σ键和π键的数目比为________ ;B2分子和NO+离子互为等离子体,则NO+的电子式为___________ 。
(4)向EDO4溶液中加入过量稀氨水,其化学方程式为_______________ ;产物中阳离子的配体是_____________ (填化学式)。
(5)D(黑球)和E(白球)形成某种晶体的晶胞如图所示。已知该晶体的晶胞边长为516Pm,则黑球和白球之间最近距离为________ pm(精确到0.1,已知 =1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因
=1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因__________ 。
(1)基态E原子的电子排布式为
(2)DO32-中D原子的杂化类型为
(3)结构式为A—B=B—A的分子中σ键和π键的数目比为
(4)向EDO4溶液中加入过量稀氨水,其化学方程式为
(5)D(黑球)和E(白球)形成某种晶体的晶胞如图所示。已知该晶体的晶胞边长为516Pm,则黑球和白球之间最近距离为
 =1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因
=1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因
您最近一年使用:0次
【推荐1】硫及其化合物有许多用途。请回答下列问题。
(1)基态硫离子价层电子的轨道表达式为___________ ,其电子填充的最高能级的轨道数为___________ 。
(2)常见含硫的物质有单质硫(S8)、SO2、Na2S、K2S等,四种物质的熔点由高到低的顺序依次为___________ ,原因是___________ 。
(3)方铅矿(即硫化铅)是一种比较常见的矿物,酸溶反应为:PbS+4HCl(浓)=H2[PbCl4]+H2S↑,则H2[PbCl4]中配位原子是_________ ,第一电离能I1(Cl)___________ I1(S)(填“>”、“<”或¨=”),H2S中硫的杂化方式为_______ ,下列分子空间的构型与H2S相同的有___________ 。
A.H2O B.SO3 C.O3 D.CH4
(4)方铅矿的立方晶胞如图所示,硫离子采取面心立方堆积,铅离子填在由硫离子形成的___________ 空隙中。已知晶体密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则晶胞中硫离子与铅离子最近的距离为___________ nm。

(1)基态硫离子价层电子的轨道表达式为
(2)常见含硫的物质有单质硫(S8)、SO2、Na2S、K2S等,四种物质的熔点由高到低的顺序依次为
(3)方铅矿(即硫化铅)是一种比较常见的矿物,酸溶反应为:PbS+4HCl(浓)=H2[PbCl4]+H2S↑,则H2[PbCl4]中配位原子是
A.H2O B.SO3 C.O3 D.CH4
(4)方铅矿的立方晶胞如图所示,硫离子采取面心立方堆积,铅离子填在由硫离子形成的

您最近一年使用:0次
【推荐2】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态 Cl原子核外电子排布式为__________________________ ,P、S、Cl的第一电离能由大到小顺序为____________________ ,P、S、Cl的电负性由大到小顺序为_______________ 。
(2)SCl2分子中的中心原子杂化轨道类型是_____________ ,该分子构型为__________ 。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中配位键个数为_______ ;以“—”表示σ键、“→”表示配位键,写出CO分子的结构式__________ 。
(4)已知MgO与NiO的晶体结构(如图1)相同, 其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:MgO_____ NiO(填“>”、“<”或“=”),理由是_______________________________ 。
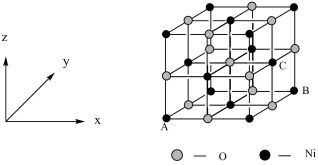
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______ 。
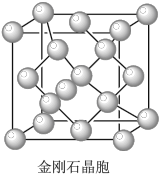
(6)金刚石晶胞含有____ 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______ a,列式表示碳原子在晶胞中的空间占有率____ (请用r和a表示不要求计算结果)。
(1)基态 Cl原子核外电子排布式为
(2)SCl2分子中的中心原子杂化轨道类型是
(3)Ni与CO能形成配合物Ni(CO)4,该分子中配位键个数为
(4)已知MgO与NiO的晶体结构(如图1)相同, 其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:MgO

(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

(6)金刚石晶胞含有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分。请回答下列问题:___________ 区。
(2)比较⑨⑩两种元素的电负性由大到小的顺序___________ ,⑥⑦两种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是___________(填序号)。
(4)④和⑤两元素比较,非金属性较弱的是④,可以验证该结论的是下列中的___________ (填序号)。
A.气态氢化物的稳定性
B.两单质在自然界的存在形式
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表④和⑤两元素)
(5)在周期表中,某些电负性相近且处于对角的元素,性质具有相似性,被称为“对角线规则”,如:元素②与元素⑦。元素②的氢氧化物能与强碱反应,写出其离子方程式为___________ 。
(6)原子序数小于36的元素甲和乙,在周期表中既处于同一周期又位于同一族,且原子序数甲比乙多2,甲的基态原子价电子排布式为___________ 。
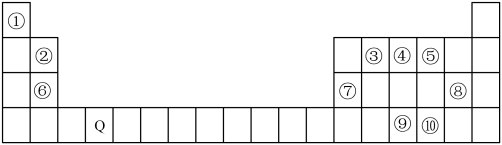
(2)比较⑨⑩两种元素的电负性由大到小的顺序
(3)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是___________(填序号)。
| A.中心原子的价层电子对数相同 |
| B.中心原子的杂化方式不同 |
| C.分子的VSEPR模型相同,空间结构也相同 |
| D.④与①形成的分子的键角比③与①形成的分子的键角更大 |
(4)④和⑤两元素比较,非金属性较弱的是④,可以验证该结论的是下列中的
A.气态氢化物的稳定性
B.两单质在自然界的存在形式
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表④和⑤两元素)
(5)在周期表中,某些电负性相近且处于对角的元素,性质具有相似性,被称为“对角线规则”,如:元素②与元素⑦。元素②的氢氧化物能与强碱反应,写出其离子方程式为
(6)原子序数小于36的元素甲和乙,在周期表中既处于同一周期又位于同一族,且原子序数甲比乙多2,甲的基态原子价电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钯(46Pd)催化剂在有机合成中有着重要的地位。请回答以下问题:
(1)钯与镍是同族元素,它们位于周期表的____ (选填s、p、d、ds、f)区。
(2)四(三苯基膦)钯(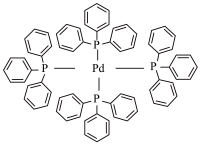 )是一种常见的钯催化剂,也是一种配合物,其配位数为
)是一种常见的钯催化剂,也是一种配合物,其配位数为_____ ,其中“三苯基膦”中磷原子与键合的三个碳原子构成的立体结构为__ 。
(3)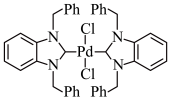 是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为____ 。配体中碳原子的杂化类型有____ ,其中氯原子的价电子轨道表达式为___ 。
(1)钯与镍是同族元素,它们位于周期表的
(2)四(三苯基膦)钯(
 )是一种常见的钯催化剂,也是一种配合物,其配位数为
)是一种常见的钯催化剂,也是一种配合物,其配位数为(3)
 是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】 发生如下转化。
发生如下转化。 是一种拟卤素,性质与卤素相似;
是一种拟卤素,性质与卤素相似; 和
和 均位于
均位于 族。请回答:
族。请回答:
(1) 和
和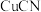 中热稳定性更好的是
中热稳定性更好的是___________ 。写出溶液A中的所有的阴离子___________ 。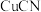 转化为
转化为 的过程中,需适当控制反应温度,反应温度不能过高,原因是
的过程中,需适当控制反应温度,反应温度不能过高,原因是___________ 。
(2)下列说法正确的是___________。
(3)设计实验检验白色沉淀C中的组成元素___________ 。写出检验白色沉淀C中的金属元素所发生的离子方程式___________ 。
 发生如下转化。
发生如下转化。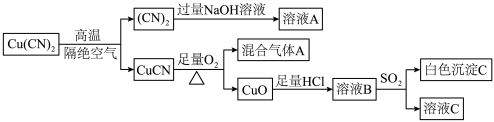
 是一种拟卤素,性质与卤素相似;
是一种拟卤素,性质与卤素相似; 和
和 均位于
均位于 族。请回答:
族。请回答:(1)
 和
和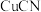 中热稳定性更好的是
中热稳定性更好的是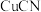 转化为
转化为 的过程中,需适当控制反应温度,反应温度不能过高,原因是
的过程中,需适当控制反应温度,反应温度不能过高,原因是(2)下列说法正确的是___________。
A. 的空间构型为直线形 的空间构型为直线形 | B.白色沉淀C可能溶于氨水 |
C. 在混合气体A中燃烧生成三种固体 在混合气体A中燃烧生成三种固体 | D.溶液B的颜色一定呈蓝色 |
(3)设计实验检验白色沉淀C中的组成元素
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、M、W是原子序数依次增大的前四周期元素,X元素有1个2p空轨道,Y为同周期离子半径最小的金属元素,Z元素原子的最外层电子数比次外层电子数少2,M原子外围电子排布式为3dn4sn,W的内层电子已全充满,最外层只有2个电子。请回答下列问题:
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是___________ ;该物质易溶于水的主要原因是_______ 。
(2)元素Z的最高价氧化物中,Z原子的杂化方式是_____ ,分子的空间构型是_____ 。
(3)某M配合物的化学式是[M(H2O)5Cl]Cl2·H2O,1 mol该配合物中含配位键的数目是______ 。
(4)元素Z与W形成的种化合物的晶胞结构如图所示,则该化合物的化学式为_______ 。
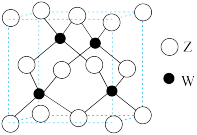
(5)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为__________ 。
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是
(2)元素Z的最高价氧化物中,Z原子的杂化方式是
(3)某M配合物的化学式是[M(H2O)5Cl]Cl2·H2O,1 mol该配合物中含配位键的数目是
(4)元素Z与W形成的种化合物的晶胞结构如图所示,则该化合物的化学式为

(5)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画《千里江山图》,《千里江山图》之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关,请回答下列问题:
(1)石青,又名蓝矿石,化学式为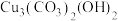 。基态
。基态 原子的价电子排布式为
原子的价电子排布式为_______ ;原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为_______ 。
(2)亚铁氰化钾,呈黄色结晶性粉末,化学式为 。
。 中配体
中配体 的配位原子是
的配位原子是_______ (填元素符号); 中
中 原子的杂化方式
原子的杂化方式_______ ;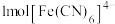 中含
中含 键为
键为_______  。
。
(3) 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。

 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是_______ , 配位数为
配位数为_______ ;已知图1中 原子的坐标参数为
原子的坐标参数为 ,则与
,则与 原子距离最近的
原子距离最近的 的坐标参数为
的坐标参数为_______ ;若晶胞边长为 ,则该晶体的密度为
,则该晶体的密度为_______  (用代数式表示,设
(用代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)石青,又名蓝矿石,化学式为
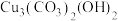 。基态
。基态 原子的价电子排布式为
原子的价电子排布式为 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)亚铁氰化钾,呈黄色结晶性粉末,化学式为
 。
。 中配体
中配体 的配位原子是
的配位原子是 中
中 原子的杂化方式
原子的杂化方式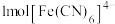 中含
中含 键为
键为 。
。(3)
 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是 配位数为
配位数为 原子的坐标参数为
原子的坐标参数为 ,则与
,则与 原子距离最近的
原子距离最近的 的坐标参数为
的坐标参数为 ,则该晶体的密度为
,则该晶体的密度为 (用代数式表示,设
(用代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。其中A与B、A与D在周期表中位置相邻,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D四种元素电负性由大到小排列顺序为_____________________ 。
(2)B的氢化物的结构式_____________ ,其空间构型为_________________________ 。
(3)E核外电子排布式是_________ ,E的某种化合物的结构如下图所示。
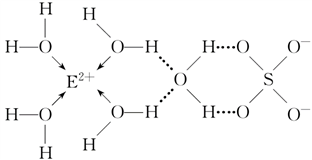
微粒间的相互作用包括化学键和分子间相互作用力,此化合物中各种粒子间的相互作用力有___________ 。
(4)A与B的气态氢化物的沸点______ 更高,A与D的气态氢化物的沸点________ 更高。
(5)A的稳定氧化物中,中心原子的杂化类型为______ ,空间构型为______ 。
(1)A、B、C、D四种元素电负性由大到小排列顺序为
(2)B的氢化物的结构式
(3)E核外电子排布式是

微粒间的相互作用包括化学键和分子间相互作用力,此化合物中各种粒子间的相互作用力有
(4)A与B的气态氢化物的沸点
(5)A的稳定氧化物中,中心原子的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】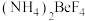 是一种可溶于水的盐,多用于制备共价化合物
是一种可溶于水的盐,多用于制备共价化合物 和金属铍。回答下列问题:
和金属铍。回答下列问题:
(1)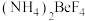 中第一电离能最大的元素,其基态原子的价电子轨道表示式为
中第一电离能最大的元素,其基态原子的价电子轨道表示式为___________ 。
(2)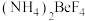 中,阳离子具有
中,阳离子具有___________ 结构,其中心原子的轨道杂化方式为___________ 。
(3)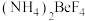 的阴离子中含有配位键,判断的依据是
的阴离子中含有配位键,判断的依据是___________ 。 晶体中含有的配位键的数目为
晶体中含有的配位键的数目为___________ 。
(4)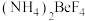 晶胞结构如图1所示,晶胞中部分原子沿z轴的投影如图2所示(分数表示原子在晶胞内的比例,全部在晶胞内就不再标示)。投影图中的○是
晶胞结构如图1所示,晶胞中部分原子沿z轴的投影如图2所示(分数表示原子在晶胞内的比例,全部在晶胞内就不再标示)。投影图中的○是___________ 原子。
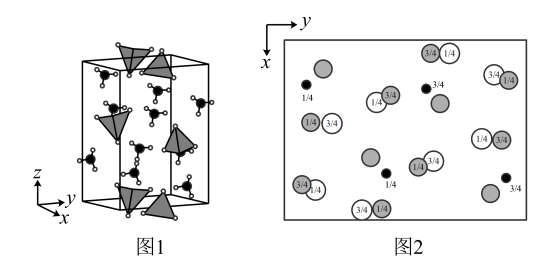
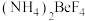 是一种可溶于水的盐,多用于制备共价化合物
是一种可溶于水的盐,多用于制备共价化合物 和金属铍。回答下列问题:
和金属铍。回答下列问题:(1)
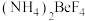 中第一电离能最大的元素,其基态原子的价电子轨道表示式为
中第一电离能最大的元素,其基态原子的价电子轨道表示式为(2)
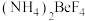 中,阳离子具有
中,阳离子具有(3)
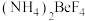 的阴离子中含有配位键,判断的依据是
的阴离子中含有配位键,判断的依据是 晶体中含有的配位键的数目为
晶体中含有的配位键的数目为(4)
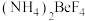 晶胞结构如图1所示,晶胞中部分原子沿z轴的投影如图2所示(分数表示原子在晶胞内的比例,全部在晶胞内就不再标示)。投影图中的○是
晶胞结构如图1所示,晶胞中部分原子沿z轴的投影如图2所示(分数表示原子在晶胞内的比例,全部在晶胞内就不再标示)。投影图中的○是
您最近一年使用:0次



