化学小组同学用铜与过量浓硝酸反应制备 气体,实验后发现溶液呈绿色,对其原因进行如下探究。
气体,实验后发现溶液呈绿色,对其原因进行如下探究。
(1)甲同学提出猜想:浓硝酸中溶解了生成的 呈黄色,黄色与蓝色叠加显绿色。
呈黄色,黄色与蓝色叠加显绿色。
实验:向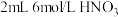 中通入稳定的
中通入稳定的 气流,溶液变黄。取该溶液与蓝色
气流,溶液变黄。取该溶液与蓝色 溶液混合,观察到溶液显绿色,验证了猜想。
溶液混合,观察到溶液显绿色,验证了猜想。
甲同学进一步探究硝酸溶液中何种粒子与 作用显黄色。
作用显黄色。
①写出铜和浓硝酸反应产生 的化学方程式
的化学方程式___________ 。
②实验1中溶液a是___________ 。
③依据上述实验推知,浓硝酸中溶液 呈黄色是溶液中
呈黄色是溶液中___________ 与 作用的结果。
作用的结果。
(2)资料:ⅰ.铜与浓硝酸反应过程中可生成 ,
, 易分解产生无色气体
易分解产生无色气体
ⅱ. 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: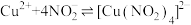 (绿色)
(绿色)
乙同学依据资料提出猜想:铜与浓硝酸反应过程中生成 ,使溶液呈绿色。
,使溶液呈绿色。
实验4: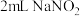 溶液与
溶液与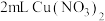 溶液混合,溶液呈绿色,加入
溶液混合,溶液呈绿色,加入 浓硝酸后,溶液变蓝。
浓硝酸后,溶液变蓝。
丙同学对加入浓硝酸后溶液变蓝的原因提出猜想并进行实验验证。
猜想1:加入浓硝酸后发生反应: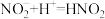 ,
, 浓度下降,绿色消失。
浓度下降,绿色消失。
猜想2:酸性条件下 分解,
分解, 浓度下降,绿色消失。
浓度下降,绿色消失。
①补全 分解的化学方程式:□
分解的化学方程式:□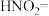 □
□ □___________+□___________
□___________+□______________________
②用离子方程式表示加入 溶液的作用
溶液的作用___________ 。
③丙同学依据实验推知猜想___________ (填“1”或“2”)成立。
(3)综合上述实验得出:过量浓硝酸与铜反应后溶液呈绿色的主要原因是___________ 。
 气体,实验后发现溶液呈绿色,对其原因进行如下探究。
气体,实验后发现溶液呈绿色,对其原因进行如下探究。(1)甲同学提出猜想:浓硝酸中溶解了生成的
 呈黄色,黄色与蓝色叠加显绿色。
呈黄色,黄色与蓝色叠加显绿色。实验:向
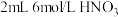 中通入稳定的
中通入稳定的 气流,溶液变黄。取该溶液与蓝色
气流,溶液变黄。取该溶液与蓝色 溶液混合,观察到溶液显绿色,验证了猜想。
溶液混合,观察到溶液显绿色,验证了猜想。甲同学进一步探究硝酸溶液中何种粒子与
 作用显黄色。
作用显黄色。| 实验装置 | 操作 | 编号 | 溶液a | 现象 |
| 向溶液a中通入稳定的 气流8s 气流8s | 实验1 | ___________ | 溶液基本无色 |
| 实验2 | 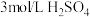 | 立即变黄 | ||
| 实验3 | 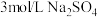 | 溶液基本无色 |
 的化学方程式
的化学方程式②实验1中溶液a是
③依据上述实验推知,浓硝酸中溶液
 呈黄色是溶液中
呈黄色是溶液中 作用的结果。
作用的结果。(2)资料:ⅰ.铜与浓硝酸反应过程中可生成
 ,
, 易分解产生无色气体
易分解产生无色气体ⅱ.
 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: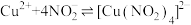 (绿色)
(绿色)乙同学依据资料提出猜想:铜与浓硝酸反应过程中生成
 ,使溶液呈绿色。
,使溶液呈绿色。实验4:
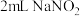 溶液与
溶液与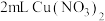 溶液混合,溶液呈绿色,加入
溶液混合,溶液呈绿色,加入 浓硝酸后,溶液变蓝。
浓硝酸后,溶液变蓝。丙同学对加入浓硝酸后溶液变蓝的原因提出猜想并进行实验验证。
猜想1:加入浓硝酸后发生反应:
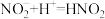 ,
, 浓度下降,绿色消失。
浓度下降,绿色消失。猜想2:酸性条件下
 分解,
分解, 浓度下降,绿色消失。
浓度下降,绿色消失。| 将实验4中蓝色溶液分成两份 | 加入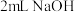 溶液,振荡 溶液,振荡 | 溶液变绿色 |
加入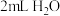 ,振荡 ,振荡 | 溶液仍为蓝色 |
 分解的化学方程式:□
分解的化学方程式:□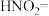 □
□ □___________+□___________
□___________+□___________②用离子方程式表示加入
 溶液的作用
溶液的作用③丙同学依据实验推知猜想
(3)综合上述实验得出:过量浓硝酸与铜反应后溶液呈绿色的主要原因是
22-23高一下·北京西城·期末 查看更多[7]
北京市西城区2022-2023学年高一下学期期末测试化学试题 北京市第五中学2023-2024学年高二上学期10月月考化学试题北京市第五中学2023-2024学年高二上学期开学考化学试卷北京市第十五中学2023-2024学年高一下学期期中考试化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)北京工业大学附属中学2023-2024学年高一下学期期中考试化学试题
更新时间:2023/07/11 16:10:26
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中。
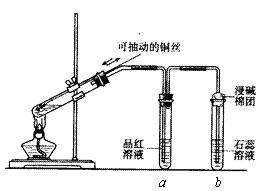
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:____________ 。
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用。
试管a中的现象____________________ ,作用是_____________________________ 。
试管b中的现象是__________________ ,作用是_____________________________ 。
(3)装置中浸碱棉团的作用是___________________________________ 。
(4)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是__________________ 。
(5)充分反应后,小组同学发现铜和硫酸都有剩余。若想使剩余的铜片继续溶解,可再加入____ (填选项的字母)。
A.HNO3 B.NaNO3 C.NaHCO3 D.Na2CO3

请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用。
试管a中的现象
试管b中的现象是
(3)装置中浸碱棉团的作用是
(4)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是
(5)充分反应后,小组同学发现铜和硫酸都有剩余。若想使剩余的铜片继续溶解,可再加入
A.HNO3 B.NaNO3 C.NaHCO3 D.Na2CO3
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某学习小组为研究铜与浓、稀HNO3反应的差异,设计了如图所示的实验装置。
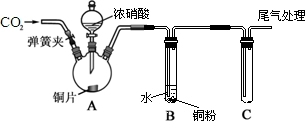
实验步骤如下:
Ⅰ.检查装置的气密性;
Ⅱ.向装置A中通入过量的CO2气体,关闭弹簧夹;
Ⅲ.滴加浓硝酸;
……
(1)步骤Ⅲ中滴加浓硝酸的具体操作是____________ 。
(2)A装置中反应的化学方程式是____________ 。
(3)B中溶液慢慢变成蓝色,能解释此现象的化学方程式是_____________ 。
(4)证明B中有NO生成的实验操作是_____________ 。
(5)步骤Ⅱ向装置A中通入过量CO2气体的目的是______________ 。
(6)上述实验结束后,观察到A装置中的溶液呈绿色,B装置中的溶液呈蓝色。在分析溶液为绿色的原因时,甲同学用加水稀释的方法,乙同学认为不合理,因在稀释时,也会引起Cu2+浓度变化。请设计实验证明绿色是由溶有NO2引起的___________ 。

实验步骤如下:
Ⅰ.检查装置的气密性;
Ⅱ.向装置A中通入过量的CO2气体,关闭弹簧夹;
Ⅲ.滴加浓硝酸;
……
(1)步骤Ⅲ中滴加浓硝酸的具体操作是
(2)A装置中反应的化学方程式是
(3)B中溶液慢慢变成蓝色,能解释此现象的化学方程式是
(4)证明B中有NO生成的实验操作是
(5)步骤Ⅱ向装置A中通入过量CO2气体的目的是
(6)上述实验结束后,观察到A装置中的溶液呈绿色,B装置中的溶液呈蓝色。在分析溶液为绿色的原因时,甲同学用加水稀释的方法,乙同学认为不合理,因在稀释时,也会引起Cu2+浓度变化。请设计实验证明绿色是由溶有NO2引起的
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空且充了氧气的注射器。
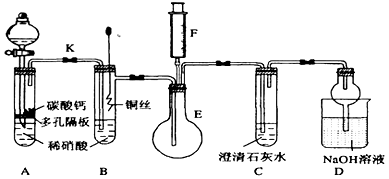
请回答有关问题:
(1)设计装置A的目的是___________________ ;为达到此目的,应如何操作?_____________ 。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是________ ; B中反应的离子方程式为:________________________ ;装置B有何优点_____________________________ 。
(3)装置E和F的作用是________________ ;为实现此作用,其操作方法是_____________________________ 。
(4)D装置中NaOH溶液的作用_____________________________ 。

请回答有关问题:
(1)设计装置A的目的是
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是
(3)装置E和F的作用是
(4)D装置中NaOH溶液的作用
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】氮化镁(Mg3N2) 在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备Mg3N2并进行有关实验。实验装置如下所示:
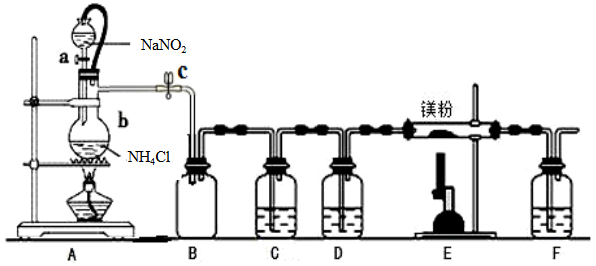
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器a、b的名称分别是____________ ,____________ ;写出装置A 中发生反应的化学方程式____________ 。
(2)装置C中为饱和硫酸亚铁溶液,作用是_________ ,该装置中发生反应的离子方程式为____________ ;装置D 中的试剂是____________ ,F 装置的作用是____________ 。
(3)加热至反应开始发生,需移走A 处酒精灯,原因是____________ 。
(4)实验结束后,取装置E的硬质玻璃管中的少量固体于试管中,加少量蒸馏水,把润湿的红色石蕊试纸放在管口,观察实验现象,该操作的目的是______________ 。反应的化学方程式为操作的目的是__________ ;再弃去上层清液,加入盐酸,观察是否有气泡产生,该操作的目的是__________ 。

已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器a、b的名称分别是
(2)装置C中为饱和硫酸亚铁溶液,作用是
(3)加热至反应开始发生,需移走A 处酒精灯,原因是
(4)实验结束后,取装置E的硬质玻璃管中的少量固体于试管中,加少量蒸馏水,把润湿的红色石蕊试纸放在管口,观察实验现象,该操作的目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】碳酸亚铁( )可用于治疗缺铁性贫血,某实验小组设计如图实验装置制备碳酸亚铁并测定其含量。
)可用于治疗缺铁性贫血,某实验小组设计如图实验装置制备碳酸亚铁并测定其含量。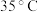 以下。
以下。
回答下列问题:
(1)仪器B的名称为___________ 。
(2)配制硫酸溶液所用的蒸馏水必须先除去溶解的氧气,操作方法是___________ 。
(3)小组某成员认为,实验装置存在明显缺陷,该缺陷可能导致产品不纯,请补充合理的改进方案___________ 。
(4)实验时,先关闭活塞 ,再打开活塞
,再打开活塞 和
和 ,加入适量稀硫酸后关闭
,加入适量稀硫酸后关闭 ,反应一段时间排出装置内的空气,接下来应进行的操作是
,反应一段时间排出装置内的空气,接下来应进行的操作是___________ 。
(5)若将 溶液换成氨水
溶液换成氨水 混合溶液,也能生成
混合溶液,也能生成 沉淀,则换成氨水—
沉淀,则换成氨水— 混合溶液后,仪器C中发生反应的离子方程式为
混合溶液后,仪器C中发生反应的离子方程式为___________ 。
(6)利用邻二氮菲(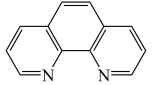 ,平面形分子,简称为phen)与
,平面形分子,简称为phen)与 完全络合生成稳定橙红色配合物
完全络合生成稳定橙红色配合物 时最大吸收波长为
时最大吸收波长为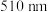 这一特征,可用来检测
这一特征,可用来检测 含量,其反应原理如下:
含量,其反应原理如下:___________ 。
②实验过程:将上述所制 全部溶解于酸中,控制溶液的
全部溶解于酸中,控制溶液的 在5~6之间,添加
在5~6之间,添加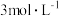 邻二氮菲溶液
邻二氮菲溶液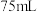 时,可获得最大吸收波长,则
时,可获得最大吸收波长,则 的质量为
的质量为___________ g。
③若添加邻二氮菲溶液前, 小于3,仍按②进行实验,则所测
小于3,仍按②进行实验,则所测 的质量将
的质量将___________ (填“偏大”“偏小”或“无影响”)。
 )可用于治疗缺铁性贫血,某实验小组设计如图实验装置制备碳酸亚铁并测定其含量。
)可用于治疗缺铁性贫血,某实验小组设计如图实验装置制备碳酸亚铁并测定其含量。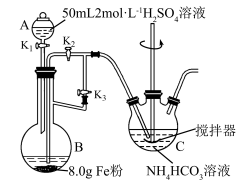
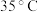 以下。
以下。回答下列问题:
(1)仪器B的名称为
(2)配制硫酸溶液所用的蒸馏水必须先除去溶解的氧气,操作方法是
(3)小组某成员认为,实验装置存在明显缺陷,该缺陷可能导致产品不纯,请补充合理的改进方案
(4)实验时,先关闭活塞
 ,再打开活塞
,再打开活塞 和
和 ,加入适量稀硫酸后关闭
,加入适量稀硫酸后关闭 ,反应一段时间排出装置内的空气,接下来应进行的操作是
,反应一段时间排出装置内的空气,接下来应进行的操作是(5)若将
 溶液换成氨水
溶液换成氨水 混合溶液,也能生成
混合溶液,也能生成 沉淀,则换成氨水—
沉淀,则换成氨水— 混合溶液后,仪器C中发生反应的离子方程式为
混合溶液后,仪器C中发生反应的离子方程式为(6)利用邻二氮菲(
 ,平面形分子,简称为phen)与
,平面形分子,简称为phen)与 完全络合生成稳定橙红色配合物
完全络合生成稳定橙红色配合物 时最大吸收波长为
时最大吸收波长为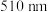 这一特征,可用来检测
这一特征,可用来检测 含量,其反应原理如下:
含量,其反应原理如下: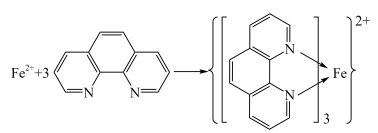
②实验过程:将上述所制
 全部溶解于酸中,控制溶液的
全部溶解于酸中,控制溶液的 在5~6之间,添加
在5~6之间,添加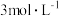 邻二氮菲溶液
邻二氮菲溶液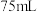 时,可获得最大吸收波长,则
时,可获得最大吸收波长,则 的质量为
的质量为③若添加邻二氮菲溶液前,
 小于3,仍按②进行实验,则所测
小于3,仍按②进行实验,则所测 的质量将
的质量将
您最近一年使用:0次
【推荐3】二氧化铈(CeO2)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有CeFCO3)为原料制备二氧化铈的一种工艺流程如图所示。
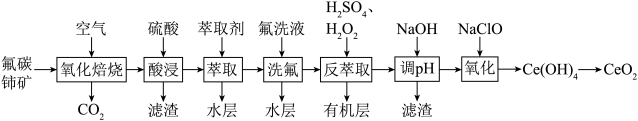
已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;
;
②Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”生成固体产物CeO2和CeF4,写出该反应的化学方程式___________ 。
(2)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP CeTBP4++F-,氟洗液中添加Al3+的作用是
CeTBP4++F-,氟洗液中添加Al3+的作用是___________ 。
(3)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为___________ 。
(4)“反萃取”后的水层溶液中c(Ce3+)=1.0mol•L-1,c(Al3+)=0.01mol•L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则加入NaOH调节溶液pH的范围是___________ ,过滤后,再向滤液中加入NaOH使Ce3+沉淀完全。
已知:①室温下,当溶液中的离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全。
②Ksp[Al(OH)3]=1.0×10-32,Ksp[Ce(OH)3]=1.0×10-21
(5)“氧化”时发生反应的离子方程式为___________ 。
(6)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得4.3吨CeO2,则CeO2的产率为___________ (保留3位有效数字,写出计算过程)。

已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF
 ;
;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”生成固体产物CeO2和CeF4,写出该反应的化学方程式
(2)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP
 CeTBP4++F-,氟洗液中添加Al3+的作用是
CeTBP4++F-,氟洗液中添加Al3+的作用是(3)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为
(4)“反萃取”后的水层溶液中c(Ce3+)=1.0mol•L-1,c(Al3+)=0.01mol•L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则加入NaOH调节溶液pH的范围是
已知:①室温下,当溶液中的离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全。
②Ksp[Al(OH)3]=1.0×10-32,Ksp[Ce(OH)3]=1.0×10-21
(5)“氧化”时发生反应的离子方程式为
(6)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得4.3吨CeO2,则CeO2的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】亚硝酰氯(NOC1)的沸点为-5.5℃,具有刺鼻恶臭味,在潮湿空气中易水解,溶于浓硫酸,是而机合成中的重要试剂。某同学用下图装置,由NO与干燥纯净的Cl2反应制备NOCl。
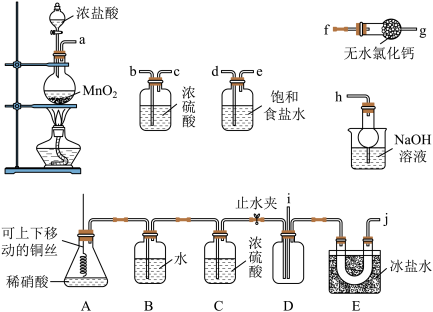
已知:①Cl2沸点为-34.6℃,NO2Cl沸点为-15℃
②2NO+Cl2= 2NOC1 2NO2+ Cl2=2NO2C1
2NO2+ Cl2=2NO2C1
回答下列问题:
(1)铜与稀硝酸反应的化学方程式为_______________ ;装置A中设计了可上下移动的铜丝,其优点是_____________________ 。
(2)上图中实验装置的连接顺序为:a→__________________ 。
(3)实验时,先制取氯气使充满除A、B、C外的整套装置,目的是______________ ;
装置中充满氯气后,下—步是制取NO,具体操作是_______________ ;
E中冰盐水的温度可低至-22℃,其作用是_______________ 。
(4)该同学的实验设计可能的不足之处是__________________ (答出一条即可)。
(5)若无C装置,则不利于NOCl的制备,主要原因是_________ (用化学方程式表示)。

已知:①Cl2沸点为-34.6℃,NO2Cl沸点为-15℃
②2NO+Cl2= 2NOC1
 2NO2+ Cl2=2NO2C1
2NO2+ Cl2=2NO2C1回答下列问题:
(1)铜与稀硝酸反应的化学方程式为
(2)上图中实验装置的连接顺序为:a→
(3)实验时,先制取氯气使充满除A、B、C外的整套装置,目的是
装置中充满氯气后,下—步是制取NO,具体操作是
E中冰盐水的温度可低至-22℃,其作用是
(4)该同学的实验设计可能的不足之处是
(5)若无C装置,则不利于NOCl的制备,主要原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】碘化钠是一种白色结晶粉末,医疗上可用于甲状腺肿瘤防治剂、祛痰剂等。实验室用NaOH、单质碘和水合肼为原料制得,部分装置如下图所示。
步骤①向三口烧瓶中加入8.2 gNaOH及30 mL水,搅拌冷却。
步骤②向制得的NaOH溶液中加入25.4 g单质碘,开动磁力搅拌器,保持60〜70℃至反应充分。
步骤③向步骤②所得溶液中加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得Nal溶液粗品和空气中常见的某气体。
步骤④向溶液③中加入1.0 g活性炭,煮沸半小时,然后将溶液与活性炭分离。
步骤⑤蒸发浓缩、结晶、过滤及干燥得产品24.3 g。
(1)步骤②温度不宜超过70℃的原因是__________ ;该步骤反应完全的现象是___________ 。
(2)步骤③N2 H4·H2O还原NaIO3的化学方程式为_______________ 。
(3)步骤④加入活性炭的目的是________ ;“将溶液与活性炭分离”的方法是__________ 。
(4)本次实验成品率为________ 。
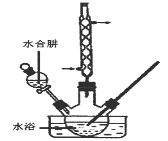
步骤①向三口烧瓶中加入8.2 gNaOH及30 mL水,搅拌冷却。
步骤②向制得的NaOH溶液中加入25.4 g单质碘,开动磁力搅拌器,保持60〜70℃至反应充分。
步骤③向步骤②所得溶液中加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得Nal溶液粗品和空气中常见的某气体。
步骤④向溶液③中加入1.0 g活性炭,煮沸半小时,然后将溶液与活性炭分离。
步骤⑤蒸发浓缩、结晶、过滤及干燥得产品24.3 g。
(1)步骤②温度不宜超过70℃的原因是
(2)步骤③N2 H4·H2O还原NaIO3的化学方程式为
(3)步骤④加入活性炭的目的是
(4)本次实验成品率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某兴趣小组以重铬酸钾( )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。
已知:在水溶液中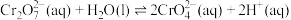
查阅资料:①含铬元素的离子在溶液中的颜色: (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);
② 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为___________ ,试剂X是___________ (填化学式)。
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是___________ ,实验⑥中发生反应的离子方程式为___________ 。
(3)结合③、④、⑦、⑧可得出结论为___________ 。
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?___________ (填“能”或“否”)。
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:
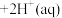 正反应的焓变
正反应的焓变
_______ 0(填“>”、“<”或“=”)。
 )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。已知:在水溶液中
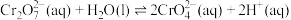
查阅资料:①含铬元素的离子在溶液中的颜色:
 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);②
 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。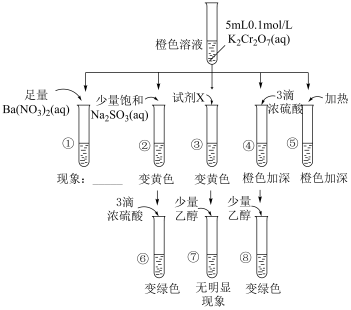
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是
(3)结合③、④、⑦、⑧可得出结论为
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:

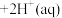 正反应的焓变
正反应的焓变
您最近一年使用:0次