钛白粉 作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含
作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含 及少量的
及少量的 )为原料生产钛白粉的工艺流程如图:
)为原料生产钛白粉的工艺流程如图:
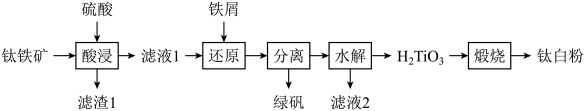
回答下列问题:
(1) 中铁的化合价是
中铁的化合价是___________ 。
(2)“酸浸”是用硫酸在温度为 下溶煮钛铁矿,“滤液1”的主要成分中含有
下溶煮钛铁矿,“滤液1”的主要成分中含有 ,则“酸浸”中主要发生的反应方程式为
,则“酸浸”中主要发生的反应方程式为___________ 。
(3)“滤渣1”的主要成分有___________ 。
(4)“还原”中加入过量铁屑的目的是___________ 。硫酸亚铁晶体的溶解度如表所示,其中绿矾 容易被氧化,则“操作Ⅱ”包括真空加热浓缩、
容易被氧化,则“操作Ⅱ”包括真空加热浓缩、___________ 、___________ 、洗涤、干燥。
(5)工业上将钛白粉与焦炭、氯气共热生成 和一种可燃气体,反应的化学方程式为
和一种可燃气体,反应的化学方程式为___________ ,最后在氯气氛围和加热的条件下用金属镁还原 制取性能优越的金属钛。
制取性能优越的金属钛。
(6)取 经煅烧至恒重后固体质量为
经煅烧至恒重后固体质量为 ,则
,则
___________ 。
 作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含
作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含 及少量的
及少量的 )为原料生产钛白粉的工艺流程如图:
)为原料生产钛白粉的工艺流程如图:
回答下列问题:
(1)
 中铁的化合价是
中铁的化合价是(2)“酸浸”是用硫酸在温度为
 下溶煮钛铁矿,“滤液1”的主要成分中含有
下溶煮钛铁矿,“滤液1”的主要成分中含有 ,则“酸浸”中主要发生的反应方程式为
,则“酸浸”中主要发生的反应方程式为(3)“滤渣1”的主要成分有
(4)“还原”中加入过量铁屑的目的是
 容易被氧化,则“操作Ⅱ”包括真空加热浓缩、
容易被氧化,则“操作Ⅱ”包括真空加热浓缩、| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27 |
| 析出晶体 |  | 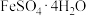 |  | |||||||
 和一种可燃气体,反应的化学方程式为
和一种可燃气体,反应的化学方程式为 制取性能优越的金属钛。
制取性能优越的金属钛。(6)取
 经煅烧至恒重后固体质量为
经煅烧至恒重后固体质量为 ,则
,则
22-23高一下·湖北恩施·期末 查看更多[2]
更新时间:2023-07-16 11:04:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是_______ 。

(2)用下列方法可制得白色的Fe(OH)2沉淀:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入_______ 。
②除去蒸馏水中溶解的O2常采用_______ 的方法。
③生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是_______ 。
(3)除去FeCl2溶液中少量的FeCl3,可加入_______ ,反应的离子方程式为_______ 。
(1)下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是

(2)用下列方法可制得白色的Fe(OH)2沉淀:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入
②除去蒸馏水中溶解的O2常采用
③生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是
(3)除去FeCl2溶液中少量的FeCl3,可加入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】FeCO3与砂糖混用可作补血剂。以黄铁矿烧渣(含CuO、Fe2O3、FeO、SiO2、Al2O3等)为主要原料制备FeCO3的流程如下:
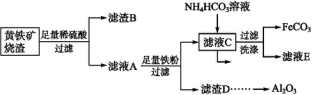
(1)质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为________ 。
(2)检验滤液A中存在Fe2+的试剂是________ 。
(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀外,还有两个作用,分别写出这两个反应的离子方程式:____________ , ________________ 。
(4)写出滤液C与NH4HCO3溶液反应的离子方程式:_____________________ 。
(5)FeCO3在空气中灼烧可制得铁系氧化物材料。已知25 ℃,101 kPa时:
4Fe(s)+3O2(g) 2Fe2O3(s) ΔH=-1 648 kJ·mol-1
2Fe2O3(s) ΔH=-1 648 kJ·mol-1
C(s)+O2(g) CO2(g) ΔH=-393 kJ·mol-1
CO2(g) ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g) 2FeCO3(s) ΔH=-1 480 kJ·mol-1
2FeCO3(s) ΔH=-1 480 kJ·mol-1
写出FeCO3在空气中灼烧生成Fe2O3的热化学方程式:________ 。
(6)某兴趣小组为充分利用副产品,欲利用滤渣D为原料制取Al2O3,请补充完成实验步骤:向滤渣D中加入适量________ 溶液,_______________________________ 。

(1)质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为
(2)检验滤液A中存在Fe2+的试剂是
(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀外,还有两个作用,分别写出这两个反应的离子方程式:
(4)写出滤液C与NH4HCO3溶液反应的离子方程式:
(5)FeCO3在空气中灼烧可制得铁系氧化物材料。已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)
 2Fe2O3(s) ΔH=-1 648 kJ·mol-1
2Fe2O3(s) ΔH=-1 648 kJ·mol-1C(s)+O2(g)
 CO2(g) ΔH=-393 kJ·mol-1
CO2(g) ΔH=-393 kJ·mol-12Fe(s)+2C(s)+3O2(g)
 2FeCO3(s) ΔH=-1 480 kJ·mol-1
2FeCO3(s) ΔH=-1 480 kJ·mol-1写出FeCO3在空气中灼烧生成Fe2O3的热化学方程式:
(6)某兴趣小组为充分利用副产品,欲利用滤渣D为原料制取Al2O3,请补充完成实验步骤:向滤渣D中加入适量
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B是中学常见的金属单质,其各物质间的转化关系如下图所示,请完成下列空白。
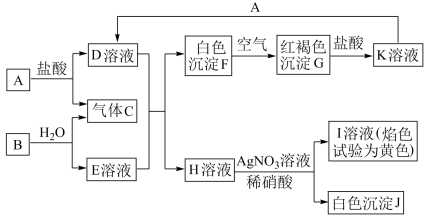
(1)写出B、C和J的化学式:B___________ ,C___________ ,J___________ 。
(2)用___________ 试剂可以检验K溶液中的阳离子。
(3)当K中混有少量D杂质时,可加入___________ 除去。
(4)写出B与水反应的离子方程式___________ 。
(5)写出F转变成G的化学方程式___________ 。
(6)写出向K溶液中加入A的离子方程式___________ 。

(1)写出B、C和J的化学式:B
(2)用
(3)当K中混有少量D杂质时,可加入
(4)写出B与水反应的离子方程式
(5)写出F转变成G的化学方程式
(6)写出向K溶液中加入A的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】用粗氧化铜(含少量Fe)制取纯净的CuCl2∙2H2O的主要过程是:

①将粗氧化铜溶解于稀盐酸中,加热、过滤。调节滤液的pH为3;
②对①所得的滤液按下列步骤进行操作:
已知:
回答下列问题:
(1)加入氧化剂X的目的的是:_____________________ 本实验最合适的氧化剂X是__________ (填字母),反应的离子方程式是_____________________ 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)Y可选:_________ ,调节pH_____________________ ,除去Fe3+的有关离子方程式为________________________
(3)采用低温减压蒸发结晶的方法得到CuCl2∙2H2O的晶体,还要在过程中不断通入______ 气体,且不能蒸干。

①将粗氧化铜溶解于稀盐酸中,加热、过滤。调节滤液的pH为3;
②对①所得的滤液按下列步骤进行操作:
已知:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
回答下列问题:
(1)加入氧化剂X的目的的是:
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)Y可选:
(3)采用低温减压蒸发结晶的方法得到CuCl2∙2H2O的晶体,还要在过程中不断通入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】莫尔盐[(NH4)2Fe(SO4)2・6H2O]是一种重要的还原剂,在空气中比一般的 亚铁盐稳定。某学习小组设计如下实验制备少量的莫尔盐并测定其纯度。

回答下列问题:
Ⅰ.制取莫尔盐
(1)连接装置,检查装置气密性。将0.1mol(NH4)2SO4晶体置于玻璃仪器中__ 填仪器 名称),将6.0g洁净铁屑加入锥形瓶中。
(2)①打开分液漏斗瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2mol·L-1稀硫酸后关闭K1。
②待大部分铁粉溶解后,打开K3、关闭K2,此时可以看到的现象为__________ ;原因是____________ 。
③关闭活塞K2、K3,采用100℃水浴蒸发B中水分,液面产生晶膜时,停止加热,冷却结晶、_______________ 、用无水乙醇洗涤晶体。该反应中硫酸需过量,保持溶液的pH在1~2之间, 其目的为_______________ 。
④装置C的作用为_____ ,装置C存在的缺点是_____ 。
Ⅱ.测定莫尔盐样品的纯度:取mg该样品配制成1L溶液,分别设计如下两个实验方案,请回答:
方案一:取20.00mL所配硫酸亚铁铵溶液用0.1000mol·L-1的酸性K2Cr2O7溶液进行滴定。重复三次。
(1)已知:Cr2O72-还原产物为Cr3+,写出此反应的离子方程式_____ 。
(2)滴定时必须选用的仪器是_____ 。

方案二:取20.00mL所配硫酸亚铁铵溶液进行如下实验。[(NH4)2Fe(SO4)2・6H2O,Mr=392,BaSO4,Mr=233]
待测液→足量的BaCl2溶液→过滤→洗涤→干燥→称量→wg固体
(3)莫尔盐晶体纯度为_____ (用含m、w的式子表示,不用算出结果)。
(4)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为_____ 。

回答下列问题:
Ⅰ.制取莫尔盐
(1)连接装置,检查装置气密性。将0.1mol(NH4)2SO4晶体置于玻璃仪器中
(2)①打开分液漏斗瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2mol·L-1稀硫酸后关闭K1。
②待大部分铁粉溶解后,打开K3、关闭K2,此时可以看到的现象为
③关闭活塞K2、K3,采用100℃水浴蒸发B中水分,液面产生晶膜时,停止加热,冷却结晶、
④装置C的作用为
Ⅱ.测定莫尔盐样品的纯度:取mg该样品配制成1L溶液,分别设计如下两个实验方案,请回答:
方案一:取20.00mL所配硫酸亚铁铵溶液用0.1000mol·L-1的酸性K2Cr2O7溶液进行滴定。重复三次。
(1)已知:Cr2O72-还原产物为Cr3+,写出此反应的离子方程式
(2)滴定时必须选用的仪器是

方案二:取20.00mL所配硫酸亚铁铵溶液进行如下实验。[(NH4)2Fe(SO4)2・6H2O,Mr=392,BaSO4,Mr=233]
待测液→足量的BaCl2溶液→过滤→洗涤→干燥→称量→wg固体
(3)莫尔盐晶体纯度为
(4)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 g/L。

请回答下列问题:
(1)写出D的名称_______ ,F的化学式_______
(2)写出反应②的离子方程式:_______ 。
(3)反应③,F在A中点燃的反应现象为:_______ 。
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:_______ 。
2 +3
+3 +10NaOH=2Na2FeO4+9
+10NaOH=2Na2FeO4+9 +5H2O
+5H2O
(5)写出反应⑤的化学方程式:_______ 。
(6)向0.02 mol B的氧化物中加入45 mL4 mol/L硫酸溶液恰好完全反应,得到B的两种不同价态的盐,所得溶液中B2+能恰好被标准状况下672 mL氯气氧化。则此B的氧化物的化学式为_______ 。

请回答下列问题:
(1)写出D的名称
(2)写出反应②的离子方程式:
(3)反应③,F在A中点燃的反应现象为:
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:
2
 +3
+3 +10NaOH=2Na2FeO4+9
+10NaOH=2Na2FeO4+9 +5H2O
+5H2O(5)写出反应⑤的化学方程式:
(6)向0.02 mol B的氧化物中加入45 mL4 mol/L硫酸溶液恰好完全反应,得到B的两种不同价态的盐,所得溶液中B2+能恰好被标准状况下672 mL氯气氧化。则此B的氧化物的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】焦亚硫酸钠( )常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的
)常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的 ,制备焦亚硫酸钠,流程如下:
,制备焦亚硫酸钠,流程如下:
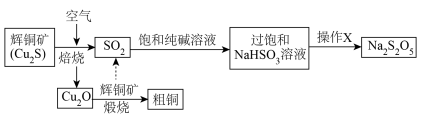
回答下列问题:
(1)焙烧、煅烧之前,辉铜矿要粉碎过筛,其目的是________ 。
(2)“煅烧”中发生反应的化学方程式为________ ,其中 ,还原产物和氧化产物的物质的量之比为________ 。
(3) 转化成
转化成 的离子方程式为
的离子方程式为________ 。
(4)操作X包括蒸发浓缩、________ 、过滤、洗涤、干燥。
(5)探究 的性质。取少量
的性质。取少量 产品溶于水,滴加酸性
产品溶于水,滴加酸性 溶液,振荡,溶液褪色,表明
溶液,振荡,溶液褪色,表明 具有的性质有________(填字母)。
具有的性质有________(填字母)。
(6)为了探究 溶液在空气中的变化情况,小组展开如下研究:
溶液在空气中的变化情况,小组展开如下研究:
查阅资料:常温下, 溶液
溶液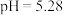 ,
,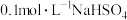 溶液
溶液 ,
, 溶液
溶液 。常温下,取
。常温下,取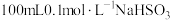 溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
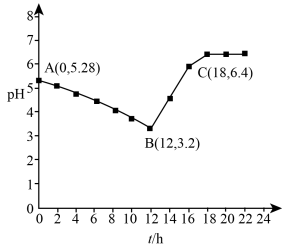
AB段pH降低的主要原因是________ 。B点pH不能降至1.0的主要原因可能是________ (用离子方程式表示)。
 )常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的
)常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的 ,制备焦亚硫酸钠,流程如下:
,制备焦亚硫酸钠,流程如下:
回答下列问题:
(1)焙烧、煅烧之前,辉铜矿要粉碎过筛,其目的是
(2)“煅烧”中发生反应的化学方程式为
(3)
 转化成
转化成 的离子方程式为
的离子方程式为(4)操作X包括蒸发浓缩、
(5)探究
 的性质。取少量
的性质。取少量 产品溶于水,滴加酸性
产品溶于水,滴加酸性 溶液,振荡,溶液褪色,表明
溶液,振荡,溶液褪色,表明 具有的性质有________(填字母)。
具有的性质有________(填字母)。| A.氧化性 | B.还原性 | C.不稳定性 | D.碱性 |
 溶液在空气中的变化情况,小组展开如下研究:
溶液在空气中的变化情况,小组展开如下研究:查阅资料:常温下,
 溶液
溶液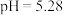 ,
,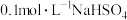 溶液
溶液 ,
, 溶液
溶液 。常温下,取
。常温下,取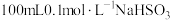 溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
AB段pH降低的主要原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】四氯化锡是重要的化工中间体和催化剂。常温下。四氯化锡为无色液体,易溶于四氯化碳、苯等有机溶剂,极易与水反应生成锡酸(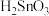 ,难溶于水、具有两性),某研究小组利用氯气与硫渣(主要成分
,难溶于水、具有两性),某研究小组利用氯气与硫渣(主要成分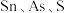 等)制备少量四氯化锡,装置如图所示。
等)制备少量四氯化锡,装置如图所示。
实验步骤:
①连接装置并检险装置气密性。
②连接 装置并加入相应试剂后,通入氮气。
装置并加入相应试剂后,通入氮气。
③控制仪器a的活塞缓慢加入浓盐酸并加热。将产生的气体缓慢通入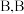 中温度维持在
中温度维持在 ,当观察到出现较多液态物质时,适当加快通入氯气并不断搅拌;当观察到B中黄绿色加深时,关闭仪器a的活塞。
,当观察到出现较多液态物质时,适当加快通入氯气并不断搅拌;当观察到B中黄绿色加深时,关闭仪器a的活塞。
回答下列问题:
(1)仪器a的名称为_____ 。仪器b中的试剂为_____ 。
(2)步骤②通入氮气的作用是_____ 。
(3)步骤③开始缓慢通入氯气,当出现较多液态物质时,可适当加快通入氯气的原因是_____ 。装置B中的温度需特维持在 ,若温度高于
,若温度高于 ,可能造成的后果是
,可能造成的后果是_____ ,应采取的措施是_____ 。
(4)四氯化锡与足量氢氧化钠溶液剧烈反应,所发生反应的化学方程式为_____ 。
(5)上述制得的四氯化锡液体中可能存在的液态杂质为_____ 。该杂质能使酸性高锰酸钾溶液褪色,生成一种对应的最高价含氧酸,该反应的离子方程式为_____
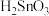 ,难溶于水、具有两性),某研究小组利用氯气与硫渣(主要成分
,难溶于水、具有两性),某研究小组利用氯气与硫渣(主要成分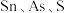 等)制备少量四氯化锡,装置如图所示。
等)制备少量四氯化锡,装置如图所示。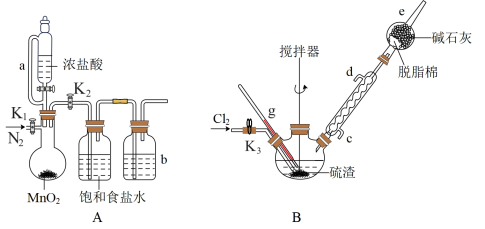
| 物质 |  |  | S |
熔点 |  |  | 112 |
沸点 | 114 | 130 | 444 |
①连接装置并检险装置气密性。
②连接
 装置并加入相应试剂后,通入氮气。
装置并加入相应试剂后,通入氮气。③控制仪器a的活塞缓慢加入浓盐酸并加热。将产生的气体缓慢通入
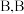 中温度维持在
中温度维持在 ,当观察到出现较多液态物质时,适当加快通入氯气并不断搅拌;当观察到B中黄绿色加深时,关闭仪器a的活塞。
,当观察到出现较多液态物质时,适当加快通入氯气并不断搅拌;当观察到B中黄绿色加深时,关闭仪器a的活塞。回答下列问题:
(1)仪器a的名称为
(2)步骤②通入氮气的作用是
(3)步骤③开始缓慢通入氯气,当出现较多液态物质时,可适当加快通入氯气的原因是
 ,若温度高于
,若温度高于 ,可能造成的后果是
,可能造成的后果是(4)四氯化锡与足量氢氧化钠溶液剧烈反应,所发生反应的化学方程式为
(5)上述制得的四氯化锡液体中可能存在的液态杂质为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景。通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示,夹持装置及搅拌装置均已略去):
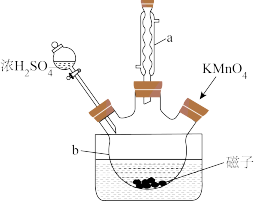
Ⅰ.将浓硫酸、NaNO3、石墨粉末在仪器b中充分混合,置于冰水中,剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶塞;
Ⅱ.转至油浴中,35 °C下搅拌1小时,缓慢滴加一定量的蒸馏水,升温至98°C并保持1小时;
Ⅲ.转移至大烧杯中,静置冷却至室温,加入大量蒸馏水,而后往烧杯中滴入H2O2至悬浊液由紫色变为土黄色;
Ⅳ.离心分离,稀盐酸洗涤沉淀;
V.蒸馏水洗涤沉淀;
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)装置图中,仪器a的作用是_______ 。
(2)步骤I中分批缓慢加入KMnO4粉末并置于冰水浴中,由此可判断该反应为_______ (填“放热反应”或“吸热反应”)。
(3)仪器b中可能发生的反应有H2SO4 (浓)+2NaNO3=Na2SO4 +2HNO3,该反应利用了H2SO4(浓)的_______ (填“ 氧化性”、“吸水性”、“脱水性”、“酸性”或“难挥发性”)。
(4)步骤III中,每消耗0.2mol氧化剂,同时消耗还原剂的物质的量为_______ mol,生成的气体体积为_______ L(标准状况下)。
(5)步骤IV中,离心分离所得的滤液中含有的溶质为_______ (填化学式)。
(6)若向步骤V的最后一次洗涤液中滴入无色酚酞,_______ (填“能”或“不能”)确定洗涤液中无H+,其理由是_______ 。

Ⅰ.将浓硫酸、NaNO3、石墨粉末在仪器b中充分混合,置于冰水中,剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶塞;
Ⅱ.转至油浴中,35 °C下搅拌1小时,缓慢滴加一定量的蒸馏水,升温至98°C并保持1小时;
Ⅲ.转移至大烧杯中,静置冷却至室温,加入大量蒸馏水,而后往烧杯中滴入H2O2至悬浊液由紫色变为土黄色;
Ⅳ.离心分离,稀盐酸洗涤沉淀;
V.蒸馏水洗涤沉淀;
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)装置图中,仪器a的作用是
(2)步骤I中分批缓慢加入KMnO4粉末并置于冰水浴中,由此可判断该反应为
(3)仪器b中可能发生的反应有H2SO4 (浓)+2NaNO3=Na2SO4 +2HNO3,该反应利用了H2SO4(浓)的
(4)步骤III中,每消耗0.2mol氧化剂,同时消耗还原剂的物质的量为
(5)步骤IV中,离心分离所得的滤液中含有的溶质为
(6)若向步骤V的最后一次洗涤液中滴入无色酚酞,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】纳米 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。
(1)用 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
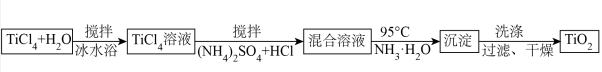
已知: 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:
第Ⅰ步(水解):
第Ⅱ步(电离):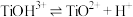
第Ⅲ步(水解):
①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是_______ 。
②流程中加入硫酸铵的目的是_______ 。
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸( )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为_______ 。
(2)测定产品中 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
①金属铝还原 的离子方程式为
的离子方程式为_______ 。
②滴定时所用的指示剂为_______ (填编号)。
a.酚酞溶液 b.KSCN溶液 c. 溶液 d.淀粉溶液
溶液 d.淀粉溶液
③样品中 的纯度为
的纯度为_______ 。
(3)纳米 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:_______ 。

 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。(1)用
 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
已知:
 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:第Ⅰ步(水解):

第Ⅱ步(电离):
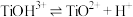
第Ⅲ步(水解):

①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是
②流程中加入硫酸铵的目的是
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸(
 )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为(2)测定产品中
 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。①金属铝还原
 的离子方程式为
的离子方程式为②滴定时所用的指示剂为
a.酚酞溶液 b.KSCN溶液 c.
 溶液 d.淀粉溶液
溶液 d.淀粉溶液③样品中
 的纯度为
的纯度为(3)纳米
 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】以钛铁矿(主要成分为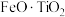 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下:
)的工艺流程如下:

回答下列问题:
“溶浸”后溶液中的主要金属阳离子包括 ,
, ,
,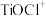 ,“滤液”经加热水解后转化为富钛渣(钛元素主要以
,“滤液”经加热水解后转化为富钛渣(钛元素主要以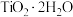 形式存在),写出上述转变的离子方程式:
形式存在),写出上述转变的离子方程式:_______ 。
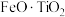 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下:
)的工艺流程如下:
回答下列问题:
“溶浸”后溶液中的主要金属阳离子包括
 ,
, ,
,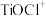 ,“滤液”经加热水解后转化为富钛渣(钛元素主要以
,“滤液”经加热水解后转化为富钛渣(钛元素主要以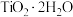 形式存在),写出上述转变的离子方程式:
形式存在),写出上述转变的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前使用最广泛的白色颜料。制备TiO2和Ti的原料是钛铁矿,用含Fe2O3的钛铁矿(主要成分为FeTiO3)制备TiO2的流程如下:

(1)步骤①加Fe的目的是_______ ;步骤②冷却的目的是_______ 。
(2)上述制备TiO2的流程中,可以利用的副产物是_______ ;考虑成本和废物的综合利用等因素,水浸后的废液中应加入_______ 处理。
(3)由金红石(TiO2)制取单质钛(Ti)的过程为 →
→

 ,其中反应TiCl4+2Mg
,其中反应TiCl4+2Mg 2MgCl2+Ti在氩气气氛中进行的理由是
2MgCl2+Ti在氩气气氛中进行的理由是_______ 。

(1)步骤①加Fe的目的是
(2)上述制备TiO2的流程中,可以利用的副产物是
(3)由金红石(TiO2)制取单质钛(Ti)的过程为
 →
→

 ,其中反应TiCl4+2Mg
,其中反应TiCl4+2Mg 2MgCl2+Ti在氩气气氛中进行的理由是
2MgCl2+Ti在氩气气氛中进行的理由是
您最近一年使用:0次



