羰基铁[Fe(CO)5]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为-20℃,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。___________ 。(填“离子晶体”或“分子晶体”)
(2)下列说法正确的是___________。
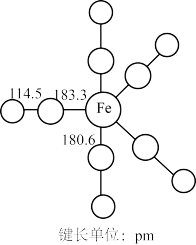
(2)下列说法正确的是___________。
| A.中心Fe原子可能采取sp3杂化 | B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于Ⅷ族,属于d区元素 | D.制备Fe(CO)5应在隔绝空气的条件下进行 |
22-23高二上·上海·期末 查看更多[4]
上海市嘉定区第一中学2022-2023学年高二上学期期末(等级)考试化学试题(已下线)3.4.1 配合物与超分子(巩固)(已下线)专题02 分子结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)(已下线)专题03 晶体结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)
更新时间:2023-06-19 16:04:26
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
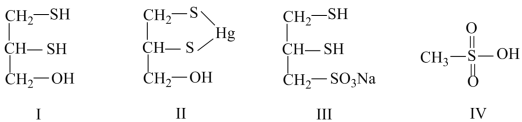
(1)1mol化合物Ⅰ含有_______ mol σ键。
(2)基态硫原子价层电子排布式为_______ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)汞的原子序数为80,位于元素周期表第_______ 周期第ⅡB族。
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)1mol化合物Ⅰ含有
(2)基态硫原子价层电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)汞的原子序数为80,位于元素周期表第
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】查阅教材附录中键长和键能的数据,将 、
、 、
、 、
、 四种气态氢化物按稳定性由强到弱排序并说明原因
四种气态氢化物按稳定性由强到弱排序并说明原因____ 。
 、
、 、
、 、
、 四种气态氢化物按稳定性由强到弱排序并说明原因
四种气态氢化物按稳定性由强到弱排序并说明原因
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】O3分子内部存在“三中心四电子”的离域π键(如图虚线部分所示),由于O3分子的中心氧原子较端位氧原子多提供一个电子,故中心氧原子带部分正电荷,端位氧原子带部分负电荷。___________ (选填“是”或“否”),解释O3在水中溶解度大于O2的可能原因。___________
2.判断并解释反应2O3=3O2是否属于氧化还原反应___________ 。
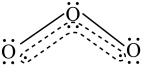
2.判断并解释反应2O3=3O2是否属于氧化还原反应
您最近一年使用:0次
【推荐2】下列反应曾用于检测司机是否酒后驾驶:2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为_________ ;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________ (填元素符号)。
(2)CH3COOH中C原子轨道杂化类型为______________ ;1molCH3COOH分子中含有σ键的数目为 ______ 。
(3)与H2O互为等电子体的一种阳离子为________ (填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为___________ 。
(1)Cr3+基态核外电子排布式为
(2)CH3COOH中C原子轨道杂化类型为
(3)与H2O互为等电子体的一种阳离子为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,基态Ti原子核外有____ 个运动状态不同的电子,在基态Fe2+中,电子占据的能量最高的轨道为___ 。
(2)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs),硫化镉(CdS)薄膜电池等。镉Cd周期表位于第五周期与Zn同族,则Cd的价电子排布式为:____ ,第一电离能:Ca____ As(填“大于”或“小于”或“等于”;H2S分子的VSEPR模型为____ 。
(3)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。NF3的沸点比NH3更低,原因是____ 。
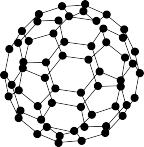
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图所示,分子中碳原子轨道的杂化类型为____ ;1个C60分子中σ键的数目为____ 个。
(1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,基态Ti原子核外有
(2)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs),硫化镉(CdS)薄膜电池等。镉Cd周期表位于第五周期与Zn同族,则Cd的价电子排布式为:
(3)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。NF3的沸点比NH3更低,原因是
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图所示,分子中碳原子轨道的杂化类型为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】镍的氨合离子 中存在的化学键有
中存在的化学键有_______ (填字母)。
A.离子键 B.共价键 C.配位键 D.氢键 E. 键 F.
键 F. 键
键
 中存在的化学键有
中存在的化学键有A.离子键 B.共价键 C.配位键 D.氢键 E.
 键 F.
键 F. 键
键
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】向Ti4+的水溶液中加入双氧水,得到产物[Ti(O2)(H2O)4]2+,则产物中含有的化学键类型有___ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】C60、金刚石和石墨的结构模型如图所示(石墨仅表示其中的一层结构):
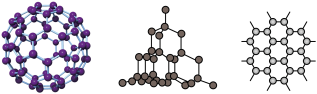
(1)C60、金刚石和石墨三者的关系互为___________。
(2)硅晶体的结构跟金刚石相似,1 mol硅晶体中含有硅硅单键的数目约是____________ NA个。二氧化硅的结构相当于在硅晶体结构中每个硅硅单键之间插入一个氧原子。二氧化硅的空间网状结构中,硅、氧原子形成的最小环上氧原子数目是___________ 。
(3)石墨层状结构中,平均每个正六边形拥有的碳原子个数是个___________ 。

(1)C60、金刚石和石墨三者的关系互为___________。
| A.同分异构体 | B.同素异形体 | C.同系物 | D.同位素 |
(3)石墨层状结构中,平均每个正六边形拥有的碳原子个数是个
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】C和Si元素在化学中占有极其重要的地位。
(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为___________ ,微粒间存在的作用力是___________ ,SiC和晶体Si的熔沸点高低顺序是___________ 。
(2)SiO2属于___________ 晶体,CO2属于___________ 晶体,所以熔点CO2___________ SiO2(填“<”“=”或“>”)。
(3)二氧化硅、CO2两种晶体的组成微粒分别是___________ 、___________ ,熔化时克服的微粒间的作用力是___________ 、___________ 。
(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
(2)SiO2属于
(3)二氧化硅、CO2两种晶体的组成微粒分别是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.有下列物质:①Na2O ②NaOH ③NH4Cl ④CO2 ⑤H2S ⑥Ar
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是___________ ,属于共价化合物的是___________ 。
(2)只含有离子键的是___________ ,既含有离子键又含有共价键的是___________ 。
(3)不存在化学键的是______________ 。
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于_ 晶体,KBr可能属于__ 晶体。
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于__ 晶体,写出BaCl2的电子式:____ 。
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是____ 晶体,而SiC可能是____ 晶体。
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;_____ 。
(8)______MnO +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;_____
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是
(2)只含有离子键的是
(3)不存在化学键的是
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;
(8)______MnO
 +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
您最近一年使用:0次

 的键角小于
的键角小于 的,分析原因
的,分析原因

